Données techniques
| Formule | C29H43NO4S |
||||||||||
| Poids moléculaire | 501.72 | Numéro CAS | 166518-60-1 | ||||||||
| Solubilité (25°C)* | In vitro | DMSO (chauffé au bain-marie à 50 °C) | 100 mg/mL (199.31 mM) | ||||||||
| Ethanol | 16 mg/mL (31.89 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||
Préparation des solutions mères
Activité biologique
| Description | Avasimibe inhibe ACAT avec une IC50 de 3,3 μM, et inhibe également les isoenzymes humaines P450 CYP2C9, CYP1A2 et CYP2C19 avec des IC50 de 2,9 μM, 13,9 μM et 26,5 μM, respectivement. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||||
| In vitro | L'avasimibe à une concentration de 1 μg/mL provoque une réduction du cholestérol total (TC) et du cholestérol estérifié (EC) en inhibant la liaison des LDL et en diminuant le nombre de récepteurs « scavenger » pendant la formation des cellules spumeuses dans les macrophages dérivés de monocytes humains (HMMs). Ce composé à une concentration de 2 μg/mL améliore l'efflux de cholestérol des cellules spumeuses HMM établies pré-incubées avec 10 μg/ml de LDL. Il inhibe l'accumulation de Lipoprotéine(a) dans le milieu de culture d'hépatocytes de singe primaires de manière dose-dépendante avec une inhibition de 11,9 % à 31,3 %, le changement étant principalement associé à une diminution de l'ApoA. Ce produit chimique incubé à des concentrations de 10 nM, 1 μM et 10 μM pendant 24 heures dans des cellules HepG2 réduit la sécrétion d'ApoB dans les milieux de 25 %, 27 % et 43 %, respectivement. Il diminue la sécrétion d'ApoB par une dégradation intracellulaire accrue de l'ApoB plutôt que par une synthèse diminuée de l'ApoB. Le composé inhibe l'ACTC avec une IC50 de 3,3 μM dans les macrophages IC-21 en tenant compte de la concentration totale de l'inhibiteur dans l'échantillon d'essai. Il inhibe les isoenzymes humaines P450 CYP2C9, CYP1A2 et CYP2C19 avec des IC50 de 2,9 μM, 13,9 μM et 26,5 μM, respectivement. Cet inhibiteur inhibe l'expression d'ACAT-1 et la synthèse des esters de cholestérol dans les lignées cellulaires de gliome. Il inhibe la croissance des cellules de gliome en induisant un arrêt du cycle cellulaire et l'apoptose due à l'activation de la caspase-8 et de la caspase-3. |
||||||||
| In vivo | L'avasimibe réduit significativement les niveaux de Lipoprotéine(a) et de cholestérol total chez neuf singes mâles sains soumis à un régime alimentaire normal et traités oralement avec CI-1011 à 30 mg/kg par jour pendant 3 semaines ; les niveaux de Lipoprotéine(a) et de cholestérol total diminuent respectivement à 68 et 73 % des niveaux de contrôle. Ce composé diminue le cholestérol total principalement en raison d'une réduction des lipoprotéines de basse densité (LDL). Il diminue la charge de plaques amyloïdes dans le cortex et l'hippocampe et réduit les niveaux d'Abeta40 et d'Abeta42 insolubles et de fragments C-terminaux de la protéine précurseur de l'amyloïde (APP) dans les extraits cérébraux chez de jeunes souris transgéniques humaines APP. Cette substance chimique réduit les plaques amyloïdes diffuses par suppression de l'astrogliose et activation microgliale améliorée chez les souris transgéniques humaines APP âgées. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
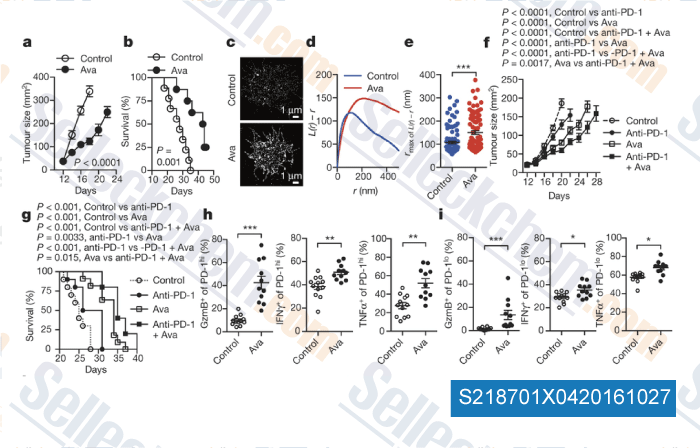
-
, , Nature, 2016, 531(7596):651-5.
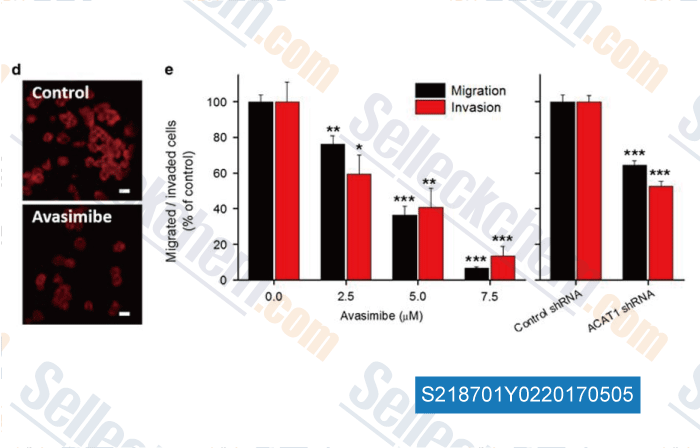
-
Données de [ , , Oncogene, 2016, 35(50):6378-6388 ]
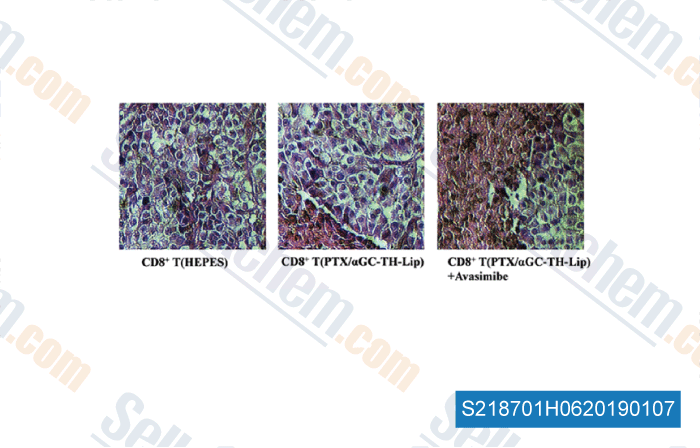
-
Données de [ , , Nanomedicine, 2018, 14(8):2541-2550 ]
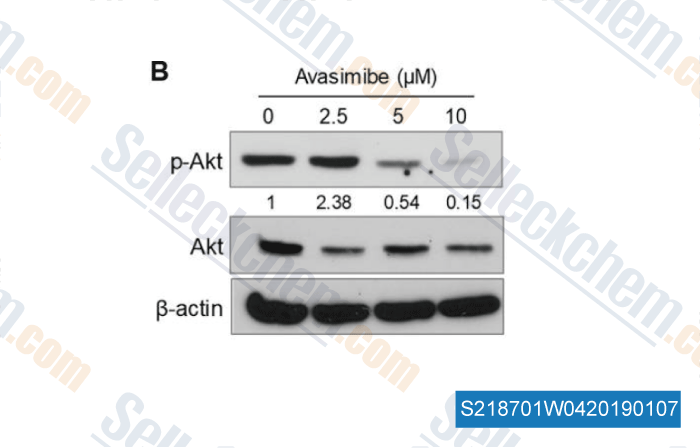
-
Données de [ , , PLoS One, 2018, 13(2):e0193318 ]
Sellecks Avasimibe A été cité par 25 Publications
| Functional characterization of genetic variants affecting the intracellular domains of ATP-binding cassette transporter A1 (ABCA1) [ J Lipid Res, 2025, 66(8):100854] | PubMed: 40617357 |
| Antioxidant interventions reduced cytokine-induced pyroptosis of peripheral MAIT cells in patients with HBV-related cirrhosis [ Hepatol Commun, 2025, 9(6)e0714] | PubMed: 40377492 |
| Specific activation of the integrated stress response uncovers regulation of central carbon metabolism and lipid droplet biogenesis [ Nat Commun, 2024, 15(1):8301] | PubMed: 39333061 |
| Stimulation of neutral lipid synthesis via viral growth factor signaling and ATP citrate lyase during vaccinia virus infection [ J Virol, 2024, 98(11):e0110324] | PubMed: 39475274 |
| An ACAT inhibitor suppresses SARS-CoV-2 replication and boosts antiviral T cell activity [ PLoS Pathog, 2023, 19(5):e1011323] | PubMed: 37134108 |
| Metabolic interventions improve HBV envelope-specific T-cell responses in patients with chronic hepatitis B [ Hepatol Int, 2023, 10.1007/s12072-023-10490-4] | PubMed: 36976426 |
| Cholesterol mediated ferroptosis suppression reveals essential roles of Coenzyme Q and squalene [ Commun Biol, 2023, 6(1):1108] | PubMed: 37914914 |
| Avasimibe Alleviates Disruption of the Airway Epithelial Barrier by Suppressing the Wnt/β-Catenin Signaling Pathway [ Front Pharmacol, 2022, 13:795934] | PubMed: 35222024 |
| Targeting cholesterol esterification as a novel immune checkpoint in viral infections and cancer [ UCL-, 2022, ] | PubMed: None |
| Targeting human Acyl-CoA:cholesterol acyltransferase as a dual viral and T cell metabolic checkpoint [ Nat Commun, 2021, 12(1):2814] | PubMed: 33990561 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
