Données techniques
| Formule | C25H26ClN5O3 |
||||||
| Poids moléculaire | 479.96 | Numéro CAS | 468740-43-4 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 96 mg/mL (200.01 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | BMS-536924 (CS-0117) est un inhibiteur d'IGF-1R/IR compétitif de l'ATP avec une CI50 de 100 nM/73 nM, une activité modeste pour Mek, Fak et Lck avec très peu d'activité pour Akt1, MAPK1/2. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | BMS-536924 inhibe également FAK et Lck avec des CI50 de 150 nM et 341 nM, respectivement. Ce composé inhibe la prolifération cellulaire et perturbe la phosphorylation d'Akt et de MAPK. Il inhibe la signalisation IGF-1R stimulée par IGF-I dans les cellules MCF10A et bloque l'activité constitutive d'IGF-1R dans les CD8-IGF-1R-MCF10A. La préincubation des cellules MCF10A avec 1 μM de cette substance chimique bloque complètement la capacité d'IGF-I à stimuler la phosphorylation d'IGF-1R. La stimulation d'IGF-I entraîne une augmentation de la phosphorylation d'ERK1/2, de GSK3β et d'Akt. Ce composé inhibe cette phosphorylation induite par le ligand. Le traitement des cellules CD8-IGF-1R-MCF10A avec cet inhibiteur entraîne une inhibition dose-dépendante de la phosphorylation avec une inhibition partielle à 0,01 μM et 0,1 μM, mais une inhibition complète du récepteur à une concentration de 1 μM. L'inhibition maximale d'IGF-1R phosphorylé est observée dès 10 minutes après l'incubation. Il conserve sa capacité à inhiber la phosphorylation d'IGF-1R pendant 48 heures. L'ajout de cet agent inhibe la phosphorylation d'Akt de manière dépendante du temps, à partir de 1 heure. À 48 heures, l'activation d'Akt est complètement bloquée. Le traitement avec ce composé montre une activité antiproliférative dans un panel de lignées cellulaires cancéreuses, y compris les cellules TC32, HT1080/S, SK-LMS-1, H513 et CTR. pIGF-1R/pIR est activé lors de la stimulation par IGF-I/insuline et l'activation est inhibée par cette substance chimique à des puissances similaires dans les lignées cellulaires Rh41 et Rh36. L'expression de la mort cellulaire programmée 4 (PDCD4), le clivage de la poly(ADP-ribose) polymérase (PARP) et de la caspase-3 sont régulés à la hausse dans les cellules Rh41 traitées avec cet inhibiteur. | |||||||||||
| In vivo | L'administration orale de BMS-536924 à 100-300 mpk inhibe fortement le modèle tumoral IGR-1R Sal. Une efficacité est également observée dans le modèle de carcinome colorectal humain non modifié Colo205. L'administration orale de ce composé une fois par jour (100-300 mpk) ou deux fois par jour (50, 100 mpk) démontre une activité antitumorale dans ce modèle tumoral. Le test d'hyperglycémie provoquée par voie orale (OGTT) montre que 100 mpk (b.i.d.) provoque une élévation significative des niveaux de glucose après un défi au glucose. Les paramètres pharmacocinétiques de cette substance chimique, administrée par voie orale dans du poly(éthylène glycol) 400 et de l'eau (80:20 v/v), sont déterminés chez la souris, le rat, le chien et le singe. Une bonne biodisponibilité est évidente chez toutes les espèces. Une pharmacocinétique non linéaire significative est observée chez les rongeurs à des doses p.o. croissantes. Ce composé réduit le volume des xénogreffes tumorales des cellules CD8-IGF-1R-MCF10A après deux semaines de traitement (100 mg/kg) à 76 %. L'administration orale de 70 mg/kg de cette substance chimique inhibe significativement la croissance tumorale (cellules TGBC-1TKB) inoculées chez des souris nues. Elle régule positivement l'apoptose dans les tumeurs xénogreffées. Le traitement n'a pas d'effets indésirables sur le poids corporel des souris ou les niveaux de glucose au moment du décès, suggérant une toxicité tolérable. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
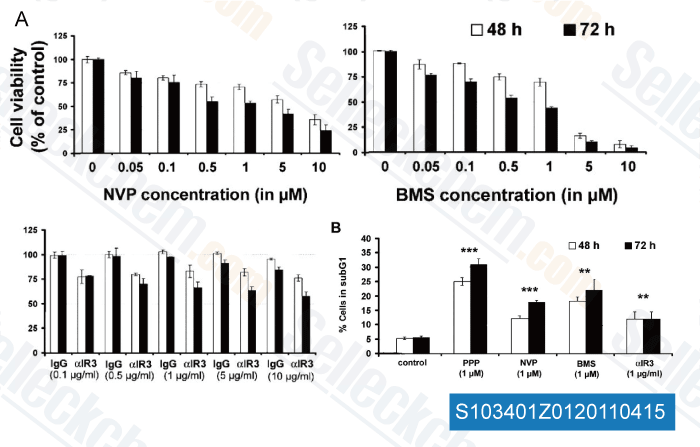
-
Données de [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
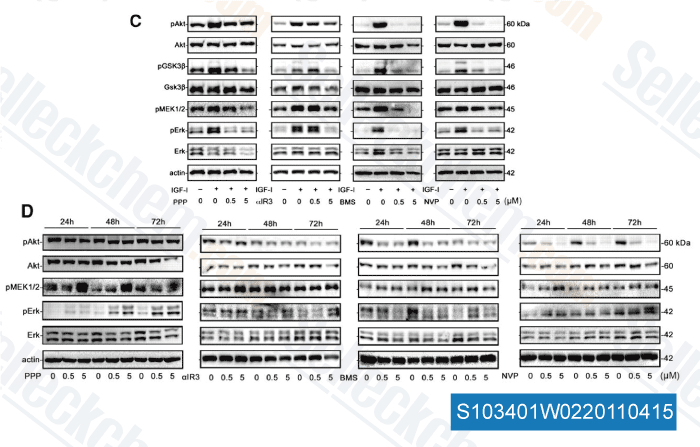
-
Données de [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
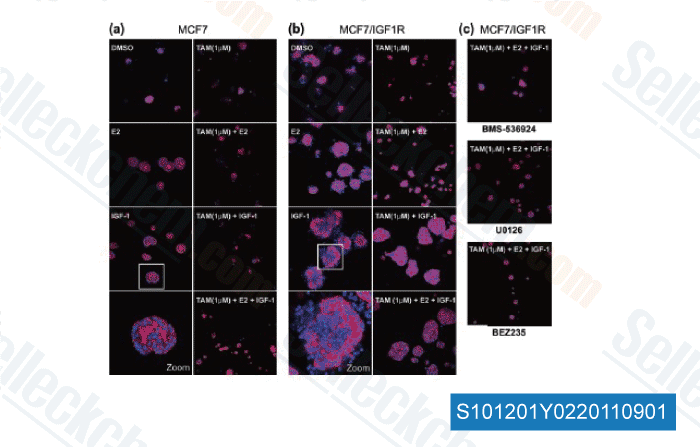
-
Données de [ Breast Cancer Res , 2011 , 13, R52 ]
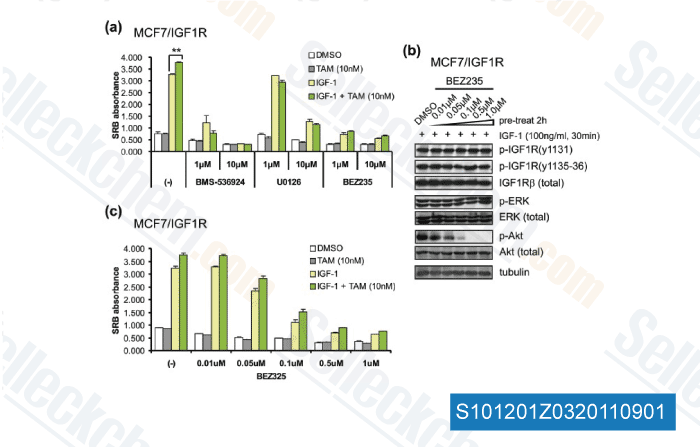
-
Données de [ Breast Cancer Res , 2011 , 13, R52 ]
Sellecks BMS-536924 A été cité par 27 Publications
| Haploinsufficiency of miR-143 and miR-145 reveal targetable dependencies in resistant del(5q) myelodysplastic neoplasm [ Leukemia, 2025, 39(4):917-928] | PubMed: 40000845 |
| Inhibition of Selenoprotein I promotes ferroptosis and reverses resistance to platinum chemotherapy by impairing Akt phosphorylation in ovarian cancer [ MedComm (2020), 2024, 5(12):e70033] | PubMed: 39669976 |
| High-Content and High-Throughput Clonogenic Survival Assay Using Fluorescence Barcoding [ Cancers -Basel), 2023, 15(19)4772] | PubMed: 37835466 |
| SFRP4+ stromal cell subpopulation with IGF1 signaling in human endometrial regeneration [ Cell Discov, 2022, 8(1):95] | PubMed: 36163341 |
| Multi-omics characterization of autophagy-related molecular features for therapeutic targeting of autophagy [ Nat Commun, 2022, 13(1):6345] | PubMed: 36289218 |
| FER-mediated phosphorylation and PIK3R2 recruitment on IRS4 promotes AKT activation and tumorigenesis in ovarian cancer cells [ Elife, 2022, 11e76183] | PubMed: 35550247 |
| Exosomes from cisplatin-induced dormant cancer cells facilitate the formation of premetastatic niche in bone marrow through activating glycolysis of BMSCs [ Front Oncol, 2022, 12:922465] | PubMed: 36568212 |
| Intermittent parathyroid hormone improves orthodontic retention via insulin-like growth factor-1 [ Oral Dis, 2021, 27(2):290-300] | PubMed: 32608117 |
| Manganese Acts upon Insulin/IGF Receptors to Phosphorylate AKT and Increase Glucose Uptake in Huntington's Disease Cells [ Mol Neurobiol, 2020, 57(3):1570-1593] | PubMed: 31797328 |
| Loss of N-Glycanase 1 Alters Transcriptional and Translational Regulation in K562 Cell Lines [ G3 (Bethesda), 2020, 4;10(5):1585-1597] | PubMed: 32265286 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
