Données techniques
| Formule | C17H14ClF2IN2O2 |
||||||||||
| Poids moléculaire | 478.67 | Numéro CAS | 212631-79-3 | ||||||||
| Solubilité (25°C)* | In vitro | DMSO | 96 mg/mL (200.55 mM) | ||||||||
| Ethanol | 14 mg/mL (29.24 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||
Préparation des solutions mères
Activité biologique
| Description | Le PD184352 (CI-1040) est un inhibiteur non compétitif de MEK1/2 de l'ATP avec une IC50 de 17 nM dans les essais cellulaires, 100 fois plus sélectif pour MEK1/2 que pour MEK5. Ce composé induit sélectivement l'apoptose. | ||||
|---|---|---|---|---|---|
| Cibles |
|
||||
| In vitro | Le traitement au CI-1040 produit une réduction des niveaux de pMAPK dans plusieurs cellules tumorales, y compris les carcinomes du côlon 26, pancréatiques BX-PC3, cervicaux A431, côlon HT-29, mammaires ZR-25-1 et ovariens SKOV-3. Ce traitement ne inhibe pas la phosphorylation de la Jun kinase, de la p38 kinase ou de l'Akt, ce qui indique qu'il cible spécifiquement MEK. L'inhibition de l'activation de MAPK par ce produit chimique empêche la progression du cycle cellulaire et induit un blocage en phase G1. L'IC50 pour l'inhibition de MEK1 par cet inhibiteur est de 0,3 μM, 15 fois plus élevée que la concentration requise pour inhiber l'activation de ERK2 induite par l'EGF dans les cellules Swiss 3T3. Ces résultats indiquent que cet agent exerce ses effets sur les cellules en supprimant l'activation de MKK1, et non en bloquant son activité. 2 nM de ce composé inhibent l'activation de MKK1 dans les cellules Swiss 3T3 de 50%, tandis qu'une concentration 100 fois plus élevée inhibe MEK1 in vitro. Il inhibe également la phosphorylation de MEK1 catalysée par Raf sans aucun effet sur la phosphorylation de la protéine basique de la myéline catalysée par Raf. Ce produit chimique inhibe 86% de la croissance des cellules de carcinome papillaire de la thyroïde (PTC) avec le réarrangement RET/PTC1 à 10μM par rapport aux cellules traitées uniquement avec du DMSO. Il montre une puissante inhibition des cellules PTC (mutation BRAF) avec une GI50 de 52 nM, mais une faible activité sur le type de réarrangement RET/PTC1 avec une GI50 de 1,1 μM. Une recherche récente indique que cet agent augmente l'effet apoptotique du BMS-214662 dans une lignée cellulaire de crise blastique de LMC, K562, et dans les cellules primaires de LMC CD34+ en phase chronique. | ||||
| In vivo | L'administration orale de CI-1040 altère la croissance des xénogreffes de tumeurs coliques de souris et humaines avec une large gamme de doses de 48 à 200 mg/kg par dose, mais pas de la leucémie P388. Ce composé inhibe les xénogreffes tumorales des cellules de CPT portant une mutation BRAF avec une réduction de 31,3 %, et portant le réarrangement RET/PTC1 avec une réduction de 47,5 % par rapport aux souris non traitées (véhicule) après 3 semaines d'administration orale (300 mg/kg/jour). Aucun effet toxique n'est observé chez les souris traitées avec ce produit chimique. L'exposition transitoire de tumeurs mammaires à ce composé et à l'UCN-01 provoque la mort des cellules tumorales in vivo et une suppression prolongée de la repousse tumorale. Le traitement combiné avec ce produit chimique (25 mg/kg) et l'UCN-01 (0,1-0,2 mg/kg) réduit significativement la croissance tumorale des MDA-MB-231 et supprime largement celle des MCF7 chez des souris athymiques implantées, tandis qu'un traitement simple n'a aucune activité significative. La combinaison de médicaments entraîne une mort profonde des cellules tumorales qui est corrélée à une réduction de la phosphorylation d'ERK1/2 et de l'immunoréactivité de Ki67 et de CD31. | ||||
| Caractéristiques | Premier inhibiteur de MEK à commencer le développement clinique. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client

-
Données de [ J Natl Cancer Inst , 2012 , 104(21), 1673-9 ]

-
Données de [ J Natl Cancer Inst , 2012 , 104(21), 1673-9 ]

-
Données de [ Science , 2011 , 331, 912-916 ]
-
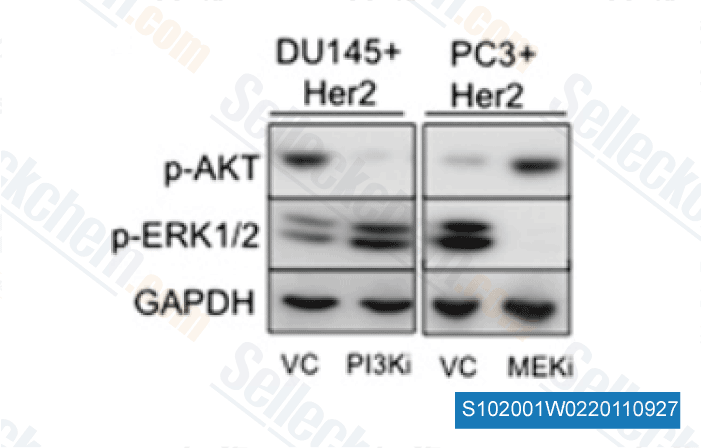
Données de [ Proc Natl Acad Sci U S A , 2011 , 108, 16392-7 ]
Sellecks PD184352 (CI-1040) A été cité par 144 Publications
| Transcriptional repressor Capicua is a gatekeeper of cell-intrinsic interferon responses [ Cell Host Microbe, 2025, 33(4):512-528.e7] | PubMed: 40132591 |
| Establishing Bovine Embryonic Stem Cells and Dissecting Their Self-Renewal Mechanisms [ Int J Mol Sci, 2025, 26(8)3536] | PubMed: 40331984 |
| Keratinocyte-derived VEGF-A is an essential pro-migratory autocrine mediator, acting through the KDR/GEF-H1/RhoA pathway [ Front Cell Dev Biol, 2025, 13:1601887] | PubMed: 40746859 |
| Inhibition of Retinoic Acid Receptor Gamma Improves Bovine Embryo Development [ Vet Sci, 2025, 12(10)924] | PubMed: 41150070 |
| GRB2 stabilizes RAD51 at reversed replication forks suppressing genomic instability and innate immunity against cancer [ Nat Commun, 2024, 15(1):2132] | PubMed: 38459011 |
| eIF4F controls ERK MAPK signaling in melanomas with BRAF and NRAS mutations [ Proc Natl Acad Sci U S A, 2024, 121(44):e2321305121] | PubMed: 39436655 |
| Dietary protein restriction regulates skeletal muscle fiber metabolic characteristics associated with the FGF21-ERK1/2 pathway [ iScience, 2024, 27(3):109249] | PubMed: 38450157 |
| MEK1/2 inhibition decreases pro-inflammatory responses in macrophages from people with cystic fibrosis and mitigates severity of illness in experimental murine methicillin-resistant Staphylococcus aureus infection [ Front Cell Infect Microbiol, 2024, 14:1275940] | PubMed: 38352056 |
| Forchlorfenuron-Induced Mitochondrial Respiration Inhibition and Metabolic Shifts in Endometrial Cancer [ Cancers (Basel), 2024, 16(5)976] | PubMed: 38473335 |
| The NF-κB-HE4 axis: A novel regulator of HE4 secretion in ovarian cancer [ PLoS One, 2024, 19(12):e0314564] | PubMed: 39621651 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
