Données techniques
| Formule | C23H27N7O3S2 |
||||||
| Poids moléculaire | 513.64 | Numéro CAS | 957054-30-7 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 100 mg/mL (194.68 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | Pictilisib (GDC-0941, RG7321) est un puissant inhibiteur de PI3Kα/δ avec une IC50 de 3 nM dans les essais sans cellules, avec une sélectivité modeste contre p110β (11 fois) et p110γ (25 fois). Pictilisib (GDC-0941) induit l'autophagy et l'apoptosis. Phase 2. | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||||||
| In vitro | Pictilisib (GDC-0941) est équipotent contre PI3Kα et PI3Kδ ainsi que contre les mutants de PI3Kα E545-K et H1047-R, affichant des niveaux de sélectivité modestes contre PI3Kβ (10 fois) et PI3Kγ (25 fois), et des niveaux de sélectivité plus élevés contre les membres des classes II, III et IV de PI3K, y compris C2β, Vps34, DNA-PK et mTOR. Il inhibe puissamment la phosphorylation d'Akt dans les cellules U87MG, PC3 et MDA-MB-361 avec des IC50 de 46 nM, 37 nM et 28 nM, respectivement. Ce composé inhibe la prolifération des cellules U87MG, A2780, PC3 et MDA-MB-361 avec des IC50 de 0,95 μM, 0,14 μM, 0,28 μM et 0,72 μM, respectivement. Il inhibe la prolifération des cellules amplifiées en HER2 qui portent des mutations PIK3CA avec une IC50 de <500 nM, et inhibe efficacement la prolifération et la viabilité des cellules de cancer du sein amplifiées en HER2. Il inhibe significativement la croissance des cellules HCT116, DLD1 et HT29 avec des GI50 de 1081 nM, 1070 nM et 157 nM, respectivement. Il inhibe également la prolifération des cellules tumorales, induit l'apoptose et supprime la population de centroblastes. |
||||||||||
| In vivo | Pictilisib (GDC-0941) montre un métabolisme microsomique limité, ce qui entraîne une biodisponibilité orale de 78 % . L'administration de ce composé à 75 mg/kg/jour montre un effet inhibiteur significatif contre les xénogreffes de glioblastome humain U87MG établies chez des souris athymiques NCr femelles, avec une inhibition de la croissance tumorale de 83 %. L'administration orale de 150 mg/kg/jour inhibe la croissance des xénogreffes MDA-MB-361.1 amplifiées en HER2 chez la souris et retarde significativement la progression tumorale, en association avec une apoptose induite puissante dans les tumeurs. Le traitement avec ce composé (75 mg/kg/jour) pendant 2 semaines induit une réduction d'environ 40 % du volume tumoral des lymphomes folliculaires à cellules B spontanés développés chez les souris PTEN+/-LKB1+/hypo, accompagné d'une ablation de la phosphorylation des protéines kinases Akt, S6K et SGK (protéine kinase sérique et glucocorticoïde). |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
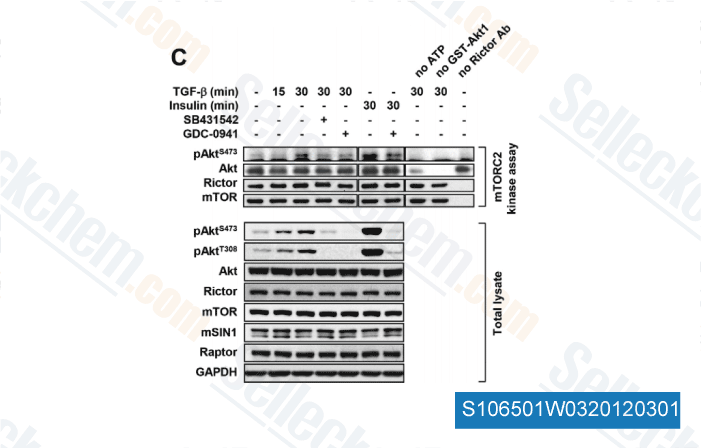
-
Données de [ J Cell Sci , 2012 , 125(Pt 5), 1259-73 ]
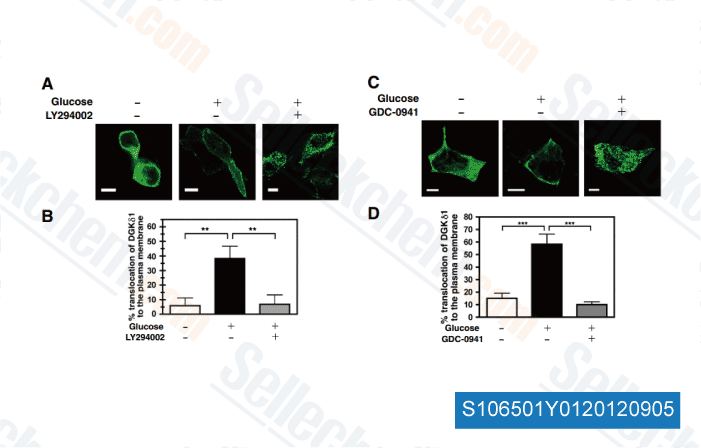
-
Données de [ Biochim Biophys Acta , 2012 , 1823, 2210-6 ]
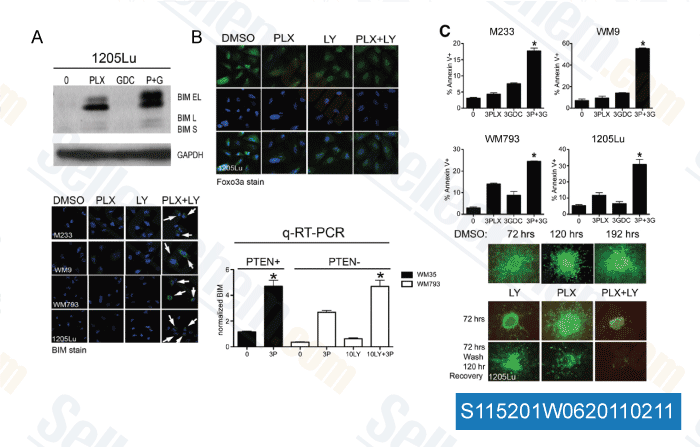
-
Données de [ Cancer Res , 2011 , 71, 2750-2760 ]
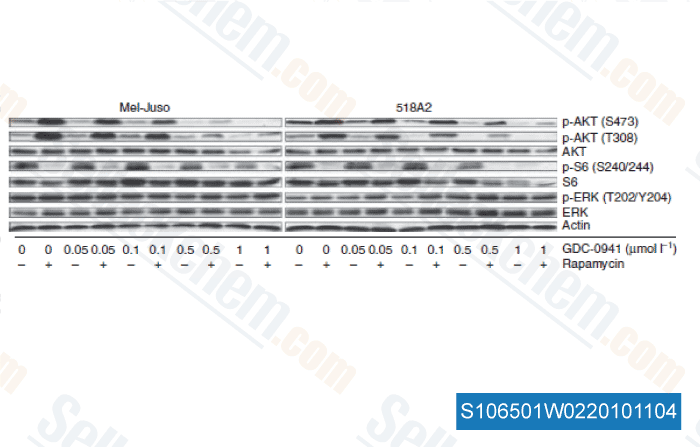
-
Données de [ J Inves Der , 2010 , 131, 495-503 ]
Sellecks Pictilisib (GDC-0941) A été cité par 461 Publications
| Targeting PI3K inhibitor resistance in breast cancer with metabolic drugs [ Signal Transduct Target Ther, 2025, 10(1):92] | PubMed: 40113784 |
| Spike-in enhanced phosphoproteomics uncovers synergistic signaling responses to MEK inhibition in colon cancer cells [ Nat Commun, 2025, 16(1):4884] | PubMed: 40419504 |
| Axial nephron fate switching demonstrates a plastic system tunable on demand [ Nat Commun, 2025, 16(1):7912] | PubMed: 40855070 |
| EGFR TKIs suppress MUC1 glycosylation through the PI3K/AKT/SP1/C1GALT1 pathway to enhance TnMUC1 CAR-T efficacy in EGFR-mutant NSCLC [ Cell Rep Med, 2025, S2666-3791(25)00272-1] | PubMed: 40562040 |
| Heterogeneous Activation of Signaling Pathways and Therapeutic Vulnerabilities in KSHV-Associated Primary Effusion Lymphoma Cell Lines [ J Med Virol, 2025, 97(8):e70534] | PubMed: 40751690 |
| Separase Inhibition Enhances Gefitinib Sensitivity of Lung Cancer via PTBP1/TAK1/RIPK1-Mediated PANoptosis [ MedComm (2020), 2025, 6(11):e70432] | PubMed: 41122447 |
| Lactate shuttle between cytotrophoblast and syncytiotrophoblast in the placenta enhances ferroptosis resistance and maintains placental homeostasis: implications for early pregnancy loss [ Cell Commun Signal, 2025, 23(1):438] | PubMed: 41088442 |
| Anthrax ET activates Rac1 and RTK signaling to induce F-actin reorganization and endothelial permeability [ iScience, 2025, 28(11):113682] | PubMed: 41158867 |
| Anti-Influenza Activity of 6BIGOE: Improved Pharmacological Profile After Encapsulation in PLGA Nanoparticles [ Int J Mol Sci, 2025, 26(9)4235] | PubMed: 40362470 |
| Cartilage Oligomeric Matrix Protein Promotes Radiation Resistance in Non-Small Cell Lung Cancer In Vitro [ Int J Mol Sci, 2025, 26(6)2465] | PubMed: 40141111 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
