Données techniques
| Formule | C20H20N4O |
||||||
| Poids moléculaire | 332.4 | Numéro CAS | 1000669-72-6 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 67 mg/mL (201.56 mM) | ||||
| Ethanol | 67 mg/mL (201.56 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | KW-2449 est un inhibiteur multi-cibles, principalement pour Flt3 avec un IC50 de 6,6 nM, modérément puissant pour FGFR1, Bcr-Abl et Aurora A; peu d'effet sur PDGFRβ, IGF-1R, EGFR. Phase 1. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | KW-2449, un inhibiteur multikinase de FLT3, ABL, ABL-T315I et Aurora kinase, est en cours d'investigation pour traiter les patients atteints de leucémie. Ce composé montre des effets inhibiteurs de croissance puissants sur les cellules leucémiques avec des mutations FLT3 par inhibition de la FLT3 kinase, entraînant une régulation à la baisse de FLT3/STAT5 phosphorylé, un arrêt en G1 et une apoptose. L'administration orale de cette substance chimique montre une inhibition de la croissance tumorale dose-dépendante et significative dans un modèle de xénogreffe muté FLT3 avec une suppression minimale de la moelle osseuse. Dans la leucémie humaine de type sauvage FLT3, il induit la réduction de l'histone H3 phosphorylée, l'arrêt en G2/M et l'apoptose. Dans la leucémie résistante à l'imatinib, cet agent contribue à la libération de la résistance par la régulation à la baisse simultanée des kinases BCR/ABL et Aurora. L'activité inhibitrice de ce composé n'est pas affectée par la présence de protéines plasmatiques humaines, telles que l'α1-glycoprotéine acide. Il possède de puissantes activités inhibitrices de croissance contre divers types de leucémie par plusieurs mécanismes d'action. Cet inhibiteur a une activité significative et justifie une étude clinique chez les patients atteints de leucémie présentant des mutations FLT3 ainsi que des mutations résistantes à l'imatinib. Les niveaux de phosphorylation de FLT3 et STAT5 sont diminués par cette substance chimique de manière dose-dépendante. De plus, il inhibe puissamment ABL-T315I, qui est associé à la résistance à l'IM, avec un IC50 de 4 nM. D'autre part, ce composé a peu d'effet sur PDGFRβ, IGF-1R, EGFR et diverses sérine/thréonine kinases même à une concentration de 1 μM. Il a de puissantes activités inhibitrices de croissance contre non seulement les cellules leucémiques exprimant FLT3/ITD, mais aussi les cellules leucémiques activées par FLT3/KDM et celles surexprimant FLT3 de type sauvage. Conformément à l'effet inhibiteur de croissance, cet agent supprime les phosphorylations de FLT3 (P-FLT3) et de sa molécule en aval phospho-STAT5 (P-STAT5) dans les cellules MOLM-13 de manière dose-dépendante. En outre, il augmente le pourcentage de cellules en phase G1 du cycle cellulaire et réduit réciproquement le pourcentage de cellules en phase S, ce qui entraîne une augmentation de la population de cellules apoptotiques. Ce composé peut déphosphoryler la kinase WT-FLT3 constitutivement active, mais n'inhibe pas la prolifération des cellules leucémiques si elles ne sont pas principalement dépendantes de la kinase FLT3. Il est rapidement absorbé et converti en un métabolite majeur M1. Des études précliniques révèlent que cette substance chimique est convertie par la monoamine oxydase-B (MAO-B) et l'aldéhyde oxydase en son métabolite majeur M1. Cet agent médiatise la cytotoxicité par l'inhibition de FLT3/ITD. C'est un inhibiteur direct de FLT3 et il induit l'inhibition de sa cible en aval STAT5. Ce composé interagit de manière synergique avec les HDACIs pour induire l'apoptose dans les cellules CML Ph+ de manière dépendante du temps et de la concentration. Il améliore synergiquement la létalité du vorinostat/SNDX275 dans les cellules CML. Ces régimes d'inhibiteurs sont actifs contre des cellules leucémiques Bcr/Abl+ résistantes à l'IM supplémentaires. Il réduit modérément la phosphorylation de l'histone H3, un indicateur de l'activité d'Aurora B, dans les cellules K562 traitées au nocodazole. | |||||||||||
| In vivo | Dans le modèle de xénogreffe tumorale MOLM-13, l'administration orale de KW-2449 pendant 14 jours montre un effet antitumoral puissant et significatif de manière dose-dépendante. | |||||||||||
| Caractéristiques | Étudié comme FLT3 inhibitor dans des essais cliniques, avec d'autres en développement précoce. |
Protocole (de référence)
| Test kinase :[2] |
|
|---|---|
| Test cellulaire : [1] |
|
| Étude animale :[3] |
|
Références
|
Validation du produit par le client
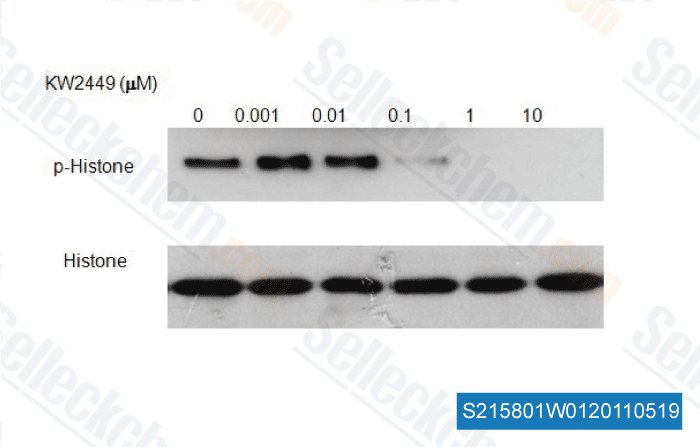
-
, , Dr. Zhang of Tianjin Medical University
Sellecks KW-2449 A été cité par 12 Publications
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| A community challenge for a pancancer drug mechanism of action inference from perturbational profile data [ Cell Rep Med, 2022, 3(1):100492] | PubMed: 35106508 |
| Phosphorylation of SHP2 at Tyr62 Enables Acquired Resistance to SHP2 Allosteric Inhibitors in FLT3-ITD-Driven AML [ Cancer Res, 2022, 82(11):2141-2155] | PubMed: 35311954 |
| KW-2449 and VPA exert therapeutic effects on human neurons and cerebral organoids derived from MECP2-null hESCs [ Stem Cell Res Ther, 2022, 13(1):534] | PubMed: 36575558 |
| Evaluation of CML TKI Induced Cardiovascular Toxicity and Development of Potential Rescue Strategies in a Zebrafish Model [ Front Pharmacol, 2021, 12:740529] | PubMed: 34733159 |
| Mechanisms of Oncogenesis in the Primary Liver Cell Cancer [ DTIC, 2021, 53] | PubMed: None |
| The Global Phosphorylation Landscape of SARS-CoV-2 Infection [ Cell, 2020, 182(3):685-712.e19] | PubMed: 32645325 |
| Synergistic Anti Leukemia Effect of a Novel Hsp90 and a Pan Cyclin Dependent Kinase Inhibitors. [ Molecules, 2020, 8;25(9) pii: E2220] | PubMed: 32397330 |
| Small-Molecule and CRISPR Screening Converge to Reveal Receptor Tyrosine Kinase Dependencies in Pediatric Rhabdoid Tumors. [ Cell Rep, 2019, 28(9):2331-2344] | PubMed: 31461650 |
| Drug Target Commons: A Community Effort to Build a Consensus Knowledge Base for Drug-Target Interactions [Tang J Cell Chem Biol, 2018, 25(2):224-229] | PubMed: 29276046 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
