Données techniques
| Formule | C17H14ClF2N3O3S |
||||||
| Poids moléculaire | 413.83 | Numéro CAS | 918505-84-7 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 83 mg/mL (200.56 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | PLX4720 est un inhibiteur puissant et sélectif de B-RafV600E avec une IC50 de 13 nM dans un essai sans cellule, aussi puissant que c-Raf-1 (mutations Y340D et Y341D), 10 fois plus sélectif pour B-RafV600E que pour B-Raf de type sauvage. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||||
| In vitro | PLX-4720 présente une sélectivité >10 fois supérieure contre le B-Raf de type sauvage, et une sélectivité >100 fois supérieure aux autres kinases telles que Frk, Src, Fak, FGFR et Aurora A avec des IC50 de 1,3 à 3,4 μM. Ce composé inhibe significativement la phosphorylation d'ERK dans les lignées cellulaires porteuses de B-RafV600E avec des IC50 de 14 à 46 nM, mais pas les cellules avec le B-Raf de type sauvage. Il inhibe significativement la croissance des lignées de cellules tumorales porteuses de l'oncogène B-RafV600E, telles que COLO205, A375, WM2664 et COLO829 avec des GI50 de 0,31 μM, 0,50 μM, 1,5 μM et 1,7 μM, respectivement. De plus, ce traitement chimique à 1 μM induit un arrêt du cycle cellulaire et une apoptose exclusivement dans les cellules 1205Lu positives pour B-RafV600E, mais pas dans les cellules C8161 de type sauvage de B-Raf. Ce traitement par composé (10 μM) induit significativement une expression de BIM >14 fois plus élevée dans les cellules PTEN+, par rapport aux lignées cellulaires PTEN- (4 fois), ce qui explique la résistance des cellules PTEN- à cette apoptose induite par des produits chimiques. | ||||||||
| In vivo | L'administration orale de PLX-4720 à 20 mg/kg/jour induit des retards et des régressions significatifs de la croissance tumorale dans les xénogreffes tumorales COLO205 dépendantes de B-RafV600E, sans effets indésirables évidents chez les souris, même à une dose de 1 g/kg. Ce composé à 100 mg/kg deux fois par jour élimine presque complètement les xénogreffes 1205Lu portant B-RafV600E, tandis qu'il n'a aucune activité contre les xénogreffes C8161 portant le B-Raf de type sauvage. Les effets antitumoraux de ce composé sont corrélés au blocage de la voie MAPK dans ces cellules abritant la mutation V600E. Ce traitement chimique à 30 mg/kg/jour inhibe significativement la croissance tumorale des xénogreffes 8505c de >90 %, et diminue considérablement les métastases pulmonaires distantes. |
Protocole (de référence)
| Test kinase :[1] |
|
|---|---|
| Test cellulaire :[1] |
|
| Étude animale :[1] |
|
Références
|
Validation du produit par le client
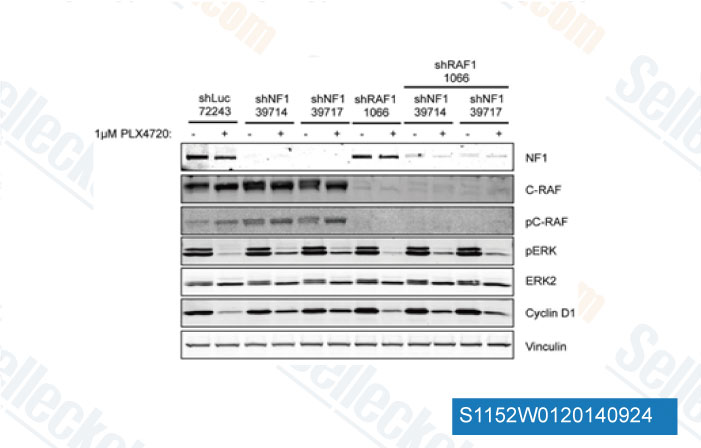
-
Données de [ Cancer Discov , 2013 , 3, 350-62 ]
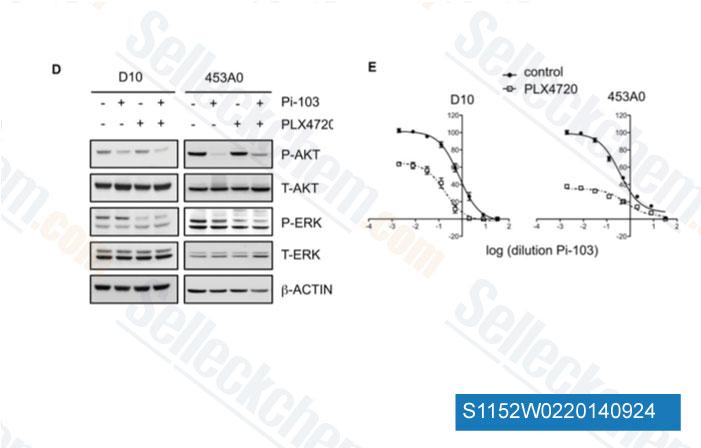
-
Données de [ Genes Dev , 2012 , 26, 1055-69 ]
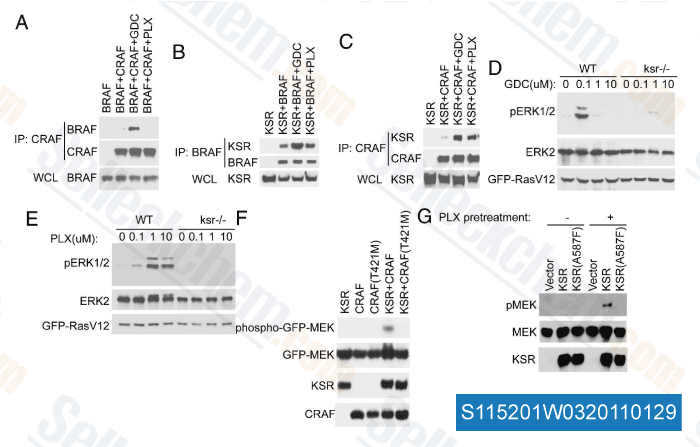
-
Données de [ Proc Natl Acad Sci USA , 2011 , 108, 6067-6072 ]
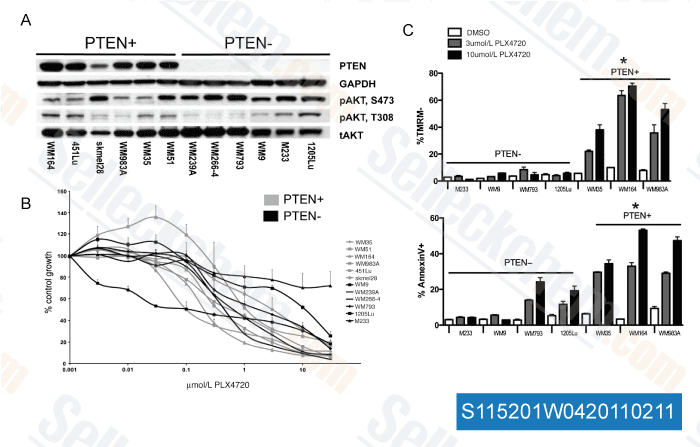
-
Données de [ Cancer Res , 2011 , 71, 2750-2760 ]
Sellecks PLX-4720 A été cité par 206 Publications
| Elevated NR2F1 underlies the persistence of invasive disease after treatment of BRAF-mutant melanoma [ J Clin Invest, 2025, 135(18)e178446] | PubMed: 40955663 |
| Elevated Transglutaminase-2 in SOX10-Deficient Melanoma Promotes Tumor Onset and Decreases Intratumoral CD4+ T Cells [ Cancer Res, 2025, 10.1158/0008-5472.CAN-24-3267] | PubMed: 40742313 |
| PTRF Confers Melanoma-Acquired Drug Resistance Through the Upregulation of EGFR [ Cell Prolif, 2025, e70086.] | PubMed: 40745979 |
| A functional comparison of two transplantable syngeneic mouse models of melanoma: B16F0 and YUMM1.7 [ Biol Open, 2025, 14(9)bio062175] | PubMed: 40878826 |
| Noncanonical role of Golgi-associated macrophage TAZ in chronic inflammation and tumorigenesis [ Sci Adv, 2025, 11(4):eadq2395] | PubMed: 39841821 |
| The ribotoxic stress response drives UV-mediated cell death [ Cell, 2024, 187(14):3652-3670.e40] | PubMed: 38843833 |
| Tracking the EMT-like phenotype switching during targeted therapy in melanoma by analyzing extracellular vesicle phenotypes [ Biosens Bioelectron, 2024, 10.1016/j.bios.2023.115819] | PubMed: 37952322 |
| Mcl-1 mediates intrinsic resistance to RAF inhibitors in mutant BRAF papillary thyroid carcinoma [ Cell Death Discov, 2024, 10(1):175] | PubMed: 38622136 |
| The ERK5 pathway in BRAFV600E melanoma cells plays a role in development of acquired resistance to dabrafenib but not vemurafenib [ FEBS Lett, 2024, 10.1002/1873-3468.14960] | PubMed: 38977937 |
| Executioner caspases restrict mitochondrial RNA-driven Type I IFN induction during chemotherapy-induced apoptosis [ Nat Commun, 2023, 14(1):1399] | PubMed: 36918588 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
