Données techniques
| Formule | C28H30CIN5O4S |
||||||
| Poids moléculaire | 568.09 | Numéro CAS | 658084-23-2 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 92 mg/mL (161.94 mM) | ||||
| Ethanol | 2 mg/mL (3.52 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | SU11274 (PKI-SU11274) est un inhibiteur sélectif de Met (c-Met) avec une IC50 de 10 nM dans les essais sans cellules, sans effets sur PGDFRβ, EGFR ou Tie2. Ce composé induit l'autophagy, l'apoptosis et l'arrêt du cycle cellulaire. | ||
|---|---|---|---|
| Cibles |
|
||
| In vitro | SU11274 présente une sélectivité supérieure à 50 fois pour Met par rapport à Flk et plus de 500 fois par rapport à d'autres Protein Tyrosine Kinase telles que FGFR-1, c-src, PDGFbR et EGFR. Ce composé inhibe la phosphorylation des régulateurs clés de la voie PI3K, y compris AKT, FKHR ou GSK3β. Le traitement avec ce produit chimique inhibe la croissance des cellules BaF3 transformées par TPR-MET de manière dose-dépendante avec une IC50 de <3 μM en l'absence d'interleukine 3, sans inhibition de la croissance des cellules BaF3 transformées par d'autres Protein Tyrosine Kinase oncogènes, y compris BCR-ABL, TEL-JAK2, TEL-ABL et TEL-PDGFβR. En plus de la croissance cellulaire, le traitement avec ce composé inhibe significativement la migration des cellules BaF3. TPR-MET de 44,8% et 80% à 1 μM et 5 μM, respectivement. Il inhibe la phosphorylation de Met dépendante de HGF ainsi que la prolifération et la motilité cellulaires dépendantes de HGF avec une IC50 de 1-1,5 μM. Dans les cellules H69 et H345 qui ont un récepteur Met fonctionnel, cet inhibiteur inhibe la croissance cellulaire induite par HGF avec une IC50 de 3,4 μM et 6,5 μM, respectivement. Il induit un arrêt du cycle cellulaire en phase G1, avec une augmentation des cellules en phase G1 de 42,4% à 70,6% à 5 μM, et induit l'apoptosis dépendante de la caspase de 24% à 1 μM. Ce composé inhibe la viabilité cellulaire dans les cellules de cancer du poumon non à petites cellules (NSCLC) exprimant c-Met avec des valeurs d'IC50 de 0,8-4,4 μM, et supprime la phosphorylation de c-Met et sa signalisation en aval induite par le facteur de croissance des hépatocytes. |
Protocole (de référence)
| Test kinase :[1] |
|
|---|---|
| Test cellulaire :[2] |
|
Références
|
Validation du produit par le client
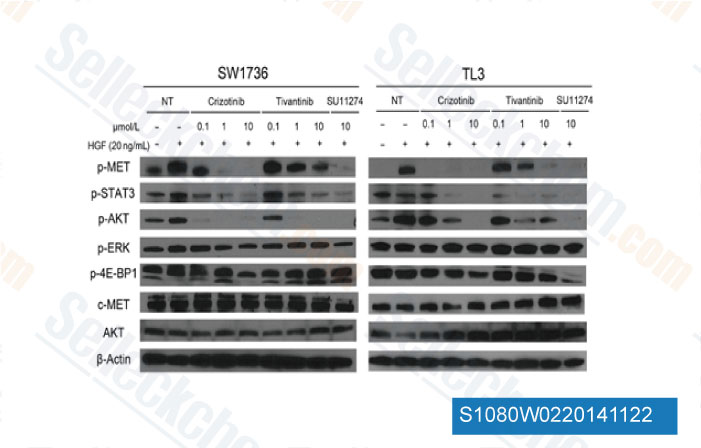
-
Données de [ Mol Cancer Ther , 2014 , 13(1), 134-43 ]
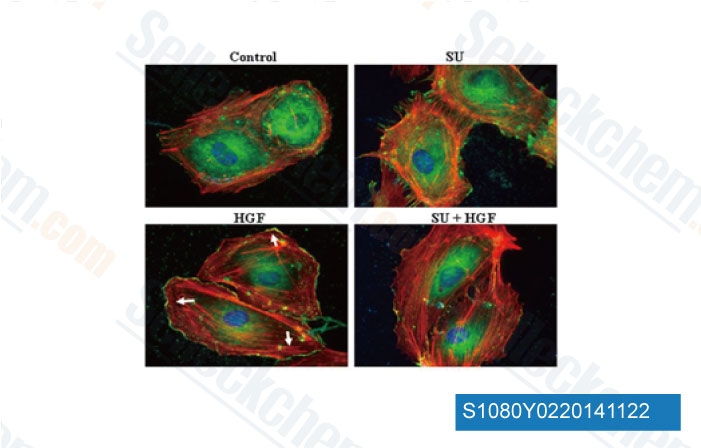
-
Données de [ J Biol Chem , 2014 , 289(19), 13476-91 ]
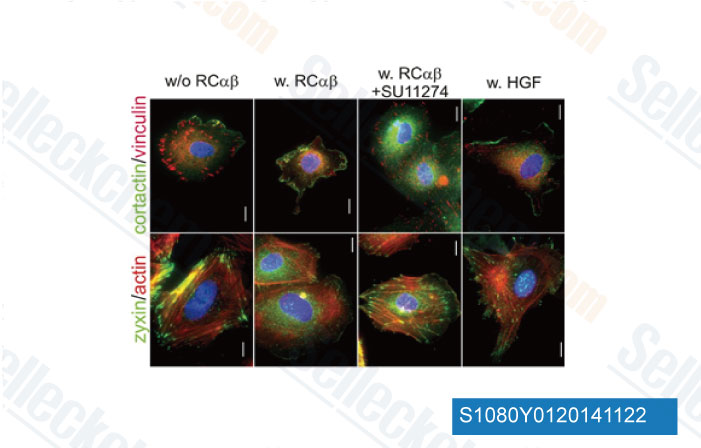
-
Données de [ Arterioscler Thromb Vasc Biol , 2013 , 33(3), 544-54 ]
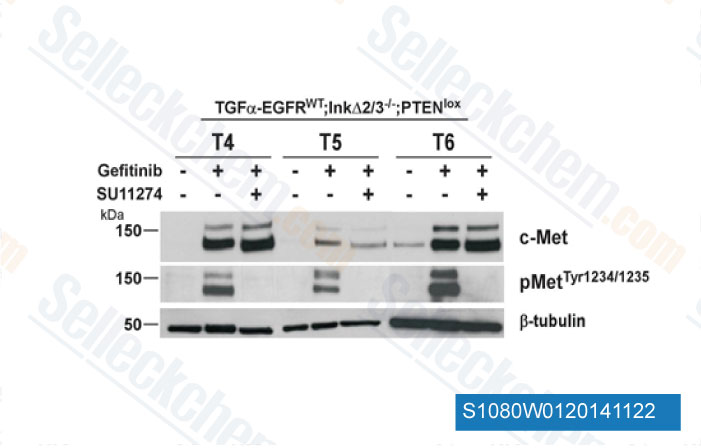
-
Données de [ Oncogene , 2012 , 31(25), 3039-50 ]
Sellecks SU11274 A été cité par 68 Publications
| Inhibition of TFF3 synergizes with c-MET inhibitors to decrease the CSC-like phenotype and metastatic burden in ER+HER2+ mammary carcinoma [ Cell Death Dis, 2025, 16(1):76] | PubMed: 39920140 |
| Establishment and characterization of a new human gallbladder cancer cell line, OCUG-2 [ World J Exp Med, 2025, 15(2):100443] | PubMed: 40546672 |
| The anti-tumor effects of AZD4547 on ovarian cancer cells: differential responses based on c-Met and FGF19/FGFR4 expression [ Cancer Cell Int, 2024, 24(1):43] | PubMed: 38273381 |
| Establishing a new human lung squamous cell carcinoma cell line, OMUL-1, expressing insulin-like growth factor 1 receptor and programmed cell death ligand 1 [ Thorac Cancer, 2024, 10.1111/1759-7714.15488] | PubMed: 39552203 |
| Hepatocyte growth factor promotes retinal pigment epithelium cell activity through MET/AKT signaling pathway [ Int J Ophthalmol, 2024, 17(5):806-814] | PubMed: 38766346 |
| Epithelial cell adhesion molecule (EpCAM) regulates HGFR signaling to promote colon cancer progression and metastasis [ J Transl Med, 2023, 21(1):530] | PubMed: 37543570 |
| Met-signaling Controls Dendritic Cell Migration in Skin by Regulating Podosome Formation and Function [ J Invest Dermatol, 2023, S0022-202X(23)00100-8] | PubMed: 36813160 |
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| Resistance to tyrosine kinase inhibitors promotes renal cancer progression through MCPIP1 tumor-suppressor downregulation and c-Met activation [ Cell Death Dis, 2022, 13(9):814] | PubMed: 36138026 |
| β2-adrenergic receptor promotes liver regeneration partially through crosstalk with c-met [ Cell Death Dis, 2022, 13(6):571] | PubMed: 35760785 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
