Données techniques
| Formule | C34H34F2N4O6 |
||||||
| Poids moléculaire | 632.65 | Numéro CAS | 849217-64-7 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 100 mg/mL (158.06 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | Foretinib est un inhibiteur ATP-compétitif de HGFR et VEGFR, principalement pour Met (c-Met) et KDR avec des IC50 de 0,4 nM et 0,9 nM dans des essais sans cellules. Moins puissant contre Ron, Flt-1/3/4, Kit (c-Kit), PDGFRα/β et Tie-2, et peu d'activité envers FGFR1 et EGFR. Phase 2. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | XL880 inhibe les Protein Tyrosine Kinases de la famille des récepteurs HGF avec des valeurs d'IC50 de 0,4 nM pour Met et 3 nM pour Ron. XL880 inhibe également KDR, Flt-1 et Flt-4 avec des valeurs d'IC50 de 0,9 nM, 6,8 nM et 2,8 nM, respectivement. XL880 inhibe la croissance des colonies de cellules B16F10, A549 et HT29 avec des IC50 de 40 nM, 29 nM et 165 nM, respectivement. Une étude récente indique que XL880 affecte différemment la croissance cellulaire dans les lignées cellulaires de cancer gastrique MKN-45 et KATO-III. XL880 inhibe la phosphorylation de MET et des molécules de signalisation en aval dans les cellules MKN-45, tandis qu'il cible GFGR2 dans les cellules KATO-III. | |||||||||||
| In vivo | Une dose unique de 100 mg/kg de XL880 par gavage oral entraîne une inhibition substantielle de la phosphorylation de Met tumorale B16F10 et de la phosphorylation des récepteurs induite par le ligand (par exemple, HGF ou VEGF) de Met dans le foie et de Flk-1/KDR dans le poumon, qui ont toutes deux persisté pendant 24 heures. Le traitement par XL880 (30-100 mg/kg, une fois par jour, gavage oral) entraîne une réduction de la charge tumorale. La charge tumorale de surface pulmonaire est réduite de 50 % et 58 % après traitement avec 30 et 100 mg/kg de XL880, respectivement. Le traitement par XL880 chez des souris porteuses de tumeurs solides B16F10 entraîne également une inhibition dose-dépendante de la croissance tumorale de 64 % et 87 % à 30 et 100 mg/kg, respectivement. Pour les deux études, l'administration de XL880 a été bien tolérée sans perte de poids corporel significative. XL880 est développé pour cibler la signalisation anormale de HGF via Met et cibler simultanément plusieurs Protein Tyrosine Kinases de récepteurs impliqués dans l'angiogenèse tumorale. XL880 a provoqué une hémorragie et une nécrose tumorale dans des xénogreffes humaines en 2 à 4 heures, et la nécrose tumorale maximale a été observée à 96 heures (après cinq doses quotidiennes), entraînant une régression complète. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
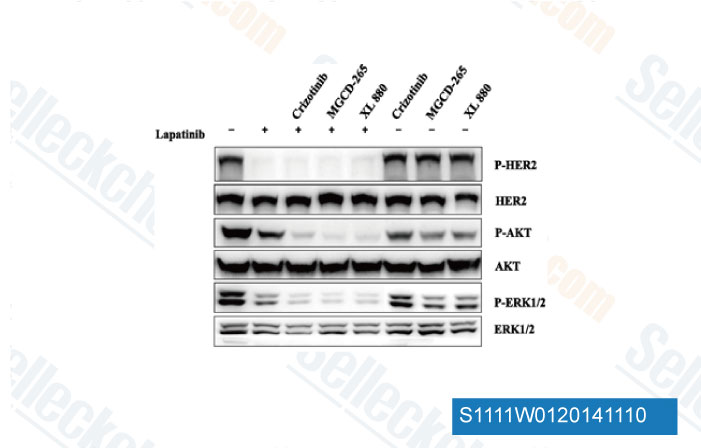
-
Données de [ Cancer Lett , 2013 , 340(1), 43-50 ]

-
, , Dr. Zhang of Tianjin Medical University

-
Données de [ , , Theranostics, 2016, 6(8):1232-43 ]
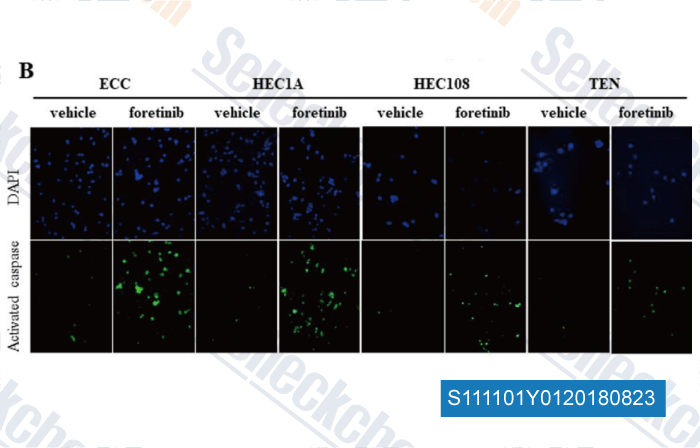
-
Données de [ , , Oncotarget, 2018, 9(32):22769-22784 ]
Sellecks Foretinib A été cité par 95 Publications
| Small molecule kinase inhibitor altiratinib inhibits brain cyst forming bradyzoites of Toxoplasma gondii [ J Microbiol, 2025, 63(2):e2409001] | PubMed: 40044130 |
| Foretinib Is Effective against Triple-Negative Breast Cancer Cells MDA-MB-231 In Vitro and In Vivo by Down-Regulating p-MET/HGF Signaling [ Int J Mol Sci, 2023, 24(1)757] | PubMed: 36614199 |
| A functional sgRNA-CRISPR screening method for generating murine RET and NTRK1 rearranged oncogenes [ Biol Open, 2023, 12(8)bio059994] | PubMed: 37470475 |
| Combined Mcl-1 and YAP1/TAZ inhibition for treatment of metastatic uveal melanoma [ Melanoma Res, 2023, 10.1097/CMR.0000000000000911] | PubMed: 37467061 |
| Investigating the mechanisms of perinatal neuron degeneration, survival, and their differentiation from neural precursor cells of the V-SVZ [ University of Toronto (Canada), 2023, ] | PubMed: None |
| A Rapid, Functional sgRNA Screening Method for Generating Murine RET and NTRK1 Fusion Oncogenes [ bioRxiv, 2023, 2023.04.06.535912] | PubMed: 37066347 |
| Adaptive c-Met-PLXDC2 Signaling Axis Mediates Cancer Stem Cell Plasticity to Confer Radioresistance-associated Aggressiveness in Head and Neck Cancer [ Cancer Res Commun, 2023, 3(4):659-671] | PubMed: 37089864 |
| Phase separation of insulin receptor substrate 1 drives the formation of insulin/IGF-1 signalosomes [ Cell Discov, 2022, 8(1):60] | PubMed: 35764611 |
| A Ctnnb1 enhancer regulates neocortical neurogenesis by controlling the abundance of intermediate progenitors [ Cell Discov, 2022, 8(1):74] | PubMed: 35915089 |
| TMUB1 is an endoplasmic reticulum-resident escortase that promotes the p97-mediated extraction of membrane proteins for degradation [ Mol Cell, 2022, S1097-2765(22)00663-3] | PubMed: 35961308 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
