Données techniques
| Formule | C30H30O8.C2H4O2 |
||||||||||
| Poids moléculaire | 578.61 | Numéro CAS | 866541-93-7 | ||||||||
| Solubilité (25°C)* | In vitro | DMSO | 100 mg/mL (172.82 mM) | ||||||||
| Ethanol | 100 mg/mL (172.82 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||
Préparation des solutions mères
Activité biologique
| Description | L'acide (R)-(-)-Gossypol (AT-101) acétique, l'énantiomère R-(-) de l'acide Gossypol acétique, se lie à Bcl-2, Bcl-xL et Mcl-1 avec des Ki de 0,32 μM, 0,48 μM et 0,18 μM dans des essais sans cellules; n'inhibe pas le domaine BIR3 et BID. L'AT-101 déclenche simultanément l'apoptosis et un type d'autophagy cytoprotecteur. Phase 2. | ||||||
|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||
| In vitro | L'AT-101 inhibe un panel de différentes hémopathies lymphoprolifératives avec une IC50 allant de 1,2 μM à 7,4 μM. L'AT-101 (10 μM) perturbe le Δψm de manière concentration- et temps-dépendante dans des lignées de lymphome diffus à grandes cellules B et de lymphome à cellules du manteau. L'AT-101 (1 μM ou 2 μM) combiné au carfilzomib (6 nM ou 10 nM) induit l'apoptose dans les lignées cellulaires HBL-2 et Granta. L'AT-101 (20 μM pendant 24 heures) entraîne une apoptose médiane de 72 % et une régulation à la baisse de Mcl-1 dans les lymphocytes de LLC en culture en suspension ainsi qu'en coculture stromale. Les cellules stromales expriment des niveaux indétectables d'antiapoptotiques, mais des niveaux élevés de protéines ERK et AKT activées et présentent peu ou pas d'apoptose avec l'AT-101. L'AT-101 induit l'apoptose de manière temps- et dose-dépendante, avec des valeurs ED50 de 1,9 mM et 2,4 mM dans les cellules Jurkat T et U937, respectivement. L'AT-101 (10 μM) combiné à la radiation (32 Gy) induit plus d'apoptose que la radiation seule et dépasse la somme des effets causés par les traitements par agent unique. L'AT-101 active SAPK/JNK de manière dose- et temps-dépendante. L'AT-101 (10 µM) induit l'apoptose par l'activation des caspases-9, -3 et -7 dans les cellules VCaP. L'AT-101 (10 µM) diminue l'expression de Bcl-2 et Mcl-1 dans les cellules VCaP. L'AT-101 (< 20 μM) est capable d'inhiber la croissance des cellules de myélome multiple malgré les effets de croissance stimulateurs fournis par les cellules stromales dans le milieu de la moelle osseuse. L'AT-101 (10 μM) induit l'apoptose dans les cellules de myélome multiple via l'activation des caspases 3, des caspases 9 et de la PARP. L'AT-101 (10 μM) favorise l'apoptose dans les cellules de myélome multiple en perturbant le rapport Bax/Bcl-2 et le potentiel de membrane mitochondrial. | ||||||
| In vivo | L'AT-101 est toujours détectable dans le plasma avec des concentrations moyennes de 0,49 μM pour le groupe 35 mg/kg et 0,39 μM pour le groupe 200 mg/kg chez des souris SCID beige porteuses d'un xénogreffe de RL-DLBCL. La concentration plasmatique maximale d'AT-101 est observée 30 minutes après l'administration du médicament aux deux niveaux de dose, le groupe 200 mg/kg montrant une concentration plasmatique moyenne presque 4 fois supérieure à celle du groupe 35 mg/kg (7,88 μM et 27,78 μM respectivement) chez des souris SCID beige. L'AT-101 (25 mg/kg à 100 mg/kg, par voie orale) entraîne indéfiniment une apparition plus précoce d'une perte de poids équivalente à plus de 10 % du poids avant traitement et la mort chez les souris SCID beige. L'AT-101 (35 mg/kg, par voie orale par jour pendant 10 jours) plus le cyclophosphamide (Cy) intrapéritonéal et le rituximab (R) intrapéritonéal montrent un contrôle significatif du volume tumoral par rapport à tout autre groupe de traitement. L'AT-101 (15 mg/kg, p.o., 5 jours/semaine) en agent unique chez des souris intactes réduit significativement le développement de la croissance tumorale VCaP par rapport aux tumeurs non traitées aux semaines 2 à 6. L'AT-101 en combinaison avec la castration chirurgicale retarde l'apparition de la croissance tumorale VCaP indépendante des androgènes par rapport aux groupes castration seule ou AT-101 seule chez les souris. |
Protocole (de référence)
| Test kinase :[1] |
|
|---|---|
| Test cellulaire :[2] |
|
| Étude animale :[2] |
|
Références
|
Validation du produit par le client
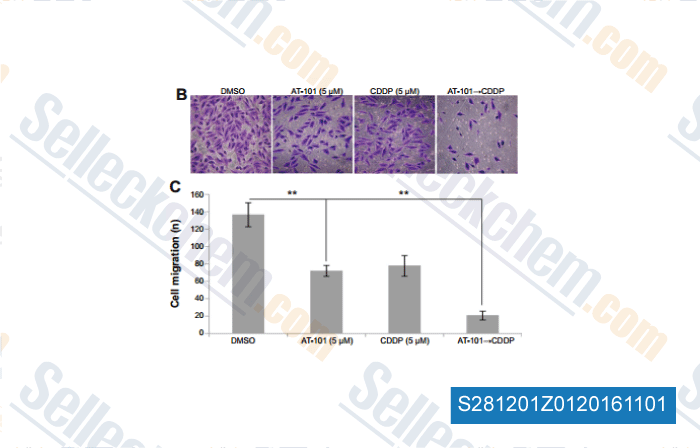
-
, , Drug Des Devel Ther, 2014, 8:2517-29.
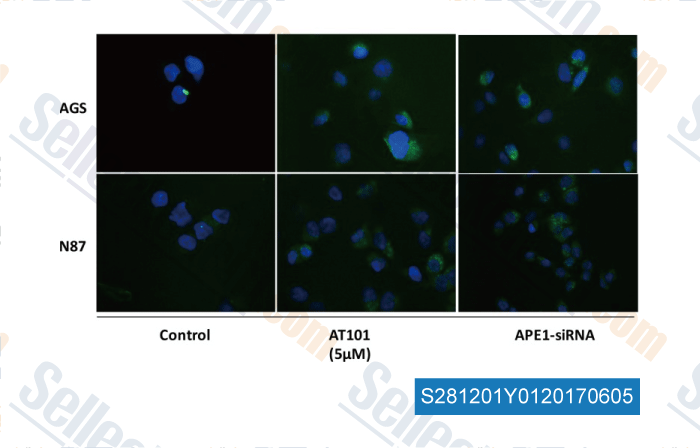
-
Données de [ , , Oncotarget, 2016, 7(23):34430-41 ]
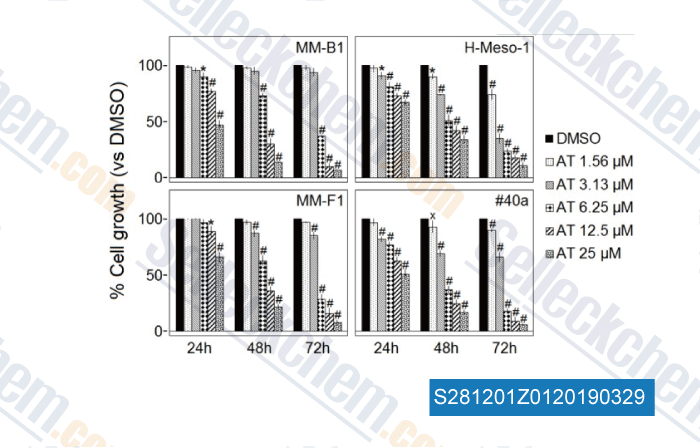
-
Données de [ , , Front Pharmacol, 2018, 9:1269 ]
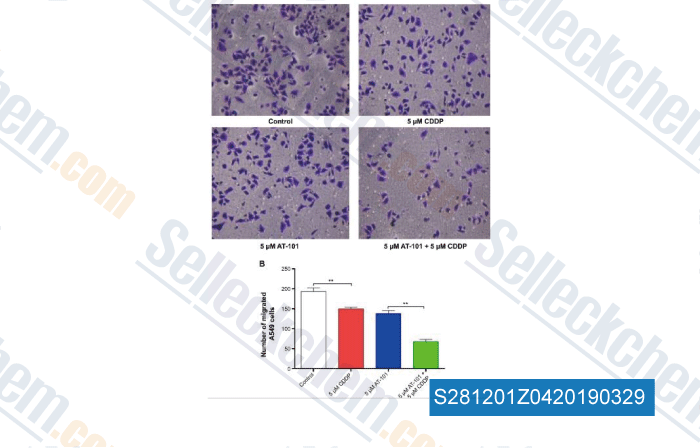
-
Données de [ , , Drug Des Devel Ther, 2015, 9:2887-910 ]
Sellecks (R)-(-)-Gossypol (AT-101) acetic acid A été cité par 20 Publications
| Follicle stimulating hormone controls granulosa cell glutamine synthesis to regulate ovulation [ Protein Cell, 2024, pwad065] | PubMed: 38167949 |
| Pharmacological Targeting of Bcl-2 Induces Caspase 3-Mediated Cleavage of HDAC6 and Regulates the Autophagy Process in Colorectal Cancer [ Int J Mol Sci, 2023, 24(7)6662] | PubMed: 37047634 |
| Exploiting ulnerabilities induced b recurrent mutations in chondrosarcoma and giant cell tumour of bone: therapeutic targeting of the altered epigenome and be [ Leiden University The Netherlands, 2023, ] | PubMed: None |
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| Lactate Dehydrogenase B Is Required for Pancreatic Cancer Cell Immortalization Through Activation of Telomerase Activity [ Front Oncol, 2022, 12:821620] | PubMed: 35669414 |
| Gossypol Acetic Acid Attenuates Cardiac Ischemia/Reperfusion Injury in Rats via an Antiferroptotic Mechanism [ Biomolecules, 2021, 11(11)1667] | PubMed: 34827665 |
| AT101 [(-)-Gossypol] Selectively Inhibits MCL1 and Sensitizes Carcinoma to BH3 Mimetics by Inducing and Stabilizing NOXA [ Cancers (Basel), 2020, 12(8):E2298] | PubMed: 32824203 |
| Using CETSA assay and a mathematical model to reveal dual Bcl-2/Mcl-1 inhibition and on-target mechanism for ABT-199 and S1. [ Eur J Pharm Sci, 2020, 142:105105] | PubMed: 31669390 |
| Comparison of putative BH3 mimetics AT-101, HA14-1, sabutoclax and TW-37 with ABT-737 in platelets. [ Platelets, 2020, 10.1080/09537104.2020.1724276] | PubMed: 32079453 |
| Effect of Exosomal APE1 on Sensitivity of NSCLC A549 Cells to Cisplatin [ Cancer Research on Prevention and Treatment, 2020, (7): 492-497] | PubMed: None |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
