Données techniques
| Formule | C30H33N7O |
||||||
| Poids moléculaire | 507.63 | Numéro CAS | 942918-07-2 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 102 mg/mL (200.93 mM) | ||||
| Ethanol | 102 mg/mL (200.93 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | GSK1070916 est un inhibiteur réversible et ATP-compétitif d'Aurora B/C avec un IC50 de 3,5 nM/6,5 nM. Il présente une sélectivité >100 fois supérieure contre le complexe Aurora A-TPX2 étroitement apparenté. Phase 1. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | GSK1070916 inhibe sélectivement Aurora B et Aurora C avec un Ki de 0,38 nM et 1,5 nM respectivement par rapport à Aurora A avec un Ki de 490 nM. L'inhibition d'Aurora B et d'Aurora C par ce composé est dépendante du temps, avec une demi-vie de dissociation enzyme-inhibiteur de >480 min et 270 min respectivement. De plus, c'est aussi un inhibiteur compétitif par rapport à l'ATP. Les cellules tumorales humaines traitées avec cet inhibiteur montrent une inhibition dose-dépendante de la phosphorylation de la sérine 10 de l'histone H3, un substrat spécifique d'Aurora B. De plus, il inhibe la prolifération des cellules tumorales avec des valeurs d'EC50 <10 nM dans plus de 100 lignées cellulaires couvrant un large éventail de types de tumeurs, avec un EC50 médian de 8 nM. Bien que ce composé ait une activité puissante contre les cellules proliférantes, un changement spectaculaire de puissance est observé dans les cellules endothéliales veineuses humaines primaires, non divisantes et normales. De plus, les cellules traitées avec cet agent n'arrêtent pas leur mitose mais ne parviennent pas à se diviser et deviennent polyploïdes, ce qui conduit finalement à l'apoptose. Dans une autre étude, il est également rapporté qu'un nombre élevé de chromosomes associé à la résistance à l'inhibition d'Aurora B et C suggère que les cellules dotées d'un mécanisme pour contourner le point de contrôle de la polyploïdie élevée sont résistantes à ce produit chimique. | |||||||||||
| In vivo | GSK1070916 (25, 50 ou 100 mg/kg) montre une inhibition dose-dépendante de la phosphorylation d'un substrat spécifique d'Aurora B chez la souris et, conformément à son activité cellulaire étendue, ce composé a des effets antitumoraux dans 10 modèles de xénogreffes tumorales humaines, y compris des modèles de cancer du sein, du côlon, du poumon et deux modèles de leucémie. |
Protocole (de référence)
| Test kinase :[1] |
|
|---|---|
| Test cellulaire :[2] |
|
| Étude animale :[2] |
|
Références
|
Validation du produit par le client
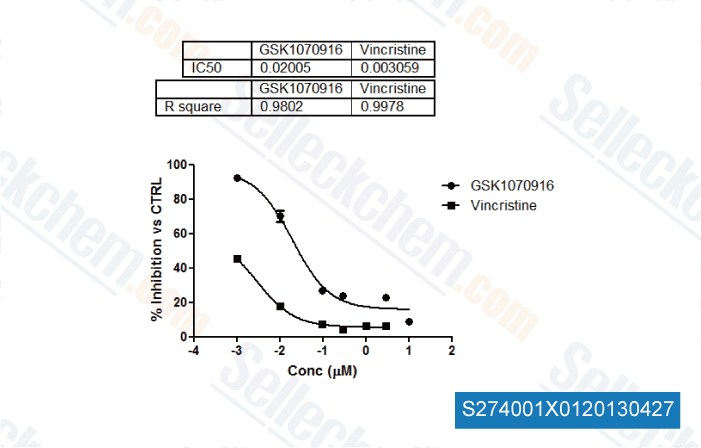
-
, , Antonino Maria Spart from University of Bologn
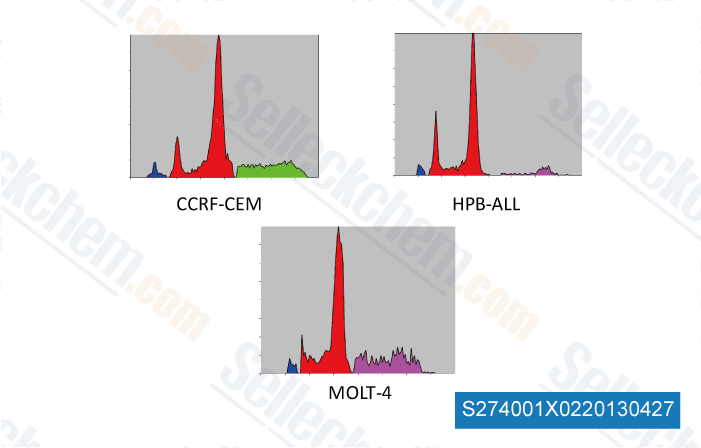
-
, , Antonino Maria Spart from University of Bologn
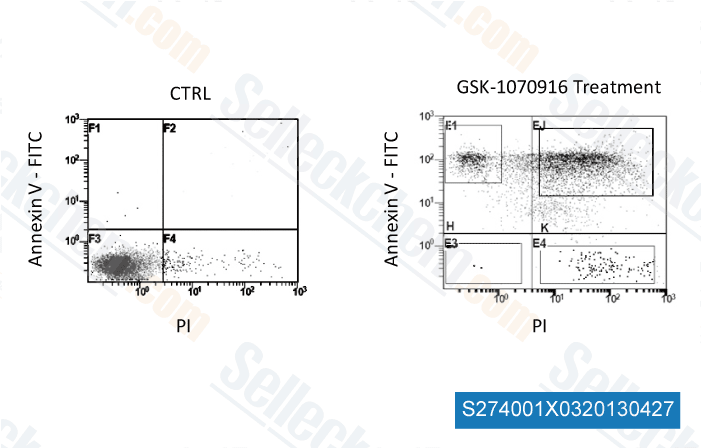
-
, , Antonino Maria Spart from University of Bologn
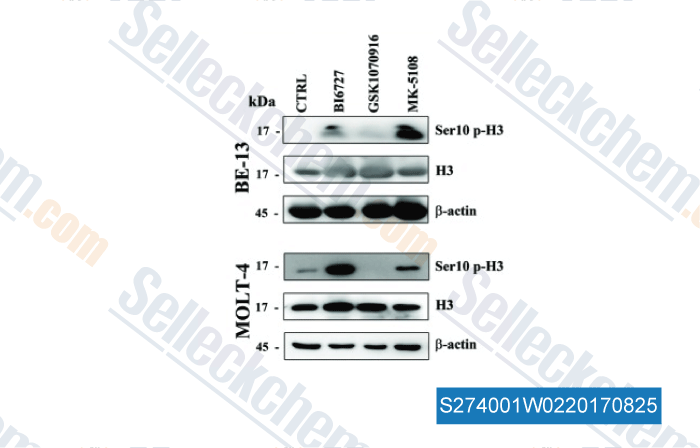
-
Données de [ , , Cell Cycle, 2014, 13(14):2237-47 ]
Sellecks GSK1070916 A été cité par 12 Publications
| Identification of chemical inhibitors targeting long noncoding RNA through gene signature-based high throughput screening [ Int J Biol Macromol, 2025, 292:139119] | PubMed: 39722392 |
| Integrated drug response prediction models pinpoint repurposed drugs with effectiveness against rhabdomyosarcoma [ PLoS One, 2024, 19(1):e0295629] | PubMed: 38277404 |
| DELs enable the development of BRET probes for target engagement studies in cells [ Cell Chem Biol, 2023, 30(8):987-998.e24] | PubMed: 37490918 |
| Targeting Aurora B kinase prevents and overcomes resistance to EGFR inhibitors in lung cancer by enhancing BIM- and PUMA-mediated apoptosis [ Cancer Cell, 2021, S1535-6108(21)00383-4] | PubMed: 34388376 |
| Loss of Aurora kinase signaling allows lung cancer cells to adopt endoreplication and form polyploid giant cancer cells that resist antimitotic drugs [ Cancer Res, 2020, canres.1693.2020] | PubMed: 33172929 |
| Tie2-FGFR1 Interaction Induces Adaptive PI3K Inhibitor Resistance by Upregulating Aurora A/PLK1/CDK1 Signaling in Glioblastoma. [ Cancer Res, 2019, 79(19):5088-5101] | PubMed: 31416846 |
| Network pharmacology modeling identifies synergistic Aurora B and ZAK interaction in triple-negative breast cancer [ NPJ Syst Biol Appl, 2019, 5:20] | PubMed: 31312514 |
| High-Throughput Screening Identifies Kinase Inhibitors That Increase Dual Adeno-Associated Viral Vector Transduction In Vitro and in Mouse Retina. [ Hum Gene Ther, 2018, 29(8):886-901] | PubMed: 29641320 |
| A small-molecule inhibitor targeting the AURKC-IκBα interaction decreases transformed growth of MDA-MB-231 breast cancer cells [ Oncotarget, 2017, 8(41):69691-69708] | PubMed: 29050234 |
| Leishmania donovani Aurora kinase: A promising therapeutic target against visceral leishmaniasis. [Chhajer R, et al. Biochim Biophys Acta, 2016, 1860(9):1973-88] | PubMed: 27288586 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
