Données techniques
| Formule | C29H31N7O |
||||||
| Poids moléculaire | 493.6 | Numéro CAS | 152459-95-5 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 25 mg/mL (50.64 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | Imatinib est un inhibiteur multi-cible de la tyrosine kinase avec une inhibition pour v-Abl, c-Kit et PDGFR, les valeurs IC50 sont respectivement de 0,6 μM, 0,1 μM et 0,1 μM dans des essais sans cellules ou basés sur des cellules. Imatinib (STI571) induit l'autophagie. | ||||||
|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||
| In vitro | Les essais in vitro pour l'inhibition d'un panel de protéines kinases à tyrosine et sérine/thréonine montrent qu'Imatinib inhibe potentiellement la tyrosine kinase v-Abl et PDGFR avec une IC50 de 0,6 et 0,1 μM, respectivement. Ce composé inhibe l'activation dépendante du SLF de l'activité de la kinase c-Kit de type sauvage avec une IC50 pour ces effets d'environ 0,1 μM, ce qui est similaire à la concentration requise pour l'inhibition de PDGFR. Il présente une activité inhibitrice de croissance sur la lignée cellulaire de carcinoïde bronchique humaine NCI-H727 et la lignée cellulaire de carcinoïde pancréatique humaine BON-1 avec une IC50 de 32,4 et 32,8 μM, respectivement. Une étude récente montre que ce produit chimique a le potentiel d'exercer ses effets antileucémiques dans la leucémie myéloïde chronique en régulant à la baisse les canaux K(+) hERG1, qui sont fortement exprimés dans les cellules leucémiques et semblent d'une importance exceptionnelle pour favoriser la leucémogenèse. |
||||||
| In vivo | Imatinib produit un effet antitumoral différent sur trois tumeurs xénogreffées dérivées d'échantillons chirurgicaux de cancers pulmonaires à petites cellules humains frais, avec 80 %, 40 % et 78 % d'inhibition de la croissance des tumeurs SCLC6, SCLC61 et SCLC108, respectivement, et aucune inhibition significative de la croissance de SCLC74. Chez des souris ApoE(-/-) nourries avec un régime riche en graisses, ce composé réduit significativement la zone de coloration lipidique induite par le régime riche en graisses de 30 %, 27 % et 35 % par rapport aux contrôles non traités par un régime riche en graisses lorsqu'il est administré par gavage à 10, 20 et 40 mg/kg, respectivement, et supprime l'accumulation de lipides dans l'artère carotide. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
Références
|
Validation du produit par le client
![<p> </p><p>Inhibition of thymidine (a and b) and cytarabine (c and d) uptake with imatinib. K562 cells (a and c) and MEG-01 cells (b and d) were incubated at 37 ◦C for 15 min with imatinib transport buffer, and then incubated with 0.5 Ci of [3H] thymidine or [3H] cytarabine for an additional 5 min in presence of imatinib. Cells were then washed 3 times, lysed and radioactivity associated to cell pellets was quantified. DMSO, dimethylsulfoxide; DPD, dipyridamole.</p>](https://file.selleckchem.com/downloads/review/700px/Imatinib-S247501Z0120130501.gif)
-
Données de [ Leukemia Res , 2012 , 36, 1311-1314 ]
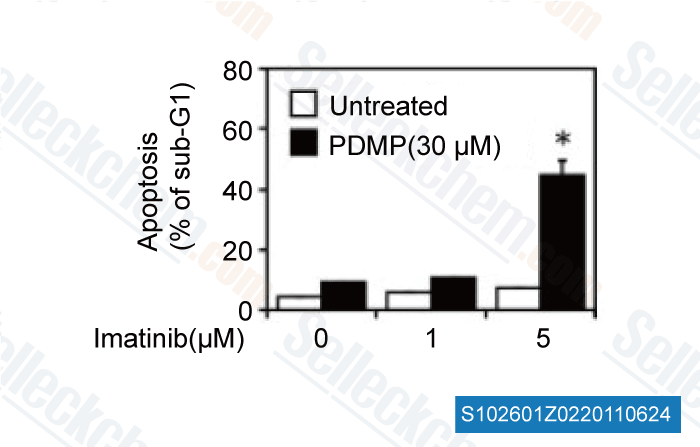
-
Données de [ FASEB J , 2011 , 25, 3661-3673 ]
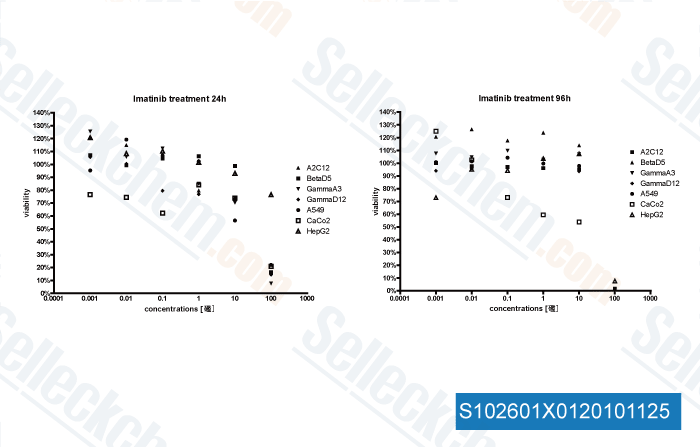
-
, , Dr. Thomas Kruwel of Fraunhofer
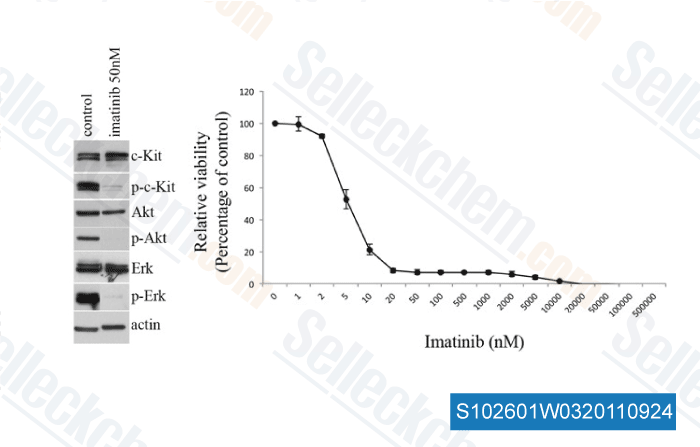
-
, , Dr. Helen Rizos from the university of Sydney
Sellecks Imatinib (STI571) A été cité par 326 Publications
| Proteogenomic characterization of non-functional pancreatic neuroendocrine tumors unravels clinically relevant subgroups [ Cancer Cell, 2025, 43(4):776-796.e14] | PubMed: 40185092 |
| CD19-targeted HSP90 inhibitor nanoparticle combined with TKIs reduces tumor burden and enhances T-cell immunity in murine B-cell malignancies [ Theranostics, 2025, 15(8):3589-3609] | PubMed: 40093890 |
| The landcape of Helicobacter pylori-mediated DNA breaks links bacterial genotoxicity to its oncogenic potential [ Genome Med, 2025, 17(1):14] | PubMed: 39994739 |
| Haploinsufficiency of miR-143 and miR-145 reveal targetable dependencies in resistant del(5q) myelodysplastic neoplasm [ Leukemia, 2025, 39(4):917-928] | PubMed: 40000845 |
| Systematic analysis of ZDHHC9 as a potential prognostic and immunotherapy biomarker in breast cancer [ Front Immunol, 2025, 16:1609621] | PubMed: 40740766 |
| Methylstat sensitizes ovarian cancer cells to PARP-inhibition by targeting the histone demethylases JMJD1B/C [ Cancer Gene Ther, 2025, 10.1038/s41417-025-00874-z] | PubMed: 39915607 |
| Activation of TMEM16E scramblase induces ligand independent growth factor receptor signaling and macropinocytosis for membrane repair [ Commun Biol, 2025, 8(1):35] | PubMed: 39794444 |
| Characterization of the Temporal Dynamics of the Endothelial-Mesenchymal-like Transition Induced by Soluble Factors from Dengue Virus Infection in Microvascular Endothelial Cells [ Int J Mol Sci, 2025, 26(5)2139] | PubMed: 40076764 |
| Senataxin and DNA-PKcs redundantly promote non-homologous end joining repair of DNA double strand breaks during V(D)J recombination [ Sci Adv, 2025, 11(25):eads5272] | PubMed: 40540553 |
| Utility of the Base Editing System for Introducing Drug-Resistant Gene Mutations Into Human Leukemia Cellular Models [ Cureus, 2025, 17(4):e81889] | PubMed: 40342439 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
