Données techniques
| Formule | C23H25ClN6O3 |
||||||||||
| Poids moléculaire | 468.94 | Numéro CAS | 761437-28-9 | ||||||||
| Solubilité (25°C)* | In vitro | DMSO | 47 mg/mL (100.22 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||
Préparation des solutions mères
Activité biologique
| Description | TAE226 (NVP-TAE226) est un puissant inhibiteur de FAK avec une IC50 de 5,5 nM et modérément puissant contre Pyk2, ~10 à 100 fois moins puissant contre InsR, IGF-1R, ALK et c-Met. Ce composé induit l'apoptose. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | Le NVP-TAE226 (< 1 μM) inhibe l'autophosphorylation de FAK (Tyr397) induite par la matrice extracellulaire dans les cellules U87 privées de sérum. Ce composé (< 1 μM) inhibe également la phosphorylation de l'IGF-1R induite par l'IGF-I et l'activité de ses gènes cibles en aval tels que MAPK et Akt dans les cellules U87 et U251. Ce produit chimique (<10 μM) retarde la croissance des cellules tumorales et atténue la progression du cycle cellulaire en G(2)-M associée à une diminution de l'expression des protéines cycline B1 et cdc2 phosphorylée (Tyr15) dans les cellules U87 et U251. Ce composé (1 μM) inhibe l'invasion des cellules tumorales d'au moins 50 % par rapport au contrôle dans un essai d'invasion Matrigel in vitro dans des lignées cellulaires de gliome. Ce produit chimique (1 μM) le traitement des lignées cellulaires de gliome contenant p53 de type sauvage présente principalement un arrêt en G(2)-M, tandis que les lignées cellulaires de gliome portant p53 muté subissent l'apoptose, comme en témoignent la détection de l'activation de la caspase-3/7 et du clivage de la poly(ADP-ribose) polymérase et par un essai d'apoptose à l'Annexine V. Ce composé (5 μM) inhibe la phosphorylation de FAK dans la lignée cellulaire de neuroblastome humain SK-N-AS. Ce produit chimique (<10 μM) le traitement de la lignée cellulaire de neuroblastome humain SK-N-AS entraîne une diminution de la viabilité cellulaire, un arrêt du cycle cellulaire et une augmentation de l'apoptose. Ce composé (0,1 μM-10 μM) inhibe la formation de tubes par les cellules HMEC1. | |||||||||||
| In vivo | Le NVP-TAE226 (75 mg/kg) augmente significativement le taux de survie des souris porteuses de xénogreffes de gliome intracrânien. Ce composé (100 mg/kg, oral) exerce une diminution significative de la densité des microvaisseaux dans un modèle de cancer du côlon humain chez des souris SCID. Ce produit chimique (100 mg/kg, oral) inhibe efficacement la croissance tumorale pancréatique humaine MIA PaCa-2 sans perte de poids corporel dans un modèle in vivo. Il inhibe la croissance tumorale mammaire murine 4T1 et la métastase vers le poumon de manière dose-dépendante dans un modèle in vivo, associée à l'inhibition de l'autophosphorylation de FAK en Y397 et de la phosphorylation d'Akt en Sérine473. |
Protocole (de référence)
| Test cellulaire :[1] |
|
|---|---|
| Étude animale :[1] |
|
Références
|
Validation du produit par le client
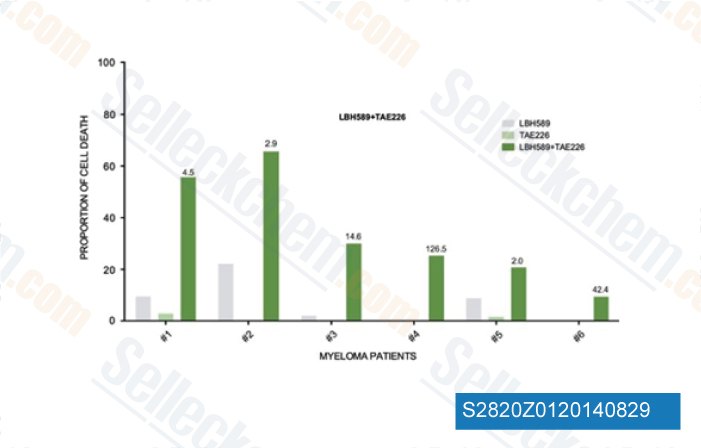
-
Données de [ Cell Death Dis , 2014 , 5, e1134 ]
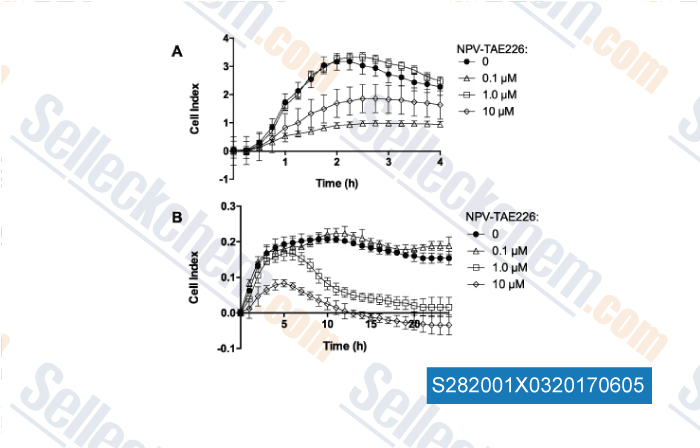
-
Données de [ , , J Inorg Biochem, 2016, 160:225-35 ]
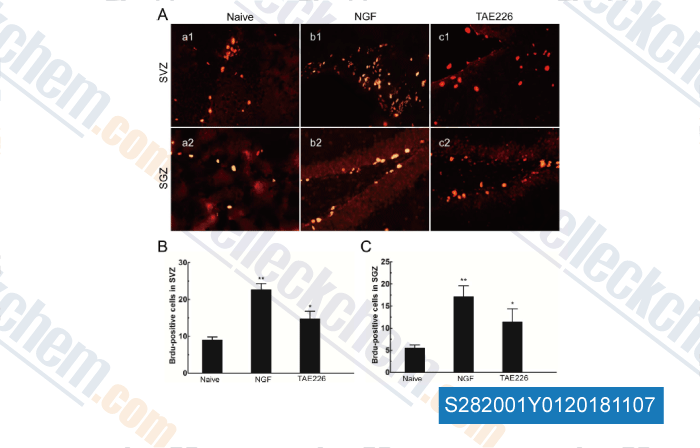
-
Données de [ , , Neurosci Lett, 2018, 672:96-102 ]
Sellecks TAE226 (NVP-TAE226) A été cité par 26 Publications
| Aurora kinase A promotes epithelial‑mesenchymal transition by regulating P130 and P107 molecules in thyroid cancer cells [ Exp Ther Med, 2025, 29(5):93] | PubMed: 40162054 |
| Overexpression of BACH1 mediated by IGF2 facilitates hepatocellular carcinoma growth and metastasis via IGF1R and PTK2 [ Theranostics, 2022, 12(3):1097-1116] | PubMed: 35154476 |
| Mechanical coupling of supracellular stress amplification and tissue fluidization during exit from quiescence [ Proc Natl Acad Sci U S A, 2022, 119(32):e2201328119] | PubMed: 35914175 |
| Integrin αvβ3 Induces HSP90 Inhibitor Resistance via FAK Activation in KRAS-Mutant Non-Small Cell Lung Cancer [ Cancer Res Treat, 2022, 54(3):767-781] | PubMed: 34607394 |
| Three subtypes of lung cancer fibroblasts define distinct therapeutic paradigms [ Cancer Cell, 2021, S1535-6108(21)00492-X] | PubMed: 34624218 |
| TLR4 signalling via Piezo1 engages and enhances the macrophage mediated host response during bacterial infection [ Nat Commun, 2021, 12(1):3519] | PubMed: 34112781 |
| Focal adhesion kinase inhibition synergizes with nab-paclitaxel to target pancreatic ductal adenocarcinoma [ J Exp Clin Cancer Res, 2021, 91-2021)] | PubMed: None |
| Focal adhesion kinase inhibition synergizes with nab-paclitaxel to target pancreatic ductal adenocarcinoma [ J Exp Clin Cancer Res, 2021, 40(1):91] | PubMed: 33750427 |
| A first-in-class anticancer dual HDAC2/FAK inhibitors bearing hydroxamates/benzamides capped by pyridinyl-1,2,4-triazoles [ Eur J Med Chem, 2021, 222:113569] | PubMed: 34111829 |
| Campylobacter jejuni Triggers Signaling through Host Cell Focal Adhesions To Inhibit Cell Motility [ mBio, 2021, 12(4):e0149421] | PubMed: 34425711 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
