Données techniques
| Formule | C16H18N2OS.HBr |
||||||
| Poids moléculaire | 367.3 | Numéro CAS | 63208-82-2 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 73 mg/mL (198.74 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | Pifithrin-α est un inhibiteur de p53, inhibant la transactivation dépendante de p53 des gènes répondant à p53. Pifithrin-α est également un puissant agoniste du récepteur des hydrocarbures aromatiques (AhR). | |
|---|---|---|
| Cibles |
|
|
| In vitro | La Pifithrin-α inhibe la transactivation dépendante de p53 des gènes répondant à p53 dans les cellules ConA. La Pifithrin-α (10 μM) inhibe la mort apoptotique des cellules C8 induite par Dox, Taxol, cytosine arabinoside. La Pifithrin-α inhibe l'arrêt de croissance dépendant de p53 des fibroblastes diploïdes humains en réponse aux dommages de l'ADN, mais n'a aucun effet sur les fibroblastes déficients en p53. La Pifithrin-α peut moduler l'importation ou l'exportation nucléaire (ou les deux) de p53 ou peut diminuer la stabilité du p53 nucléaire. La Pifithrin-α (100-200 nM) supprime complètement l'augmentation induite par la camptothécine du niveau de liaison de p53 à l'ADN ainsi que du gène Bax répondant à p53 dans les cellules hippocampiques. La Pifithrin-α diminue également le niveau basal de l'activité de liaison de p53 à l'ADN. La Pifithrin-α (200 nM) protège les neurones hippocampiques cultivés contre la mort induite par les agents endommageant l'ADN. La Pifithrin-α (200 μM) stabilise la fonction mitochondriale, supprime l'activation des caspases et protège les neurones hippocampiques cultivés contre la mort induite par le glutamate et le peptide β-amyloïde. La Pifithrin α, en plus de p53, peut supprimer la signalisation du choc thermique et des récepteurs des glucocorticoïdes, mais n'a aucun effet sur la signalisation du facteur nucléaire-kappaB. La Pifithrin α (10 μM) réduit l'activation du facteur de transcription du choc thermique (HSF1) et augmente la sensibilité cellulaire à la chaleur. La Pifithrin α (10 μM) réduit l'activation du récepteur des glucocorticoïdes et sauve les thymocytes de souris de la mort apoptotique après traitement dans les cellules HeLa. Le PFTalpha bloque l'induction médiatisée par p53 de p21/Waf-1 dans les cellules rénales embryonnaires humaines. |
|
| In vivo | Le traitement par Pifithrin-α (2,2 mg/kg i.p.) sauve complètement les souris (C57BL et Balb/c) des deux souches de doses létales de 60 % d'irradiation gamma (8 Gy pour C57BL et 6 Gy pour Balb/c). Les souris injectées avec Pifithrin-α ont perdu moins de poids que les souris irradiées non prétraitées avec la Pifithrin-α. La Pifithrin-α (2,2 mg/kg) abroge la régulation dépendante de p53 de la réplication de l'ADN après irradiation gamma de tout le corps chez les souris. La Pifithrin-α (2 mg/kg i.p.) 30 min avant le traitement d'occlusion de l'artère cérébrale moyenne chez les souris réduit les lésions cérébrales ischémiques et protège les neurones hippocampiques contre les lésions excitotoxiques. La Pifithrin α (3,6 μg/kg i.p.) inhibe la dégénérescence du thymus induite par le Dex chez les souris. La Pifithrin α (2 mg/kg) entraîne un degré significativement plus faible d'incapacité motrice chez les rats recevant une occlusion transitoire de l'artère cérébrale moyenne par rapport aux contrôles. Les animaux traités à la Pifithrin α présentent moins d'incapacité motrice et des infarctus plus petits lorsque le médicament est administré jusqu'à une heure après le début de l'accident vasculaire cérébral. La Pifithrin α entraîne des scores d'incapacité motrice significativement plus faibles chez les rats que chez les animaux traités par véhicule 7 jours après l'opération. La Pifithrin α entraîne une réduction significative de l'apoptose chez les rats, comme indiqué par la coloration Tunel et de la caspase 3. |
Protocole (de référence)
| Test cellulaire : |
|
|---|---|
| Étude animale : |
|
Références
|
Validation du produit par le client
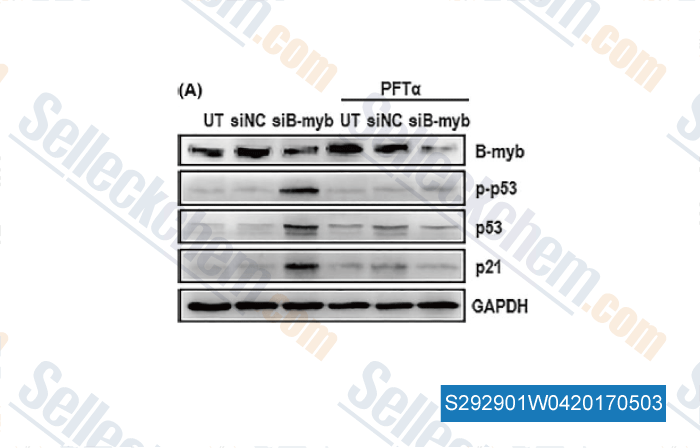
-
, , Cell Prolif, 2017, doi: 10.1111/cpr.12319
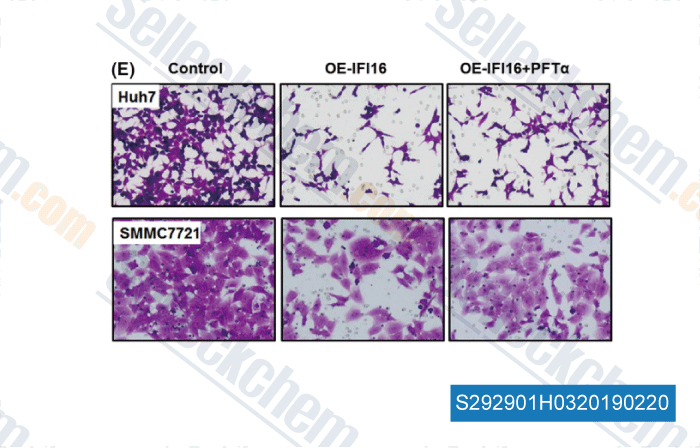
-
Données de [ , , Cell Prolif, 2017, 50(6) ]
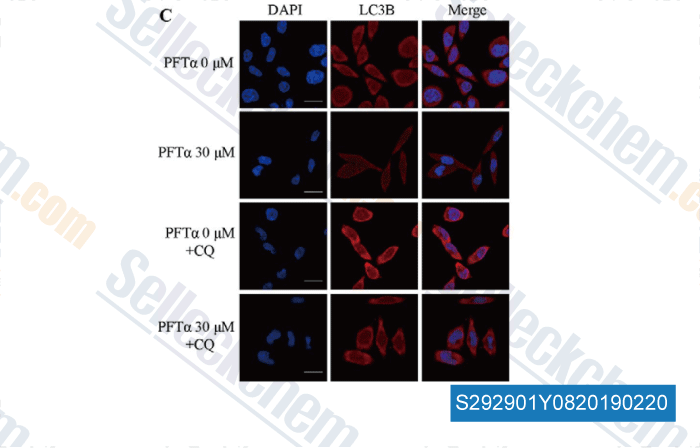
-
Données de [ , , J Biol Chem, 2016, 291(9):4462-72 ]
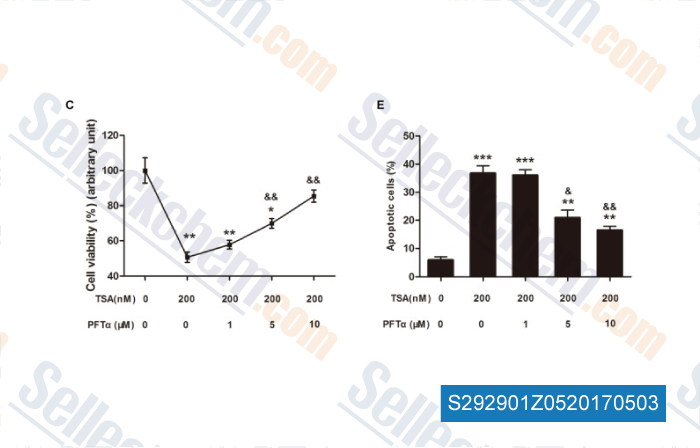
-
Données de [ , , Int J Biol Sci, 2016, 12(11):1298-1308 ]
Sellecks Pifithrin-α (PFTα) Hhydrobromide A été cité par 133 Publications
| Minichromosome maintenance 4 plays a key role in protecting against acute kidney injury by regulating tubular epithelial cells survival and regeneration [ J Adv Res, 2025, S2090-1232(25)00192-4] | PubMed: 40107353 |
| Inhibition of SIRT3 by a specific inhibitor induces cellular senescence and growth arrest of ovarian granulosa cell tumor via p53 and NF-κB axis [ Front Pharmacol, 2025, 16:1608156] | PubMed: 40777993 |
| Downregulation of Alox5 Inhibits Ferroptosis to Improve Doxorubicin-Induced Cardiotoxicity via the P53/SLC7A11 Pathway [ J Cell Mol Med, 2025, 29(11):e70641] | PubMed: 40485049 |
| Substrate Stiffness Modulates Fibroblast Extracellular Vesicle Secretion via Mechanotransduction Pathways [ bioRxiv, 2025, 2025.07.29.667440] | PubMed: 40766685 |
| Integrated molecular and functional characterization of the intrinsic apoptotic machinery identifies therapeutic vulnerabilities in glioma [ Nat Commun, 2024, 15(1):10089] | PubMed: 39572533 |
| DNMT1 regulates human erythropoiesis by modulating cell cycle and endoplasmic reticulum stress in a stage-specific manner [ Cell Death Differ, 2024, 31(8):999-1012] | PubMed: 38719927 |
| Chk2 Modulates Bmi1-Deficiency-Induced Renal Aging and Fibrosis via Oxidative Stress, DNA Damage, and p53/TGFβ1-Induced Epithelial-Mesenchymal Transition [ Int J Biol Sci, 2024, 20(6):2008-2026] | PubMed: 38617548 |
| BOP1 contributes to the activation of autophagy in polycystic ovary syndrome via nucleolar stress response [ Cell Mol Life Sci, 2024, 81(1):101] | PubMed: 38409361 |
| Suppression of neuronal CDK9/p53/VDAC signaling provides bioenergetic support and improves post-stroke neuropsychiatric outcomes [ Cell Mol Life Sci, 2024, 81(1):384] | PubMed: 39235466 |
| Guided monocyte fate to FRβ/CD163+ S1 macrophage antagonises atopic dermatitis via fibroblastic matrices in mouse hypodermis [ Cell Mol Life Sci, 2024, 82(1):14] | PubMed: 39720957 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
