Données techniques
| Formule | C51H79NO13 |
||||||||||||||
| Poids moléculaire | 914.18 | Numéro CAS | 53123-88-9 | ||||||||||||
| Solubilité (25°C)* | In vitro | DMSO | 100 mg/mL (109.38 mM) | ||||||||||||
| Ethanol | 100 mg/mL (109.38 mM) | ||||||||||||||
| Water | Insoluble | ||||||||||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||||||
Préparation des solutions mères
Activité biologique
| Description | La Rapamycin est un inhibiteur spécifique de mTOR avec une IC50 d'environ 0,1 nM dans les cellules HEK293. Ce composé se lie à la FKBP12 et agit spécifiquement comme un inhibiteur allostérique de mTORC1. C'est un activateur d'Autophagy et un immunosuppresseur. | ||
|---|---|---|---|
| Cibles |
|
||
| In vitro | La Rapamycin inhibe l'activité endogène de mTOR dans les cellules HEK293 avec une IC50 d'environ 0,1 nM, plus puissamment que l'iRap et l'AP21967 avec des IC50 d'environ 5 nM et 10 nM, respectivement. Chez Saccharomyces cerevisiae, le traitement par ce composé induit un arrêt sévère du cycle cellulaire G1/S et une inhibition de l'initiation de la traduction à des niveaux inférieurs à 20% du contrôle. Il inhibe significativement la viabilité cellulaire de T98G et U87-MG de manière dose-dépendante avec des IC50 de 2 nM et 1 μM, respectivement, tout en affichant peu d'activité contre les cellules U373-MG avec une IC50 de >25 μM malgré l'étendue similaire de l'inhibition de la signalisation mTOR. Ce produit chimique (100 nM) induit un arrêt en G1 et l'Autophagy mais pas l'apoptose dans les cellules U87-MG et T98G sensibles à la Rapamycin en inhibant la fonction de mTOR. |
||
| In vivo | Le traitement par la Rapamycin in vivo bloque spécifiquement les cibles connues pour être en aval de mTOR, telles que la phosphorylation et l'activation de la p70S6K et la libération de l'inhibition de l'eIF4E par PHAS-1/4E-BP1, entraînant un blocage complet des augmentations hypertrophiques du poids du muscle plantaire et de la taille des fibres. Un traitement à court terme avec ce composé, même à la dose la plus faible de 0,16 mg/kg, produit une inhibition profonde de l'activité de la p70S6K, ce qui est corrélé à une augmentation de la mort des cellules tumorales et de la nécrose des tumeurs rénales d'Eker. Ce produit chimique inhibe la croissance tumorale métastatique et l'angiogenèse dans les modèles de xénogreffe CT-26 en réduisant la production de VEGF et le blocage de la signalisation des cellules endothéliales induite par le VEGF. Le traitement avec ce composé à 4 mg/kg/jour réduit significativement la croissance tumorale des xénogreffes C6 et la perméabilité vasculaire tumorale. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
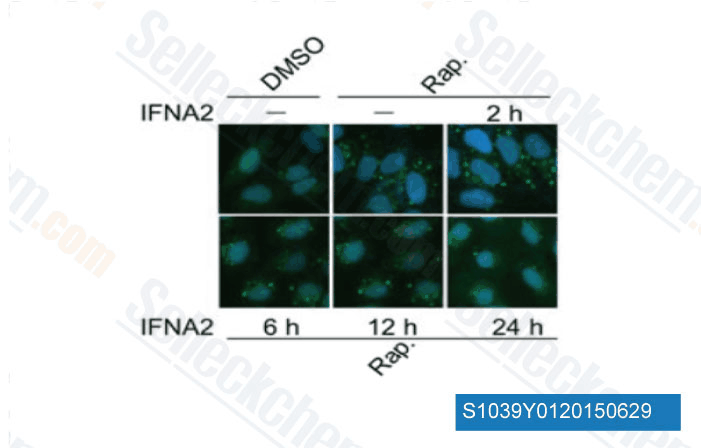
-
Données de [ Autophagy , 2015 , 11(4), 617-28 ]
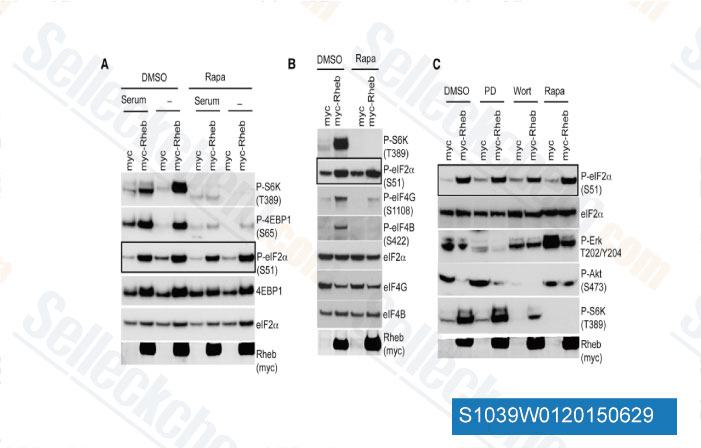
-
Données de [ Cell Rep , 2015 , 10.1016/j.celrep.2015.01.014 ]

-
Données de [ Biochem Pharmacol , 2015 , 95(3), 156-69 ]
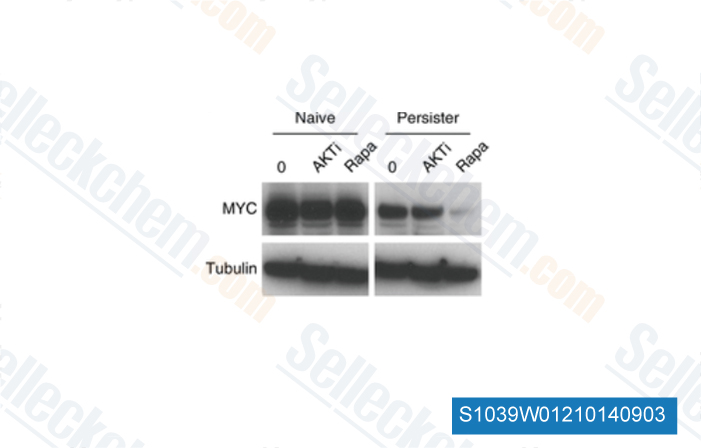
-
Données de [ Nat Genet , 2014 , 46(4), 364-70 ]
Sellecks Rapamycin (Sirolimus) A été cité par 1914 Publications
| Taurine from tumour niche drives glycolysis to promote leukaemogenesis [ Nature, 2025, 10.1038/s41586-025-09018-7] | PubMed: 40369079 |
| High fructose consumption aggravates inflammation by promoting effector T cell generation via inducing metabolic reprogramming [ Signal Transduct Target Ther, 2025, 10(1):271] | PubMed: 40854873 |
| RIPK1 senses S-adenosylmethionine scarcity to drive cell death and inflammation [ Cell Metab, 2025, S1550-4131(25)00294-3] | PubMed: 40570842 |
| Interferon-responsive intestinal BEST4/CA7+ cells are targets of bacterial diarrheal toxins [ Cell Stem Cell, 2025, S1934-5909(25)00042-6] | PubMed: 40010349 |
| USP5 stabilizes YTHDF1 to control cancer immune surveillance through mTORC1-mediated phosphorylation [ Nat Commun, 2025, 16(1):1313] | PubMed: 39900921 |
| Macrophage-derived amphiregulin induces myofibroblast transition in adipogenic lineage precursors near Staphylococcus aureus abscess in bone marrow [ Nat Commun, 2025, 16(1):8409] | PubMed: 40998791 |
| WNK1 signalling regulates amino acid transport and mTORC1 activity to sustain acute myeloid leukaemia growth [ Nat Commun, 2025, 16(1):4920] | PubMed: 40425534 |
| Lysosomal NKG7 restrains mTORC1 activity to promote CD8+ T cell durability and tumor control [ Nat Commun, 2025, 16(1):1628] | PubMed: 39952956 |
| DRAM1 promotes the stability of lysosomal VAMP8 to enhance autolysosome formation and facilitates the extravasation [ Nat Commun, 2025, 16(1):5826] | PubMed: 40595569 |
| Lipoic acid functions in Paneth cells to prevent human intestinal stem cell aging [ Nat Commun, 2025, 16(1):6016] | PubMed: 40593722 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
