Données techniques
| Formule | C21H16ClF3N4O3 |
||||||
| Poids moléculaire | 464.82 | Numéro CAS | 284461-73-0 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 92 mg/mL (197.92 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | Sorafenib est un inhibiteur multikinase de Raf-1 et B-Raf avec une IC50 de 6 nM et 22 nM dans des tests sans cellules, respectivement. Sorafenib inhibe VEGFR-2, VEGFR-3, PDGFR-β, Flt-3 et c-KIT avec une IC50 de 90 nM, 20 nM, 57 nM, 59 nM et 68 nM, respectivement. Sorafenib induit l'autophagy et l'apoptosis et active la ferroptosis avec une activité anti-tumorale. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | Sorafenib inhibe l'activité B-Raf de type sauvage et mutante V599E avec une IC50 de 22 nM et 38 nM, respectivement. Ce composé inhibe également puissamment mVEGFR2 (Flk-1), mVEGFR3, mPDGFRβ, Flt3 et c-Kit avec une IC50 de 15 nM, 20 nM, 57 nM, 58 nM et 68 nM, respectivement. Il inhibe faiblement FGFR-1 avec une IC50 de 580 nM. Cette substance chimique n'est pas active contre ERK-1, MEK-1, EGFR, HER-2, IGFR-1, c-Met, PKB, PKA, cdk1/cyclinB, PKCα, PKCγ et pim-1. Il inhibe nettement la phosphorylation de VEGFR2 dans les cellules NIH 3T3 avec une IC50 de 30 nM et la phosphorylation de Flt-3 dans les cellules HEK-293 avec une IC50 de 20 nM. Cet agent bloque puissamment la phosphorylation de MEK 1/2 et ERK 1/2 dans la plupart des lignées cellulaires mais pas dans les cellules A549 ou H460, tout en n'ayant aucun effet sur l'inhibition de la voie PKB. Il inhibe la prolifération des cellules HAoSMC et MDA-MB-231 avec une IC50 de 0,28 μM et 2,6 μM, respectivement. En plus de l'inhibition de la voie de signalisation RAF/MEK/ERK, ce composé inhibe significativement la phosphorylation de eIF4E et régule à la baisse les niveaux de Mcl-1 dans les cellules de carcinome hépatocellulaire (HCC) d'une manière indépendante de MEK/ERK. Il inhibe la prolifération des cellules PLC/PRF/5 et HepG2 avec une IC50 de 6,3 μM et 4,5 μM, respectivement, et conduit à une induction significative de l'apoptosis. | |||||||||||
| In vivo | L'administration orale de Sorafenib (~60 mg/kg) démontre une activité antitumorale à large spectre, dose-dépendante, contre une variété de modèles de xénogreffes de tumeurs humaines, y compris MDA-MB-231, Colo-205, HT-29, DLD-1, NCI-H460 et A549, sans preuve de toxicité. En association avec l'efficacité antitumorale, ce traitement composé inhibe puissamment la phosphorylation de MEK 1/2 et les niveaux de pERK 1/2 dans les xénogreffes HT-29 et MDA-MB-231 mais pas dans les xénogreffes Colo-205, et supprime significativement la surface microvasculaire (MVA) et la densité microvasculaire (MVD) dans les xénogreffes tumorales MDA MB-231, HT-29 et Colo-205. Cet agent produit une inhibition de croissance dose-dépendante des xénogreffes tumorales PLC/PRF/5 chez des souris SCID avec des TGI de 49% et 78% à 10 mg/kg et 30 mg/kg, respectivement, ce qui est cohérent avec l'inhibition de la phosphorylation de ERK et eIF4E, la réduction de la surface microvasculaire et l'induction de l'apoptosis des cellules tumorales. Il sensibilise les cellules bax-/- au TRAIL de manière dose-dépendante, par un mécanisme impliquant la régulation à la baisse de l'expression de Mcl-1 et cIAP2 médiée par NF-κB. La combinaison de ce composé (30-60 mg/kg) avec le TRAIL (5 mg/kg) montre une efficacité dramatique dans les xénogreffes tumorales HCT116 bax-/- et HT29 résistantes au TRAIL. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
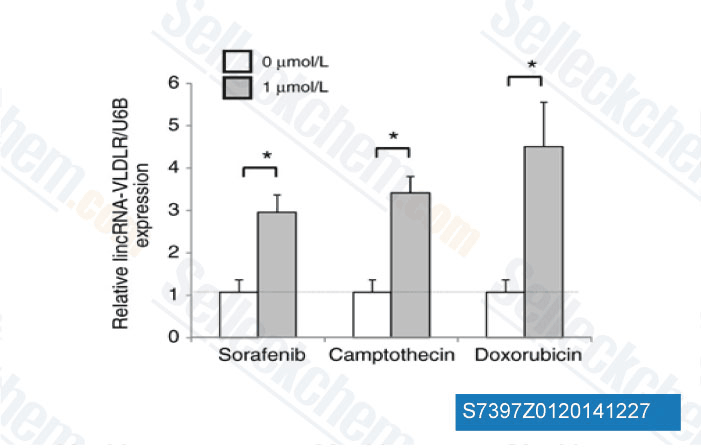
-
Données de [ Mol Cancer Res , 2014 , 12(10), 1377-87 ]
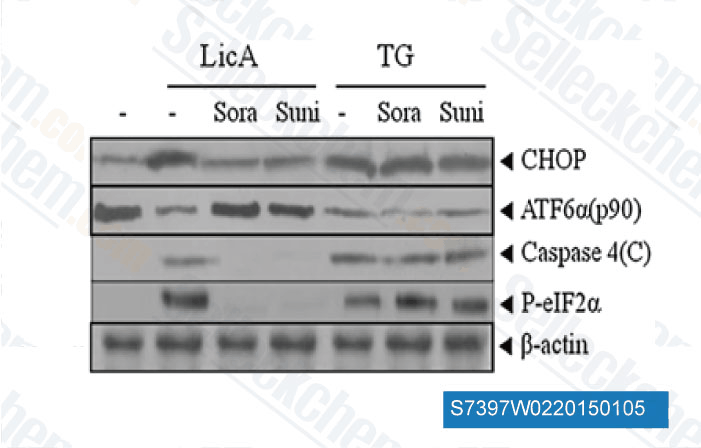
-
Données de [ Apoptosis , 2014 , 19(4), 682-97 ]
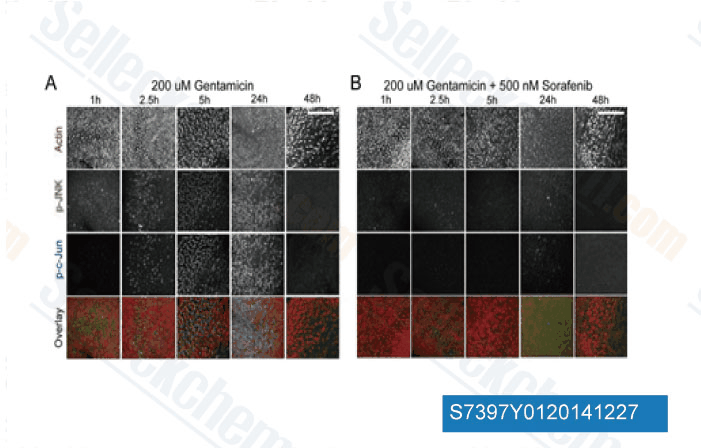
-
Données de [ J Neurosci , 2013 , 33(7), 3079-93 ]
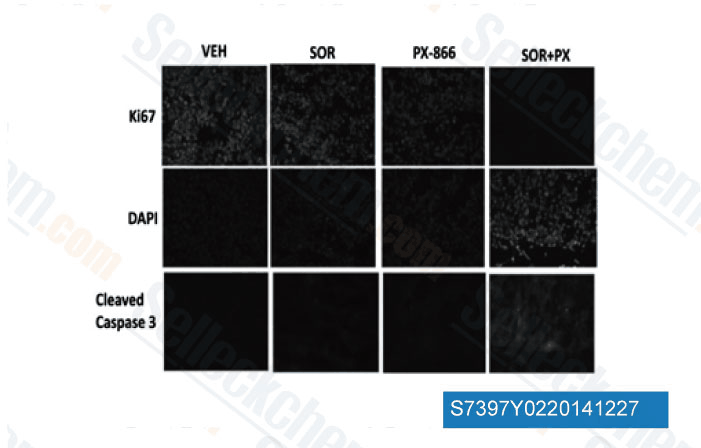
-
Données de [ Mol Pharmacol , 2013 , 84(4), 562-71 ]
Sellecks Sorafenib (BAY 43-9006) A été cité par 599 Publications
| Sorafenib enhanced the function of myeloid-derived suppressor cells in hepatocellular carcinoma by facilitating PPARα-mediated fatty acid oxidation [ Mol Cancer, 2025, 24(1):34] | PubMed: 39876004 |
| S100P is a ferroptosis suppressor to facilitate hepatocellular carcinoma development by rewiring lipid metabolism [ Nat Commun, 2025, 16(1):509] | PubMed: 39779666 |
| PIP5K1A Suppresses Ferroptosis and Induces Sorafenib Resistance by Stabilizing NRF2 in Hepatocellular Carcinoma [ Adv Sci (Weinh), 2025, 12(30):e04372] | PubMed: 40405713 |
| Injectable SF-platform orchestrates GPX4-targeted ferroptosis-autophagy-immunogenic circuit for overcoming oxidative resistance in triple-negative breast cancer [ Theranostics, 2025, 15(17):8757-8778] | PubMed: 40963899 |
| FLT3 inhibitors induce p53 instability, driven by STAT5/MDM2/p53 competitive interactions in acute myeloid leukemia [ Cancer Lett, 2025, 611:217446] | PubMed: 39756787 |
| In vivo optoacoustic imaging of endothelin receptor expression and treatment response in the hypoxic tumor microenvironment [ Eur J Nucl Med Mol Imaging, 2025, 10.1007/s00259-025-07494-7] | PubMed: 40802092 |
| Matrix stiffness regulates glucose-6-phosphate dehydrogenase expression to mediate sorafenib resistance in hepatocellular carcinoma through the ITGB1-PI3K/AKT pathway [ Cell Death Dis, 2025, 16(1):538] | PubMed: 40685383 |
| Inhibition of Wnt/β-catenin increases anti-tumor activity by synergizing with sorafenib in hepatocellular carcinoma [ Cell Death Dis, 2025, 16(1):466] | PubMed: 40593458 |
| Targeting PTGDS Promotes ferroptosis in peripheral T cell lymphoma through regulating HMOX1-mediated iron metabolism [ Br J Cancer, 2025, 132(4):384-400] | PubMed: 39706989 |
| Targeting the MYC oncogene with a selective bi-steric mTORC1 inhibitor elicits tumor regression in MYC-driven cancers [ Cell Chem Biol, 2025, 32(8):994-1012.e11] | PubMed: 40803322 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
