Données techniques
| Formule | C14H8N2O |
||||||
| Poids moléculaire | 220.23 | Numéro CAS | 129-56-6 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 44 mg/mL (199.79 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | SP600125 (Nsc75890) est un inhibiteur à large spectre de JNK pour JNK1, JNK2 et JNK3 avec une IC50 de 40 nM, 40 nM et 90 nM dans des essais acellulaires, respectivement ; une sélectivité 10 fois supérieure contre MKK4, 25 fois supérieure contre MKK3, MKK6, PKB et PKCα, et une sélectivité 100 fois supérieure contre ERK2, p38, Chk1, EGFR etc. Ce composé est également un inhibiteur à large spectre de sérine/thréonine kinases incluant Aurora kinase A, FLT3 et TRKA avec une IC50 de 60 nM, 90 nM et 70 nM. Il inhibe l'autophagie et active l'apoptose. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | SP600125 est initialement caractérisé comme un inhibiteur sélectif ATP-compétitif de la c-Jun N-terminal kinase JNK. Dans les cellules T Jurkat, ce composé inhibe la phosphorylation de c-Jun avec une IC50 de 5 μM à 10 μM. Dans les cellules CD4+, telles que les cellules Th0 isolées du cordon ombilical humain ou du sang périphérique, il bloque l'activation et la différenciation cellulaire et inhibe l'expression des gènes inflammatoires COX-2, IL-2, IL-10, IFN-γ et TNF-α, avec une IC50 de 5 μM à 12 μM. Cependant, des études ultérieures révèlent que ce produit chimique supprime également le récepteur des hydrocarbures aromatiques (AhR) , Mps1 , et un panel d'autres sérine/thréonine kinases, y compris Aurora kinase A, FLT3, MELK et TRKA . Dans des cellules bêta de souris MIN6, ce composé (20 μM) induit la phosphorylation de p38 MAPK et l'activation de son promoteur dépendant de CREB. Dans les cellules HCT116, il (20 μM) bloque la transition de la phase G2 à la mitose et induit l'endoréplication. Cette capacité de cet inhibiteur est indépendante de l'inhibition de JNK, mais due à son inhibition de l'activation de CDK1-cyclin B en amont d'Aurora A et de la Polo-like kinase 1. |
|||||||||||
| In vivo | Chez la souris, le SP600600125 (15 mg/kg ou 30 mg/kg) inhibe significativement l'expression du TNF-α induite par le lipopolysaccharide (LPS) et l'apoptose des thymocytes CD4+ CD8+ induite par l'anti-CD3. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
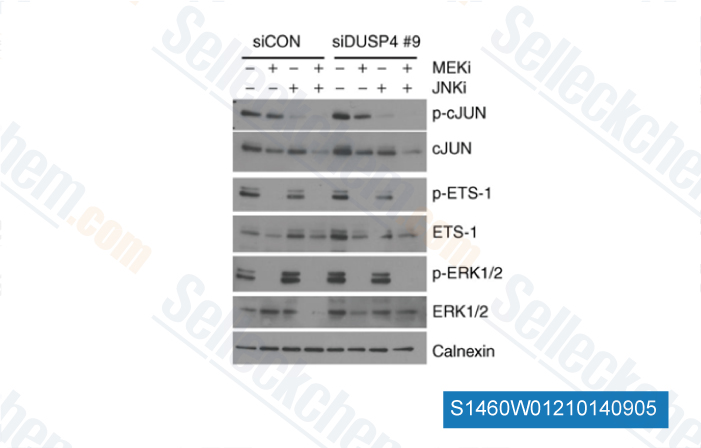
-
Données de [ Cancer Res , 2013 , 73(20):6346-58 ]
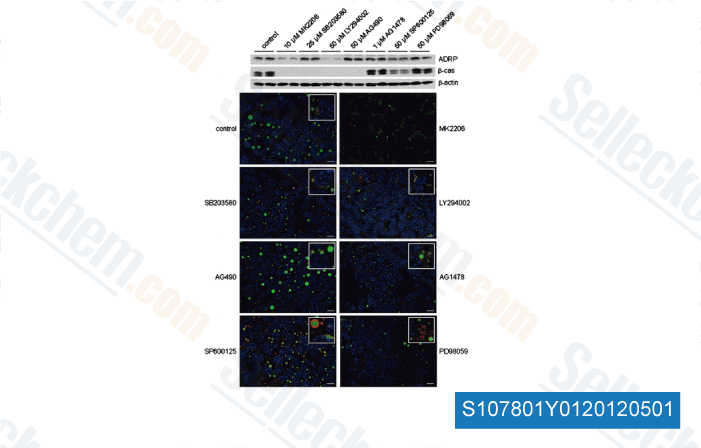
-
Données de [ Biochim Biophys Acta , 2012 , 1823(5), 987-96 ]
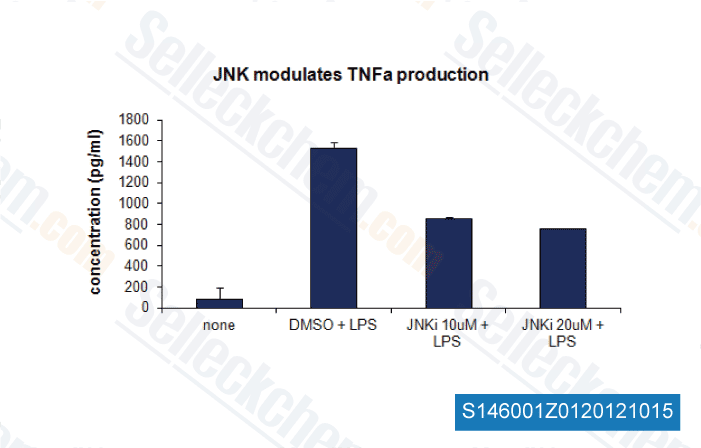
-
, , Lee lay hoon from National University of Singapore
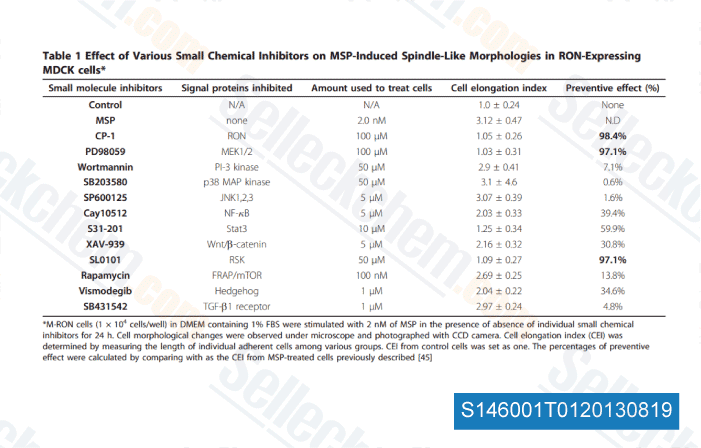
-
,
Sellecks SP600125 A été cité par 1098 Publications
| Nucleus-translocated glucokinase functions as a protein kinase to phosphorylate TAZ and promote tumour growth [ Nat Commun, 2025, 16(1):7156] | PubMed: 40759645 |
| Gut Microbiota Modulates Obesity-Associated Skeletal Deterioration Through Macrophage Aging and Grancalcin Secretion [ Adv Sci (Weinh), 2025, 12(28):e2502634] | PubMed: 40349163 |
| Orosomucoid 1 Ameliorates Temporomandibular Joint Osteoarthritis by Maintaining Cartilage Homeostasis [ Adv Sci (Weinh), 2025, 12(36):e00028] | PubMed: 40583170 |
| Enhancing radiosensitivity of osteosarcoma by ITGB3 knockdown: a mechanism linked to enhanced osteogenic differentiation status through JNK/c-JUN/RUNX2 pathway activation [ J Exp Clin Cancer Res, 2025, 44(1):159] | PubMed: 40410897 |
| Hypoxia-induced degradation of FTO promotes apoptosis by unmasking RACK1-mediated activation of MTK1-JNK1/2 pathway [ J Adv Res, 2025, S2090-1232(25)00038-4] | PubMed: 39805423 |
| FNDC5/irisin-enriched sEVs conjugated with bone-targeting aptamer alleviate osteoporosis: a potential alternative to exercise [ J Nanobiotechnology, 2025, 23(1):504] | PubMed: 40652239 |
| Lipin3 deficiency aggravates cisplatin induced acute kidney injury via activating Sirt1-p21-Caspase 3-GSDME pyroptosis pathway [ Int J Biol Sci, 2025, 21(12):5185-5205] | PubMed: 40959286 |
| RNA polymerase II subunit 5-mediating protein limits TLR4-induced innate immune activation in macrophages by inhibiting IKKβ/NF-κB signaling during sepsis [ Cell Commun Signal, 2025, 23(1):274] | PubMed: 40495190 |
| CDO1 phosphorylation is required for IL-6-induced tumor cell proliferation through governing cysteine availability [ Cell Commun Signal, 2025, 23(1):194] | PubMed: 40269955 |
| M2 macrophage-derived extracellular vesicles protect against abdominal aortic aneurysm by modulating macrophage polarization through miR221-5p [ Cell Mol Biol Lett, 2025, 30(1):96] | PubMed: 40784924 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
