Données techniques
| Formule | C24H16F3NO4 |
||||||||||
| Poids moléculaire | 439.38 | Numéro CAS | 393105-53-8 | ||||||||
| Solubilité (25°C)* | In vitro | DMSO | 72 mg/mL (163.86 mM) | ||||||||
| Ethanol | 18 mg/mL (40.96 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||
Préparation des solutions mères
Activité biologique
| Description | PAI-039 (Tiplaxtinin) est un inhibiteur oralement efficace et sélectif de l'inhibiteur de l'activateur du plasminogène-1 (PAI-1) avec une IC50 de 2,7 μM. | ||
|---|---|---|---|
| Cibles |
|
||
| In vitro | Tiplaxtinin (PAI-039) réduit la prolifération cellulaire, l'adhésion cellulaire et la formation de colonies, et induit l'apoptose et l'anoïkis dans un panel de lignées cellulaires de vessie humaine. | ||
| In vivo | Il a été démontré dans de multiples études que Tiplaxtinin (PAI-039) présente divers effets biologiques. Dans un modèle de thrombose carotidienne chez le rat, il (1 mg/kg, p.o.) augmente le temps jusqu'à l'occlusion et prévient la réduction du flux sanguin carotidien. Chez les souris C57BL/6J, (1 mg/g de nourriture) il atténue le remodelage aortique induit par l'Ang II. Chez les souris diabétiques de type 1 non traitées, ce composé (p.o.) restaure la régénération musculaire squelettique. Chez les souris athymiques portant des xénogreffes de lignées cellulaires cancéreuses humaines T24 et HeLa, il (1 mg/kg, p.o.) réduit la croissance des xénogreffes tumorales, associée à une réduction de l'angiogenèse tumorale, une réduction de la prolifération cellulaire et une augmentation de l'apoptose. |
Protocole (de référence)
| Test kinase :[1] |
|
|---|---|
| Test cellulaire :[4] |
|
| Étude animale :[1] |
|
Références
|
Validation du produit par le client
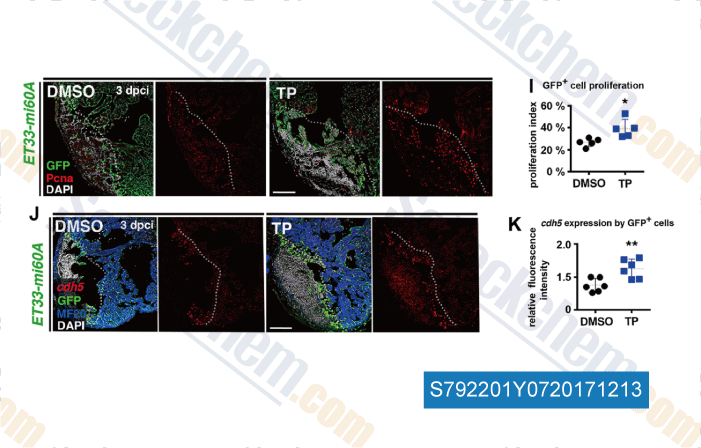
-
Données de [ , , Development, 2017, 144(8):1425-1440 ]
Sellecks Tiplaxtinin (PAI-039) A été cité par 17 Publications
| Modeling oxaliplatin resistance in colorectal cancer reveals a SERPINE1-based gene signature (RESIST-M) and therapeutic strategies for pro-metastatic CMS4 subtype [ Cell Death Dis, 2025, 16(1):529] | PubMed: 40664638 |
| Cellular senescence as a prognostic marker for predicting breast cancer progression in 2D and 3D organoid models [ Biomed Pharmacother, 2025, 189:118324] | PubMed: 40616881 |
| ProBDNF as a Myokine in Skeletal Muscle Injury: Role in Inflammation and Potential for Therapeutic Modulation of p75NTR [ Int J Mol Sci, 2025, 26(1)401] | PubMed: 39796256 |
| hapln1a+ cells guide coronary growth during heart morphogenesis and regeneration [ Nat Commun, 2023, 14(1):3505] | PubMed: 37311876 |
| CSE reduces OTUD4 triggering lung epithelial cell apoptosis via PAI-1 degradation [ Cell Death Dis, 2023, 14(9):614] | PubMed: 37726265 |
| CSE reduces OTUD4 triggering lung epithelial cell apoptosis via PAI-1 degradation [ Cell Death Dis, 2023, 10.1038/s41419-023-06131-1] | PubMed: 37726265 |
| Ligand-mediated PAI-1 inhibition in a mouse model of peritoneal carcinomatosis [ Cell Rep Med, 2022, 3(2):100526] | PubMed: 35243423 |
| ProBDNF Dependence of LTD and Fear Extinction Learning in the Amygdala of Adult Mice [ Cereb Cortex, 2022, 32(7):1350-1364] | PubMed: 34470044 |
| Development of potent and selective inhibitors targeting the papain-like protease of SARS-CoV-2 [ Cell Chem Biol, 2021, S2451-9456(21)00213-0] | PubMed: 33979649 |
| Cancer‑associated fibroblast‑induced M2‑polarized macrophages promote hepatocellular carcinoma progression via the plasminogen activator inhibitor‑1 pathway [ Int J Oncol, 2021, 59(2)59] | PubMed: 34195849 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
