Données techniques
| Formule | C23H24O8 |
||||||
| Poids moléculaire | 428.43 | Numéro CAS | 19545-26-7 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 85 mg/mL (198.39 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Ajouter les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | La Wortmannine est le premier inhibiteur de PI3K décrit avec une IC50 de 3 nM dans un essai sans cellules, avec peu de sélectivité au sein de la famille PI3K. La Wortmannine bloque la formation d'autophagosomes et inhibe puissamment DNA-PK/ATM avec une IC50 de 16 nM et 150 nM dans des essais sans cellules. La Wortmannine inhibe également l'activité de PLK1. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||||
| In vitro | L'inhibition de MLCK par la Wortmannine n'est pas affectée par la calmoduline ou le substrat peptidique, tandis qu'elle est réduite par une forte concentration d'ATP. Ce composé interagit directement avec le domaine catalytique de MLCK et entraîne une perte irréversible de l'activité enzymatique. Il n'a pas d'effet inhibiteur sur la protéine kinase dépendante de l'AMPc, la protéine kinase dépendante du GMPc et la protéine kinase II dépendante de la calmoduline, et a peu d'effet sur l'activité de la protéine kinase C. Cet inhibiteur inhibe la formation de PtdInsP3 (phosphatidylinositol 3,4,5-trisphosphate) stimulée par le N-formylméthionyl-leucylphénylalanine (fMLP) avec une IC50 de 5 nM et cette inhibition est complètement abolie lorsque les neutrophiles humains sont prétraités avec 100 nM de ce composé, avec des niveaux de PtdInsP2 augmentés et aucun effet sur les teneurs cellulaires en PtdInsP et PtdIns. Il pourrait développer des changements oscillatoires de la teneur en F-actine et n'inhibe pas la polymérisation de l'actine stimulée par le fMLP dans les neutrophiles. Ce produit chimique inhibe irréversiblement l'activité de la phosphatidylinositol 3-kinase (PI3-kinase) en se liant à la protéine de 110 kDa (IC50 de 3 nM) et n'a aucun effet sur la PI4-kinase dans les cellules RBL-2H3. Il inhibe également la libération de leucotriènes, sans effet sur l'activation de la tyrosine kinase Lyn. Ce composé abolit complètement l'absorption de l'hexose induite dans les adipocytes de rat isolés à 0,1 μM, sans altérer l'activité lipolytique stimulée. Il supprime la production induite d'oxyde nitrique de 50 % à 500 nM dans les cellules endothéliales de la veine ombilicale humaine, en réponse à l'IGF-1. Ce produit chimique supprime la réparation des cassures double brin de l'ADN (DSB) et n'a aucun effet sur les niveaux de DSB ou la cinétique de réparation des cassures simple brin (SSB) dans les cellules ovariennes de hamster chinois à 50 μM. Il pourrait potentialiser la cytotoxicité induite par les rayonnements ionisants (IR) sans toxicité propre. Cet inhibiteur inhibe l'activité de la polo-like kinase (PLK1) avec une IC50 de 24 nM dans des cellules intactes arrêtées en G2/M. Il augmente l'accumulation d'IL-6 médiée par les récepteurs Toll-like (TLR) dans les macrophages humains avec une EC50 de 50 nM. Parallèlement, ce composé améliore significativement l'expression de la monoxyde d'azote synthase inductible (iNOS) médiée par les TLR et l'accumulation de nitrites dans les macrophages de souris. Il active le facteur nucléaire-κB et régule à la hausse la production d'ARNm des cytokines. Ce produit chimique inhibe également la polo-like kinase (PlK) 1 et PlK3, qui jouent des rôles importants dans la mitose. Son traitement pourrait entraîner une réduction de la phosphorylation de p53 sur la sérine 20 induite par les dommages à l'ADN. Il supprime la phosphorylation d'Akt induite par l'hyaluronane et la motilité/migration cellulaire dans les cellules SW1990. |
||||||||
| In vivo | La Wortmannine inhibe la métastase péritonéale des cellules SW1990 chez la souris à 1 mg/kg, sans perte de poids. Ce composé inhibe la phosphorylation de la phosphatidylinositide 3-kinase-protéine kinase B (PKB)/Akt dans les tissus normaux (homogénats de poumon, de cœur et de cerveau) et le tissu tumoral chez la souris, sans mortalité ni toxicité aiguë à 0,7 mg/kg. En combinaison avec le LY188011, ce produit chimique augmente significativement l'apoptose et inhibe la croissance tumorale dans le cas d'une tumeur orthotopique, alors que les deux monothérapies n'y parvenaient pas. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
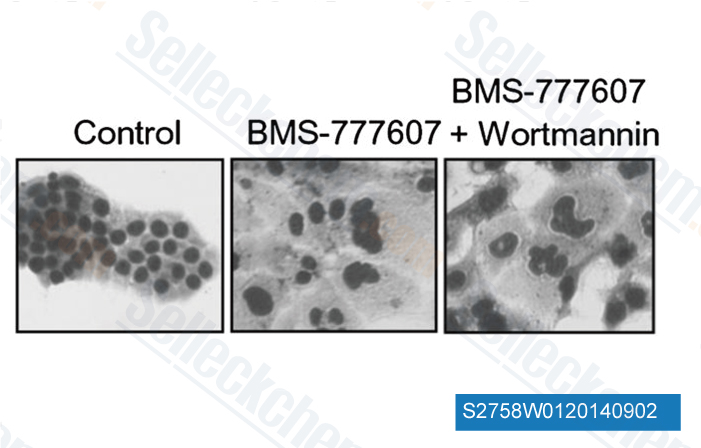
-
Données de [ Mol Cancer Ther , 2014 , 13(1), 37-48 ]
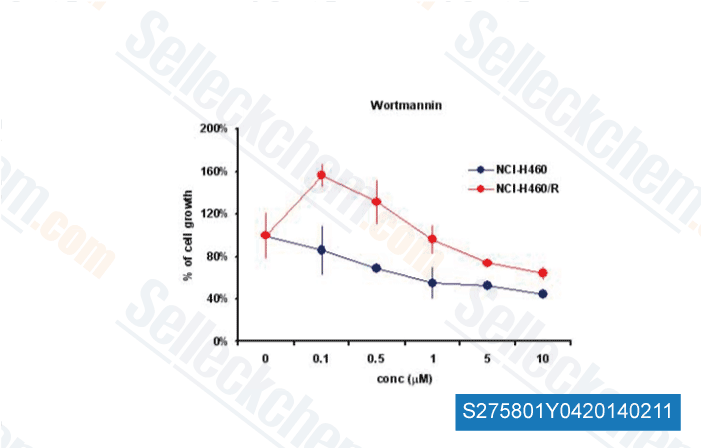
-
, 2014 , Dr.Milica Pesic from Institute for Biological Research
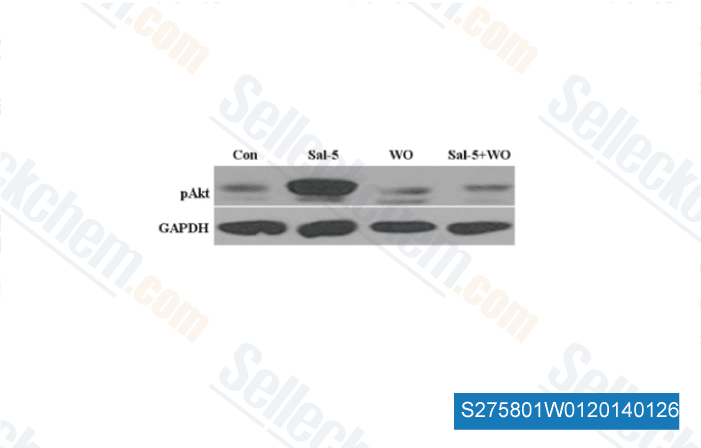
-
Données de [ Int J Mol Sci , 2013 , 14(9), 17304-18 ]
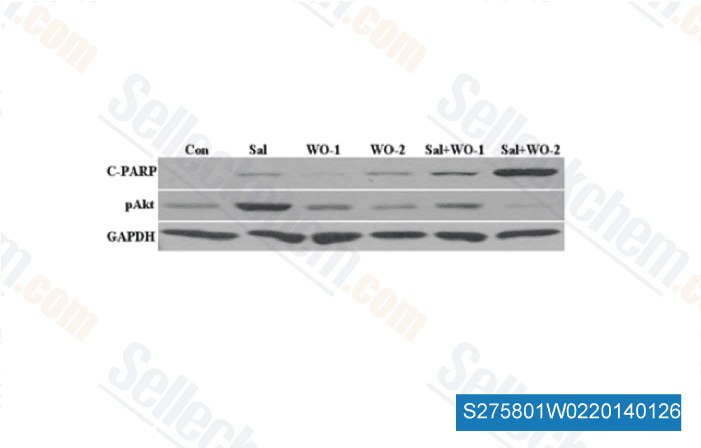
-
Données de [ Int J Mol Sci , 2013 , 14(9), 17304-18 ]
Sellecks Wortmannin (SL-2052) A été cité par 343 Publications
| USP5 stabilizes YTHDF1 to control cancer immune surveillance through mTORC1-mediated phosphorylation [ Nat Commun, 2025, 16(1):1313] | PubMed: 39900921 |
| Cardiolipin inhibits the non-canonical inflammasome by preventing LPS binding to caspase-4/11 [ EMBO J, 2025, 10.1038/s44318-025-00507-z] | PubMed: 40670771 |
| Selective tubulin-binding drugs induce pericyte phenotype switching and anti-cancer immunity [ EMBO Mol Med, 2025, 10.1038/s44321-025-00222-6] | PubMed: 40140727 |
| Mechanical force-induced oncostatin M secretion by Jun-positive neutrophils promotes craniofacial bone regeneration for midface hypoplasia treatment [ Stem Cell Res Ther, 2025, 16(1):330] | PubMed: 40598376 |
| Siramesine induced cell death of glioblastoma through inactivating the STAT3-MGMT signaling pathway [ J Transl Med, 2025, 23(1):780] | PubMed: 40640878 |
| Depleting the action of EZH2 through PI3K-mTOR inhibition to overcome metastasis and immunotherapy resistance in triple-negative breast cancer [ Mol Cancer Ther, 2025, 10.1158/1535-7163.MCT-24-0693] | PubMed: 40497697 |
| Cepharanthine hydrochloride: a novel ferroptosis-inducing agent for prostate cancer treatment [ Front Pharmacol, 2025, 16:1536375] | PubMed: 40066333 |
| Intracellular Sphingosine-1-Phosphate Induces Lipolysis Through Direct Activation of Protein Kinase C Zeta [ FASEB J, 2025, 39(7):e70528] | PubMed: 40193069 |
| Vegfr3 activation of Pkd2l1+ CSF-cNs triggers the neural stem cell response in spinal cord injury [ Cell Signal, 2025, 130:111675] | PubMed: 39986360 |
| RhFGF21 protected PC12 cells against mitochondrial apoptosis triggered by H2O2 via the AKT-mediated ROS signaling pathway [ Exp Cell Res, 2025, 445(1):114417] | PubMed: 39793749 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
