pour la recherche uniquement
Cyclophosphamide Monohydrate Alkylating Agent
Réf. CatalogueS2057
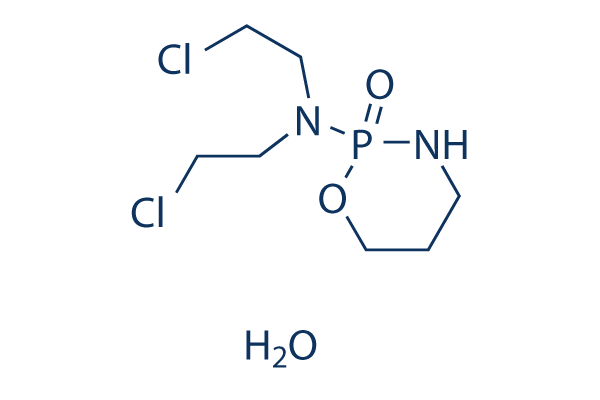
Structure chimique
Poids moléculaire: 279.1
Contrôle Qualité
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| HL60 cells | Cytotoxicity assay | Cytotoxicity against human HL60 cells by MTT assay, IC50=8.79 μM | 20850303 | |||
| BALB/c 3T3 cells | Cytotoxicity assay | In vitro cytotoxicity was evaluated in mouse embryo BALB/c 3T3 cells, IC50=37.6 μM | 9873412 | |||
| BALB/c 3T3 | Cytotoxicity assay | In vitro cytotoxicity against BALB/c 3T3 cells, IC50 = 37.6 μM. | 7877150 | |||
| T-cells | Immunosuppressive assay | 100 mg/kg | 8 days | Immunosuppressive activity against MAV-1 infected BALB/c mouse assessed as T cells suppression at 100 mg/kg, ip treated 8 days before infection for 4 weeks measured 14 days post infection by flow cytometry | 18268085 | |
| B-cells | Immunosuppressive assay | 100 mg/kg | 8 days | Immunosuppressive activity against MAV-1 infected BALB/c mouse assessed as B cells suppression at 100 mg/kg, ip treated 8 days before infection for 4 weeks measured 14 days post infection by flow cytometry | 18268085 | |
| U87 MG | Antitumor assay | 80 mg/kg | Antitumor activity in human U87 MG cells xenografted mouse at 80 mg/kg, iv administered in Q2D x 5 schedule | 18450456 | ||
| MX1 | Antitumor assay | 120 mg/kg | up to 3 weeks | Antitumor activity against human MX1 cells xenografted in nude mouse adjuvant model assessed as increase in mouse survival time at 120 mg/kg, po BID measured up to 3 weeks | 20726512 | |
| U87MG | Anticancer assay | 80 mg/kg | 6 days | Anticancer activity against human U87MG cells xenografted in athymic mouse assessed as tumor suppression at 80 mg/kg, iv Q2D for 6 days | 21106377 | |
| NCI-H522 | Antitumor assay | 50 mg/kg | 28 days | Antitumor activity against human NCI-H522 cells xenografted in Balb/c nude mouse assessed as tumor growth inhibition at 50 mg/kg, ig administered once daily for 28 days relative to control | 28092860 | |
| U2932 | Antitumor assay | 50 mg/kg | 5 consecutive days | Antitumor activity against human U2932 cells xenografted in SCID mouse assessed as reduction in tumor burden at 50 mg/kg, ip administered for 5 consecutive days measured up to day 40 post cell injection | 28605593 | |
| MDA-MB-231 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) MDA-MB-231 cells after 48 hr by MTT assay, IC50 = 0.09 μM. | ChEMBL | ||
| K562 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) K562 cells after 48 hr by MTT assay, IC50 = 0.15 μM. | ChEMBL | ||
| K562 | Antiproliferative assay | 48 hr | Antiproliferative activity against Homo sapiens (human) K562 cells after 48 hr by MTT assay, IC50 = 0.153 μM. | ChEMBL | ||
| MCF7 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) MCF7 cells after 48 hr by SRB assay, IC50 = 10 mM. | 19372630 | ||
| HepG2 | Cytotoxicity assay | 48 hr | Cytotoxicity against Homo sapiens (human) HepG2 cells after 48 hr by MTT assay, IC50 = 0.24 μM. | ChEMBL | ||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 279.1 | Formule | C7H15Cl2N2O2P.H2O |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 6055-19-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | NSC-26271 Monohydrate | Smiles | C1CNP(=O)(OC1)N(CCCl)CCCl.O | ||
Solubilité
|
In vitro |
DMSO
: 55 mg/mL
(197.06 mM)
Water : 55 mg/mL Ethanol : 55 mg/mL |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
La Cyclophosphamide (CY) est un agent chimiothérapeutique avec un effet bimodal dose-dépendant sur le système immunitaire. Le traitement par Cyclophosphamide améliore l'apoptose et diminue la prolifération homéostatique des lymphocytes T régulateurs. La Cyclophosphamide régule à la baisse l'expression de GITR et FoxP3, qui sont impliqués dans l'activité suppressive des T(REGs). La Cyclophosphamide augmente les niveaux de protéines CYP3A4, CYP2C8 et CYP2C9 dans les cultures d'hépatocytes humains primaires, ce qui améliore ainsi leurs propres taux de 4-hydroxylation dans les hépatocytes en culture. La Cyclophosphamide a produit des mutations dans des souches de Salmonella tryphimurium substituant les paires de bases en présence d'activation métabolique, mais elle s'est avérée négative dans le chromotest E. coli. La Cyclophosphamide a montré qu'elle produisait des mutations géniques, des aberrations chromosomiques, des micronoyaux et des échanges de chromatides sœurs dans une variété de cellules cultivées en présence d'activation métabolique ainsi que des échanges de chromatides sœurs sans activation métabolique. |
|---|---|
| In vivo |
La Cyclophosphamide a également produit des dommages chromosomiques et des micronoyaux chez les rats, les souris et les hamsters chinois, et des mutations géniques dans le test de tache de la souris et dans le construit lacZ transgénique de Muta Mouse. La Cyclophosphamide, administrée selon une séquence définie avec un vaccin à cellules entières sécrétant du GM-CSF et exprimant neu, améliore le potentiel du vaccin à retarder la croissance tumorale chez les souris transgéniques neu. La Cyclophosphamide exerce ses effets en améliorant l'efficacité du vaccin plutôt que par un effet cytolytique direct sur les cellules cancéreuses. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | PTEN / pAkt / Caspase 3 / GAPDH Caspase 3 / Cleaved-Caspase 3 / Cleaved-PARP / Tubulin Nuclear AIF / Cytosolic AIF / TBP / GAPDH LC3B I / LC3B II / GAPDH |
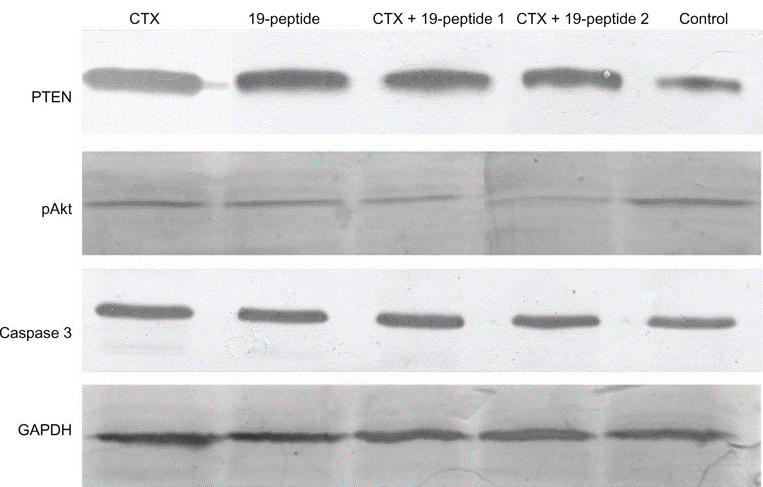
|
23874108 |
| Growth inhibition assay | Cell Viability Tumor Volume Tumor Volume |
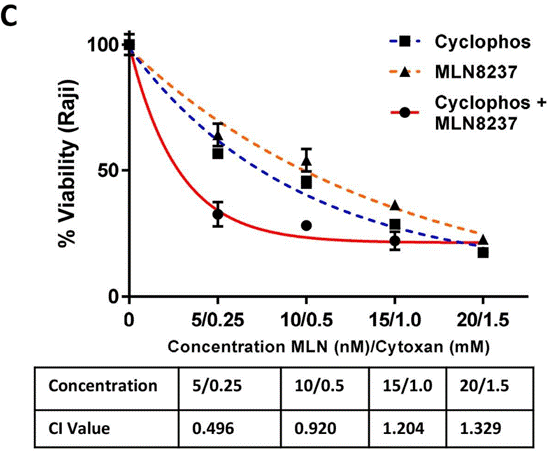
|
31429028 |
| IHC | tumor cell invasion TUNEL / Caspase 3 PTEN / pAkt / PCNA ovary of mice Caspase-3 |
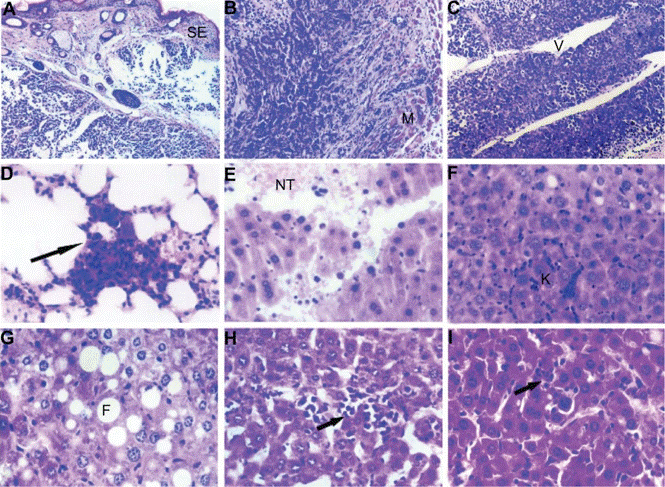
|
23874108 |
| Immunofluorescence | pAKT / pERK Ki-67 / UPK3 / KRT5 / pERK Ki-67 / KRT14 / KRT5 autophagy levels |
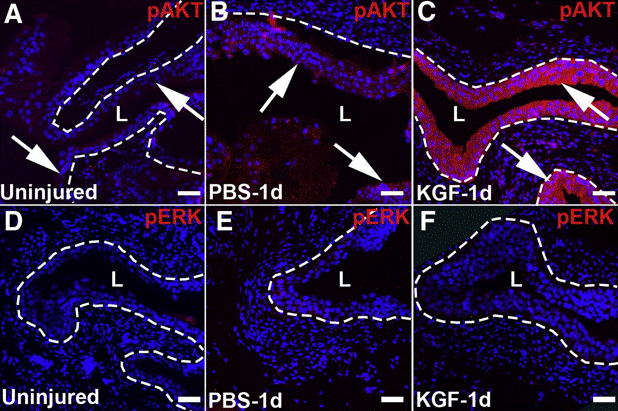
|
31654636 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06186700 | Active not recruiting | Breast Cancer Female |
Mansoura University |
December 25 2023 | Phase 2 |
| NCT06085742 | Recruiting | Breast Cancer |
University of Illinois at Chicago |
November 22 2023 | Phase 2 |
| NCT05800041 | Not yet recruiting | Gout Tophus |
RenJi Hospital|Westlake Therapeutics |
April 10 2023 | Early Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
Foire aux questions
Question 1:
Why does it show no activity in vitro assays?
Réponse :
The activity of this compound in vitro is controversial and has not been fully determined. It is a prodrug and may need Cytochrome P450 to convert it to the active form: 4-hydroxy cyclophosphamide. It is widely used in vivo, if you are going to use it in vitro, you may need to supplement Cytochrome P450 exogenously.
