réservé à la recherche
PF-5274857 Hedgehog/Smoothened antagoniste
N° Cat.S2777
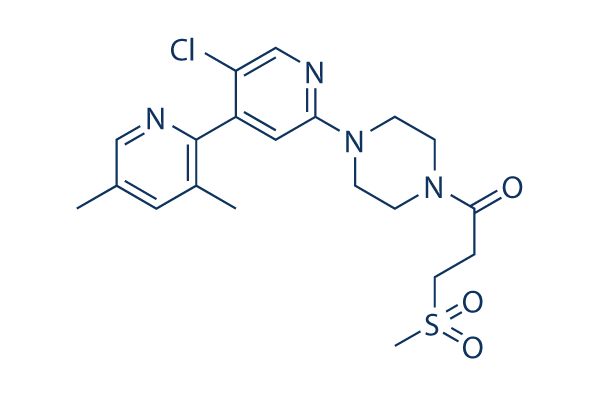
Structure chimique
Poids moléculaire: 436.96
Contrôle qualité
| Cibles apparentées | JAK TGF-beta/Smad Wnt/beta-catenin ERK GSK-3 ROCK PKA Secretase STAT Casein Kinase |
|---|---|
| Autre Hedgehog/Smoothened Inhibiteurs | SAG (Smoothened Agonist) Hydrochloride Purmorphamine Cyclopamine (11-Deoxojervine) GANT61 SAG (Smoothened Agonist) SANT-1 HPI-4 (Ciliobrevin A) BMS-833923 Taladegib (LY2940680) Ciliobrevin D |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 436.96 | Formule | C20H25ClN4O3S |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1373615-35-0 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CC1=CC(=C(N=C1)C2=CC(=NC=C2Cl)N3CCN(CC3)C(=O)CCS(=O)(=O)C)C | ||
Solubilité
|
In vitro |
DMSO
: 93 mg/mL
(212.83 mM)
Water : 93 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Smoothened
4.6 nM(Ki)
Smoothened
5.8 nM
|
|---|---|
| In vitro |
PF-5274857 inhibe complètement l'activité de la voie Hh induite par Shh avec un IC50 de 2,7 nM mesuré par l'activité transcriptionnelle du gène en aval de Smo, Gli1, dans les cellules MEF. Le récepteur μ-opioïde est faiblement inhibé par ce composé avec une constante de dissociation de 36 μM déterminée ultérieurement dans un essai fonctionnel.
|
| Kinase Assay |
Essais biochimiques
|
|
Les cellules HEK293 surexprimant la protéine Smo humaine (acides aminés 181-787) sont cultivées dans du milieu de Dulbecco's Modified Eagle's Media (DMEM) supplémenté avec 10% de FBS, de la Pénicilline-Streptomycine et 0,1 mg/mL d'hygromycine jusqu'à 90% de confluence. Après lavage avec du PBS de Dulbecco froid, le culot cellulaire est remis en suspension dans un tampon de préparation membranaire (50 mM Tris-HCl, pH 7,5, 250 mM saccharose avec un cocktail de protéase complet de Roche) et homogénéisé. L'homogénat est centrifugé et le culot cellulaire est remis en suspension dans un tampon d'essai (50 mM Tris-HCl, pH 7,5, 100 mM NaCl, 25 mM MgCl2, 1 mM EDTA et 0,1% d'albumine sérique bovine sans protéase) et homogénéisé dans un broyeur de tissus en verre. La quantité totale de protéines dans la préparation membranaire contenant Smo est déterminée à l'aide de l'essai protéique Pierce BCA. Pour l'essai de liaison compétitive, 100 μL de tampon d'essai sont ajoutés à une plaque filtrante GF/B à 96 puits pendant 10 minutes pour pré-humidifier le filtre, puis retirés. Les réactifs suivants sont ensuite ajoutés : 20 μL de tampon d'essai, 10 μL de dilutions en série de ce composé, 20 μL d'antagoniste 3H-Smo (concentration finale de 3 nM) et 50 μL de préparation membranaire (40 μg de protéines totales). Les plaques sont incubées à température ambiante pendant 2 heures, puis lavées et séchées sous vide. Les plaques sont ensuite séchées pendant 1 heure dans un four à 60°C avant l'ajout de 45 μL de Microscint 20 et incubées à température ambiante pendant 30 minutes à 1 heure, puis comptées dans un compteur à scintillation TopCount. Les données sont analysées à l'aide du logiciel GraphPad Prism.
|
|
| In vivo |
PF-5274857 montre une inhibition significative de la croissance tumorale (TGI) dose-dépendante et induit une régression tumorale à des doses élevées (>10 mg/kg). Ce composé régule négativement les niveaux d'expression des gènes Gli1, Gli2, Ptch1 et Ptch2 à divers degrés, avec des effets maximaux atteints entre 6 et 12 heures post-dose (Gli1 étant le gène le plus sensible), tandis qu'il a peu d'effet sur les niveaux de Smo. Dans le tissu cutané, une régulation négative de Gli1 et Gli2 est également observée avec une cinétique similaire par ce produit chimique. La concentration médicamenteuse dérivée du modèle pour une inhibition semi-maximale du taux de production d'ARNm de Gli1 tumoral (IC50) par ce composé est déterminée à 8,9 nM chez les souris allogreffées de médulloblastome Ptch+/−p53+/−, ce qui correspond mathématiquement à une régression tumorale de 119% TGI après 6 jours d'exposition plasmatique à cette concentration. Chez les souris allogreffées de médulloblastome Ptch+/−p53−/−, la valeur de l'IC50 est estimée à 3,5 nM, ce qui est cohérent avec les résultats Ptch+/−p53+/−. Il est également capable de traverser la barrière hémato-encéphalique chez le rat dans les 4 heures suivant l'administration.
|
Références |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
