réservé à la recherche
Sonidegib (NVP-LDE225, Erismodegib) Antagoniste de Smo
N° Cat.S2151
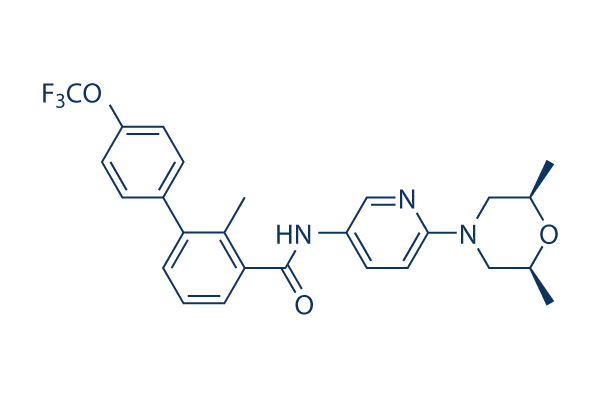
Structure chimique
Poids moléculaire: 485.5
Contrôle qualité
| Cibles apparentées | JAK TGF-beta/Smad Wnt/beta-catenin ERK GSK-3 ROCK PKA Secretase STAT Casein Kinase |
|---|---|
| Autre Hedgehog/Smoothened Inhibiteurs | SAG (Smoothened Agonist) Hydrochloride Purmorphamine Cyclopamine (11-Deoxojervine) GANT61 SAG (Smoothened Agonist) SANT-1 HPI-4 (Ciliobrevin A) BMS-833923 Taladegib (LY2940680) Ciliobrevin D |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| A2780ip2 | Cytoxicity assay | ~10 μM | IC50=12 μM | 22553355 | ||
| A2780cp20 | Cytoxicity assay | ~10 μM | IC50=7.5 μM | 22553355 | ||
| SKOV3ip1 | Cytoxicity assay | ~10 μM | IC50=24 μM | 22553355 | ||
| SKOV3TRip2 | Cytoxicity assay | ~10 μM | IC50=12 μM | 22553355 | ||
| HeyA8 | Cytoxicity assay | ~10 μM | IC50=18 μM | 22553355 | ||
| HeyA8MDR | Cytoxicity assay | ~10 μM | IC50=8 μM | 22553355 | ||
| OS5 | Growth inhibitory assay | ~5 μM | reduces the proliferation | 23243595 | ||
| OS18 | Growth inhibitory assay | ~5 μM | reduces the proliferation | 23243595 | ||
| Glioblastoma initiating cells | Cytoxicity assay | ~10 μM | Inhibits Cell Viability | 23482671 | ||
| Glioblastoma initiating cells | Function assay | ~10 μM | inhibits neurosphere formation | 23482671 | ||
| Glioblastoma initiating cells | Cytoxicity assay | ~10 μM | induces apoptosis | 23482671 | ||
| Glioblastoma initiating cells | Function assay | ~10 μM | downregulates the SHH signaling pathway | 23482671 | ||
| Glioblastoma initiating cells | Function assay | ~10 μM | Inhibits the Expression of Genes Involved in Maintaining Pluripotency | 23482671 | ||
| Glioblastoma initiating cells | Function assay | ~10 μM | Inhibits Motility, Invasion, and Migration | 23482671 | ||
| LOX IMVI | Function assay | 10 μM | DMSO | inhibits Hedgehog-GLI pathway | 23935925 | |
| UACC 257 | Function assay | 10 μM | DMSO | inhibits Hedgehog-GLI pathway | 23935925 | |
| LOX IMVI | Function assay | 10 μM | DMSO | induces G1 cell cycle arrest | 23935925 | |
| UACC 257 | Function assay | 10 μM | DMSO | induces G1 cell cycle arrest | 23935925 | |
| LOX IMVI | Cytoxicity assay | 10 μM | DMSO | decreases tumor cell viability | 23935925 | |
| UACC 257 | Cytoxicity assay | 10 μM | DMSO | decreases tumor cell viability | 23935925 | |
| LOX IMVI | Apoptosis assay | 10 μM | DMSO | induces apoptosis | 23935925 | |
| UACC 257 | Apoptosis assay | 10 μM | DMSO | induces apoptosis | 23935925 | |
| ACHN | Growth inhibitory assay | ~5 μM | DMSO | IC50=2-3 μM | 25093491 | |
| 769-P | Growth inhibitory assay | ~5 μM | DMSO | IC50=2-3 μM | 25093491 | |
| 786-O | Growth inhibitory assay | ~5 μM | DMSO | IC50=2-3 μM | 25093491 | |
| 786-O SuR | Growth inhibitory assay | ~5 μM | DMSO | IC50=2-3 μM | 25093491 | |
| SP53 | Function assay | 30 μM | DMSO | inhibits cell adhesion and migration | 26885608 | |
| SP53 | Function assay | 30 μM | DMSO | inhibits the VLA4-mediated FAK signaling pathway | 26885608 | |
| HS5 | Function assay | 30 μM | DMSO | inhibits cell adhesion and migration | 26885608 | |
| HS27a | Function assay | 30 μM | DMSO | inhibits cell adhesion and migration | 26885608 | |
| SP53 | Cytoxicity assay | 30 μM | DMSO | induces autophagy | 26885608 | |
| Jeko | Cytoxicity assay | 30 μM | DMSO | induces autophagy | 26885608 | |
| U2OS | Function assay | 2 hrs | Displacement of [3H]cyclopamine from wild type Smo expressed in U2OS cells after 2 hrs by scintillation counting, Ki = 0.006 μM. | 23063522 | ||
| NIH/3T3 | Function assay | Inhibition of hedgehog signaling pathway in mouse NIH/3T3 cells expressing wild type Smo assessed as reduction in Gli mRNA expression by RT-PCR method, IC50 = 0.0044 μM. | 27810591 | |||
| NIH/3T3 | Function assay | Inhibition of hedgehog signaling pathway in mouse NIH/3T3 cells harboring Smo D477H mutant assessed as reduction in Gli mRNA expression by RT-PCR method, IC50 = 0.0227 μM. | 27810591 | |||
| NIH/3T3 | Function assay | 24 hrs | Inhibition of hedgehog signaling pathway in mouse NIH/3T3 cells measured after 24 hrs by Gli-dual luciferase reporter gene assay, IC50 = 0.006 μM. | 27810591 | ||
| TM3 | Function assay | 48 hrs | Inhibition of Hh signaling pathway in mouse TM3 cells assessed as downregulation of Gli1 gene expression after 48 hrs by luciferase reporter gene assay, EC50 = 0.0012 μM. | 26976215 | ||
| NIH3T3 | Function assay | 48 hrs | Inhibition of SHH signaling pathway in mouse NIH3T3 cells measured after 48 hrs by Gli-luciferase reporter assay, IC50 = 0.0055 μM. | 24176396 | ||
| NIH3T3 | Function assay | 48 hrs | Inhibition of Sonic-induced hedgehog signalling in mouse NIH3T3 cells after 48 hrs by Gli-luciferase reporter assay, IC50 = 0.0055 μM. | 26820554 | ||
| NIH/3T3 | Function assay | Inhibition of hedgehog signaling pathway expressed in mouse NIH/3T3 cells assessed as inhibition of hedgehog-induced Gli-2 accumulation at tip of primary cilia by DAPI staining based confocal microscopic analysis | 27810591 | |||
| NIH/3T3 | Function assay | Inhibition of hedgehog signaling pathway in mouse NIH/3T3 cells assessed as inhibition of hedgehog-induced Smo-EGFP ciliary translocation by DAPI staining based confocal microscopic analysis | 27810591 | |||
| MG 63 (6-TG R) | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for MG 63 (6-TG R) cells | 29435139 | |||
| Rh41 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for Rh41 cells | 29435139 | |||
| U-2 OS | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for U-2 OS cells | 29435139 | |||
| A673 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| BT-12 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-12 cells | 29435139 | |||
| MG 63 (6-TG R) | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for MG 63 (6-TG R) cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| OHS-50 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| Saos-2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| SK-N-MC | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| SK-N-SH | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-SH cells | 29435139 | |||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 485.5 | Formule | C26H26F3N3O3 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 956697-53-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | NVP-LDE225, Erismodegib | Smiles | CC1CN(CC(O1)C)C2=NC=C(C=C2)NC(=O)C3=CC=CC(=C3C)C4=CC=C(C=C4)OC(F)(F)F | ||
Solubilité
|
In vitro |
DMSO
: 97 mg/mL
(199.79 mM)
Ethanol : 16 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Smo (mouse)
(Cell-free assay) 1.3 nM
Smo (human)
(Cell-free assay) 2.5 nM
|
|---|---|
| In vitro |
Sonidegib (Erismodegib, NVP-LDE225) inhibe la lignée cellulaire luciférisée TM3 avec 0,6 nM et 8 nM, en présence de 1 nM et 25 nM d'agoniste Hh Ag1.5, respectivement.
|
| In vivo |
Sonidegib (Erismodegib, NVP-LDE225) est fortement lié aux protéines plasmatiques de souris, de rat et humaines (>99 %) et modérément lié aux protéines plasmatiques de chien et de singe (77 et 85 %, respectivement). Le LDE225 présente une perméabilité élevée (90,8 % chez l'homme) dans l'essai PAMPA. Le LDE225 montre une bonne biodisponibilité orale allant de 69 à 102 % chez les espèces précliniques lorsqu'il est administré en solution. Le LDE225 est une base faible avec un pKa mesuré de 4,20 et présente une solubilité aqueuse relativement faible. Le LDE225 démontre une activité antitumorale dose-dépendante. À une dose de 5 mg/kg/jour qd, le LDE225 inhibe significativement la croissance tumorale, correspondant à une valeur T/C de 33 %. Lorsque la dose est de 10 et 20 mg/kg/jour qd, le LDE225 entraîne respectivement 51 et 83 % de régression. L'inhibition de l'ARNm de Gli1 est corrélée à l'exposition tumorale et plasmatique au LDE225. Le LDE225 pénètre avec succès la barrière hémato-encéphalique chez les animaux porteurs de tumeurs et entraîne une inhibition de la croissance tumorale après 4 jours de traitement. Le LDE225 réduit significativement le volume tumoral de 95,7 % chez les souris Rip1-Tag2. Le LDE225 prolonge la survie chez les souris Rip1Tag2. Le LDE225 diminue l'expression des marqueurs stromaux chez les souris traitées au LDE225.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | p-p130CAS / p130CAS / p-FAK / FAK / p-Paxillin / Paxillin pp70S6K / P70s6k Gli-1 / Gli-2 / p-Akt / Akt Bcl2 / c-myc / Cyclin D1 / pERK / ERK / pJNK / JNK / Caspase 3 / Cleaved caspase 3 |
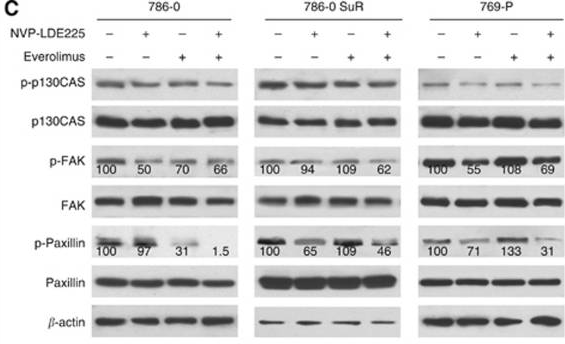
|
25093491 |
| Immunofluorescence | GLI1 |
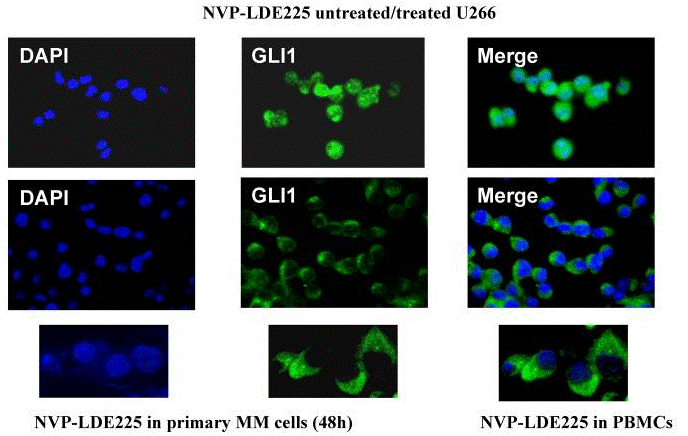
|
22821765 |
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT02358161 | Completed | Pancreatic Cancer |
Academisch Medisch Centrum - Universiteit van Amsterdam (AMC-UvA)|Novartis|Celgene Corporation |
September 2015 | Phase 1|Phase 2 |
| NCT02254551 | Terminated | Multiple Myeloma |
SCRI Development Innovations LLC|Novartis |
January 2015 | Phase 2 |
| NCT02138929 | Completed | Esophageal Cancer |
M.D. Anderson Cancer Center|Novartis|National Cancer Institute (NCI) |
November 10 2014 | Phase 1 |
| NCT02195973 | Completed | Recurrent Ovarian Cancer |
University of Alabama at Birmingham|Novartis Pharmaceuticals |
September 2014 | Phase 1 |
| NCT02027376 | Completed | Advanced Breast Cancer |
Spanish Breast Cancer Research Group|Novartis |
May 2014 | Phase 1 |
| NCT02111187 | Completed | Prostate Cancer |
Sidney Kimmel Comprehensive Cancer Center at Johns Hopkins |
April 2014 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
