pour la recherche uniquement
Bicalutamide Androgen Receptor antagoniste
Réf. CatalogueS1190
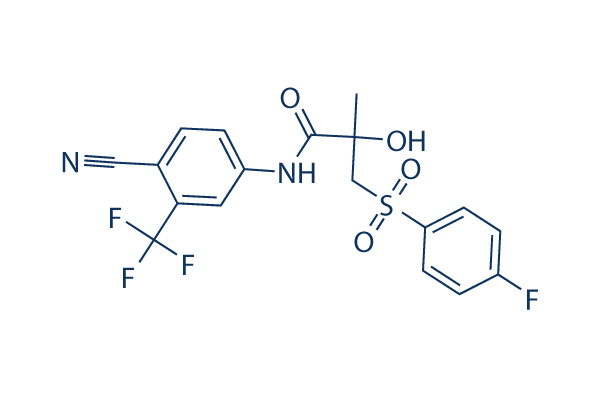
Structure chimique
Poids moléculaire: 430.37
Contrôle Qualité
| Cibles apparentées | Adrenergic Receptor Estrogen/progestogen Receptor GPR Glucocorticoid Receptor ACE RAAS Progesterone Receptor Opioid Receptor PGES THR |
|---|---|
| Autre Androgen Receptor Inhibiteurs | Bavdegalutamide (ARV-110) RU58841 EPI-001 Galeterone Cyproterone Acetate 3,3'-Diindolylmethane Ailanthone Proxalutamide (GT0918) AZD3514 Chlormadinone acetate |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| human MDA-MB-453 cells | Function assay | Displacement of [3H]R1881 from AR in human MDA-MB-453 cells, EC50=31 nM | ||||
| LNCaP cells | Function assay | Inhibition of [3H]-DHT binding to T877A androgen receptor of LNCaP cells, Ki=35 nM | ||||
| Freestyle293F cells | Function assay | Inhibition of wild type Androgen receptor (unknown origin) expressed in Freestyle293F cells, IC50=0.054 μM | ||||
| HEK293 cells | Function assay | 3 h | Displacement of [17-alpha-methyl-3H]mibolerone from androgen receptor expressed in HEK293 cells after 3 hrs, IC50=54 nM | |||
| MDA453 cells | Function assay | Displacement of [3H]DHT from human androgen receptor in MDA453 cells, Ki=64 nM | ||||
| human MDA-MB-453 cells | Function assay | Displacement of [3H]DHT from AR in human MDA-MB-453 cells, IC50=64 nM | ||||
| COS1 cells | Function assay | Antagonist activity against pSG5-tagged human androgen receptor expressed in COS1 cells assessed as reduction in receptor-mediated transcriptional activity by AR-regulated rat probasin promoter fragment driven firefly luciferase reporter assay, IC50=0.0869 μM | ||||
| HeLa cells | Function assay | Antagonist activity at human androgen receptor expressed in HeLa cells assessed as inhibition of dihydrotestosterone induced transcriptional activity by reporter gene assay, IC50=0.14 μM | ||||
| CV1 cells | Function assay | Binding affinity to human androgen receptor expressed in CV1 cells, Ki=0.151 μM | ||||
| monkey COS7 cells | Function assay | Binding affinity to human androgen receptor expressed in monkey COS7 cells by whole cell binding assay, Ki=0.151 μM | ||||
| COS7 cells | Function assay | Agonist activity at human androgen receptor W741C mutant expressed in COS7 cells assessed as luciferase activity after 24 hrs by reporter gene assay, EC50=0.18 μM | ||||
| CHO-K1 cells | Function assay | 2 h | Displacement of [3H]mibolerone from human AR expressed in CHO-K1 cells after 2 hrs by scintillation counting, IC50=0.2 μM | |||
| human HT-3 cell | Growth inhibition assay | Inhibition of human HT-3 cell growth in a cell viability assay, IC50=0.73134 μM | ||||
| human LNCAP cells | Proliferation assay | 3 days | Antiproliferative activity against human LNCAP cells after 3 days, IC50=0.7327 μM | |||
| human PC3 cells | Function assay | Displacement of [3H]R1881 from androgen receptor in human PC3 cells, EC50=4.3 μM | ||||
| human 22Rv1 cells | Function assay | 3 days | Antagonist activity at androgen receptor H874Y mutant (unknown origin) expressed in human 22Rv1 cells assessed as inhibition of DHT-induced cell growth after 3 days by WST-8 assay, IC50=4.6 μM | |||
| human CCF-STTG1 cell | Growth inhibition assay | Inhibition of human CCF-STTG1 cell growth in a cell viability assay, IC50=4.92929 μM | ||||
| human SCC-25 cell | Growth inhibition assay | Inhibition of human SCC-25 cell growth in a cell viability assay, IC50=6.08656 μM | ||||
| human MKN45 cell | Growth inhibition assay | Inhibition of human MKN45 cell growth in a cell viability assay, IC50=6.9605 μM | ||||
| human ES5 cell | Growth inhibition assay | Inhibition of human ES5 cell growth in a cell viability assay, IC50=8.61154 μM | ||||
| human SK-MEL-3 cell | Growth inhibition assay | Inhibition of human SK-MEL-3 cell growth in a cell viability assay, IC50=10.0964 μM | ||||
| human PC-3 cell | Growth inhibition assay | Inhibition of human PC-3 cell growth in a cell viability assay, IC50=10.2791 μM | ||||
| human NOS-1 cell | Growth inhibition assay | Inhibition of human NOS-1 cell growth in a cell viability assay, IC50=11.2917 μM | ||||
| human LB1047-RCC cell | Growth inhibition assay | Inhibition of human LB1047-RCC cell growth in a cell viability assay, IC50=12.253 μM | ||||
| human CAMA-1 cell | Growth inhibition assay | Inhibition of human CAMA-1 cell growth in a cell viability assay, IC50=12.3926 μM | ||||
| human SAS cell | Growth inhibition assay | Inhibition of human SAS cell growth in a cell viability assay, IC50=13.3081 μM | ||||
| human NCI-H2228 cell | Growth inhibition assay | Inhibition of human NCI-H2228 cell growth in a cell viability assay, IC50=13.7531 μM | ||||
| human NCI-H187 cell | Growth inhibition assay | Inhibition of human NCI-H187 cell growth in a cell viability assay, IC50=16.6616 μM | ||||
| human BFTC-905 cell | Growth inhibition assay | Inhibition of human BFTC-905 cell growth in a cell viability assay, IC50=17.4857 μM | ||||
| human G-361 cell | Growth inhibition assay | Inhibition of human G-361 cell growth in a cell viability assay, IC50=17.826 μM | ||||
| human DU145 cells | Cytotoxic assay | 72 h | Cytotoxicity against ERalpha-deficient human DU145 cells expressing ERbeta assessed as growth inhibition after 72 hrs by MTT assay, IC50=18 μM | |||
| human SW780 cell | Growth inhibition assay | Inhibition of human SW780 cell growth in a cell viability assay | ||||
| human BB49-HNC cell | Growth inhibition assay | Inhibition of human BB49-HNC cell growth in a cell viability assay, IC50=18.9532 μM | ||||
| human KALS-1 cell | Growth inhibition assay | Inhibition of human KALS-1 cell growth in a cell viability assay, IC50=19.6635 μM | ||||
| human AU565 cell | Growth inhibition assay | Inhibition of human AU565 cell growth in a cell viability assay, IC50=19.7402 μM | ||||
| human NCI-H2087 cell | Growth inhibition assay | Inhibition of human NCI-H2087 cell growth in a cell viability assay, IC50=21.0591 μM | ||||
| human RVH-421 cell | Growth inhibition assay | Inhibition of human RVH-421 cell growth in a cell viability assay, IC50=21.5795 μM | ||||
| human SK-CO-1 cell | Growth inhibition assay | Inhibition of human SK-CO-1 cell growth in a cell viability assay, IC50=21.8872 μM | ||||
| human KU-19-19 cell | Growth inhibition assay | Inhibition of human KU-19-19 cell growth in a cell viability assay, IC50=22.0242 μM | ||||
| human NB6 cell | Growth inhibition assay | Inhibition of human NB6 cell growth in a cell viability assay, IC50=22.9135 μM | ||||
| human RO82-W-1 cell | Growth inhibition assay | Inhibition of human RO82-W-1 cell growth in a cell viability assay, IC50=23.1318 μM | ||||
| human LNCAP cells | Cytotoxic assay | 2 days | Cytotoxicity against human LNCAP cells assessed as cell viability after 2 days by cell counting method, IC50=23.79 μM | |||
| human CTB-1 cell | Growth inhibition assay | Inhibition of human CTB-1 cell growth in a cell viability assay, IC50=24.5536 μM | ||||
| human SW48 cell | Growth inhibition assay | Inhibition of human SW48 cell growth in a cell viability assay, IC50=24.6546 μM | ||||
| human TCCSUP cell | Growth inhibition assay | Inhibition of human TCCSUP cell growth in a cell viability assay, IC50=24.7232 μM | ||||
| human DK-MG cell | Growth inhibition assay | Inhibition of human DK-MG cell growth in a cell viability assay, IC50=24.8917 μM | ||||
| human ST486 cell | Growth inhibition assay | Inhibition of human ST486 cell growth in a cell viability assay, IC50=25.7464 μM | ||||
| human H4 cell | Growth inhibition assay | Inhibition of human H4 cell growth in a cell viability assay, IC50=26.9458 μM | ||||
| human SBC-1 cell | Growth inhibition assay | Inhibition of human SBC-1 cell growth in a cell viability assay, IC50=28.3507 μM | ||||
| human CAS-1 cell | Growth inhibition assay | Inhibition of human CAS-1 cell growth in a cell viability assay, IC50=28.6294 μM | ||||
| human OAW-42 cell | Growth inhibition assay | Inhibition of human OAW-42 cell growth in a cell viability assay, IC50=28.7195 μM | ||||
| human HCC1954 cell | Growth inhibition assay | Inhibition of human HCC1954 cell growth in a cell viability assay, IC50=28.7525 μM | ||||
| human MDA-MB-453 cell | Growth inhibition assay | Inhibition of human MDA-MB-453 cell growth in a cell viability assay, IC50=29.907 μM | ||||
| human MCF7 cell | Growth inhibition assay | Inhibition of human MCF7 cell growth in a cell viability assay, IC50=39.301 μM | ||||
| human PC3 cells | Function assay | 100 μM | 48 h | Inhibition of actin based pseudopodia formation in androgen-dependent human PC3 cells at 100 uM after 48 hrs by DAPI staining based fluorescence microscopy assay | ||
| human PC3 cells | Function assay | 0.1-1 μM | Agonist activity at androgen receptor W741C mutant expressed in human PC3 cells assessed as stimulation of receptor transactivation at 0.1 to 1 uM by luciferase reporter gene assay | |||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 430.37 | Formule | C18H14F4N2O4S |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 90357-06-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | ICI-176334 | Smiles | CC(CS(=O)(=O)C1=CC=C(C=C1)F)(C(=O)NC2=CC(=C(C=C2)C#N)C(F)(F)F)O | ||
Solubilité
|
In vitro |
DMSO
: 86 mg/mL
(199.82 mM)
Ethanol : 7 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Androgen Receptor
(LNCaP/AR(cs) cells) 0.16 μM
|
|---|---|
| In vitro |
Bicalutamide subit un passage d'antagoniste à agoniste, stimulant l'activité AR. Ce traitement composé de cellules LNCaP/AR(cs) en l'absence de l'androgène synthétique R1881 entraîne une expression génique altérée, cohérente avec son activité agoniste bien documentée dans le contexte d'une surexpression d'AR. Il induit la prolifération cellulaire de manière dose-dépendante, et n'antagonise que partiellement les effets du R1881. Ce traitement chimique entraîne également une quantité significative d'AR nucléaire, bien que moins importante que celle observée avec le R1881. Il présente une activité agoniste partielle, comme en témoignent l'induction de la liaison à l'ADN au niveau des gènes cibles de l'AR et l'antagonisme incomplet des effets du R1881. En l'absence de R1881, cet agent active partiellement la transcription médiée par VP16-AR, ce qui indique une liaison de l'AR à l'ADN. Dans les cellules LNCaP/AR-luc avec un construit rapporteur luciférase piloté par AR intégré de manière stable. En présence de R1881, il ne montre qu'un faible antagonisme partiel de la transcription médiée par VP16-AR avec une IC50 de 0,35 μM. Le bicalutamide micromolaire provoque une réduction significative dose-dépendante de la clonogénicité. L'inhibition duale des voies de signalisation de l'AR et de mTOR procure un bénéfice supplémentaire avec la combinaison ridaforolimus-ce composé produisant des effets antiprolifératifs synergiques dans les cellules de cancer de la prostate in vitro par rapport à chaque agent seul.
|
| Essai kinase |
Tests de liaison compétitive sur cellules entières
|
|
Des tests de liaison compétitive sur cellules entières sont effectués dans les lignées LNCaP/AR(codon-switch) (LNCaP/AR(cs)) (qui héberge un mélange d'AR de type sauvage exogène et d'AR mutant endogène (T877A)) et des cellules propagées dans des milieux Iscove's ou RPMI complétés avec 10 % de sérum de veau fœtal, ou pendant le test avec 10 % de sérum de veau fœtal traité au charbon actif et au dextran (CSS). Les cellules sont pré-incubées avec du 18F-FDHT, des concentrations croissantes (1 pM à 1 μM) de ce composé froid sont ajoutées, et le test est effectué pour mesurer l'absorption spécifique du 18F-FDHT (4). Les valeurs d'IC50 sont déterminées à l'aide d'un modèle de liaison à un site avec un ajustement de courbe par moindres carrés et un R2 > 0,99.
|
|
| In vivo |
Le Bicalutamide seul réduit la croissance tumorale de 79 %, à des doses sous-maximales définies. La combinaison ridaforolimus-ce composé présente une activité antitumorale améliorée et puissante, abrogant presque complètement la croissance tumorale. La combinaison est également bien tolérée, comme en témoignent l'absence de changements significatifs du poids corporel au cours du traitement. Les niveaux plasmatiques de PSA sont à nouveau étroitement liés à la croissance tumorale chez les souris traitées par la combinaison.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
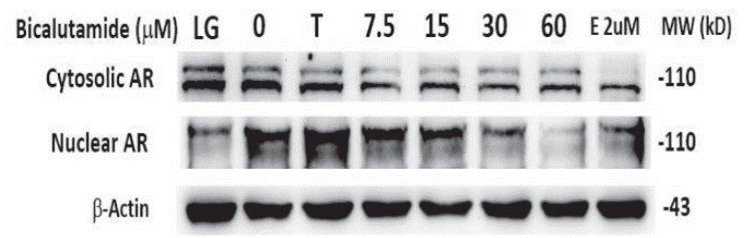
| Western blot | Cytosolic AR / Nuclear AR |
|
30833616 |
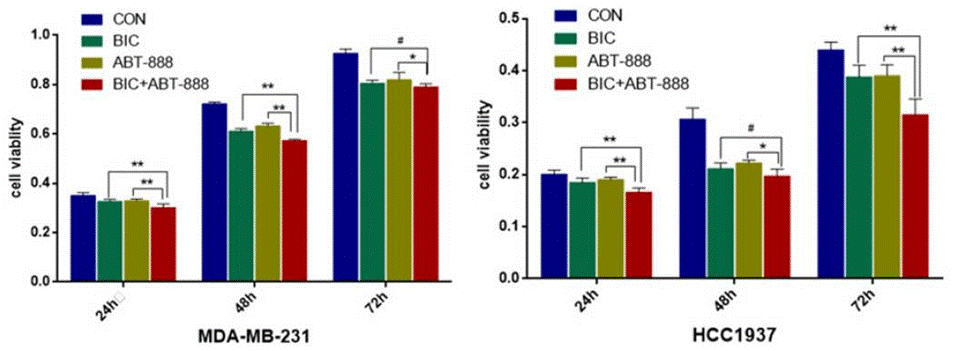
| Growth inhibition assay | Cell viability |
|
27994514 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06222593 | Not yet recruiting | Carcinoma Renal Cell |
State University of New York at Buffalo |
June 1 2024 | Phase 1|Phase 2 |
| NCT04573231 | Recruiting | Breast Cancer|HER2-negative Breast Cancer|Metastatic Breast Cancer |
University of Wisconsin Madison |
May 24 2021 | Phase 2 |
| NCT04443062 | Recruiting | Prostate Cancer |
Radboud University Medical Center|Prostaatkankerstichting|Advanced Accelerator Applications |
July 20 2020 | Phase 2 |
| NCT02910050 | Unknown status | Breast Cancer |
Xu fei|Sun Yat-sen University |
January 2016 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
