pour la recherche uniquement
Gabapentin HCl GABA Receptor agoniste
Réf. CatalogueS1338
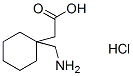
Structure chimique
Poids moléculaire: 207.7
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- Fiche technique
- SDS
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- Fiche technique
- SDS
| Cibles apparentées | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Autre GABA Receptor Inhibiteurs | Dihydromyricetin CGP52432 Oxiracetam Ginkgolide A Pentylenetetrazol 4-Aminobutyric acid (GABA) Emamectin Benzoate Nefiracetam Piracetam Bemegride |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 207.7 | Formule | C9H17NO2.HCl |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 60142-95-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Neurontin HCl | Smiles | C1CCC(CC1)(CC(=O)O)CN.Cl | ||
Solubilité
|
In vitro |
Water : 42 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
GABA receptor
|
|---|---|
| In vitro |
La Gabapentin supprime l'activité de décharge afférente ectopique générée par les nerfs périphériques lésés. La Gabapentin, à des doses allant de 30 à 90 mg/kg, atténue significativement l'allodynie chez les rats atteints de lésions nerveuses. La Gabapentin inhibe de manière dose-dépendante l'activité de décharge ectopique de 15 fibres nerveuses afférentes sciatiques lésées par une action sur la génération d'impulsions. La Gabapentin inhibe l'influx de Ca(2+) voltage-dépendant évoqué par le KCl (30 mM). La Gabapentin inhibe puissamment le courant de pointe des canaux Ca(2+) à cellule entière (I(Ba)) de manière dose-dépendante avec une valeur d'IC(50) estimée à 167 nM. L'inhibition par la Gabapentin est voltage-dépendante, produisant un décalage hyperpolarisant d'environ 7 mV des propriétés courant-tension et réduisant une composante non inactivante du courant à cellule entière activée à des potentiels relativement dépolarisés. La Gabapentin active sélectivement les récepteurs GABAB1a-B2 hétérodimères, mais pas les récepteurs GABAB1b-B2 ou GABAB1c-B2. La Gabapentin active sélectivement les hétérorécepteurs GABAB présynaptiques sur les terminaisons glutamatergiques, mais pas les autorécepteurs GABAB sur les terminaisons GABAergiques. Il a été constaté que la Gabapentin inhibe à la fois la transmission synaptique excitatrice in vitro et la réponse neuronale à la stimulation électrique et mécanique nocive in vivo médiées par l'acide α-amino-3-hydroxy-5-méthyl-4-isoxazolepropionique (AMPA), mais pas celles médiées par les récepteurs N-méthyl-D-asparate (NMDA). La Gabapentin agit comme un antagoniste des récepteurs AMPA dans la moelle épinière de rat pour exercer son effet antinociceptif spinal. La Gabapentin déprime, mais le NMDA améliore, la volée de fibres présynaptiques dans la région CA1 des tranches d'hippocampe de rat. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04613024 | Not yet recruiting | Weight Loss|Pain Postoperative |
Stanford University |
July 1 2023 | Early Phase 1 |
| NCT05276089 | Not yet recruiting | Opioid Use |
Dr Yu Fu|Teesside University|NIHR Applied Research Collaboration for North East and North Cumbria|North East Academic Health Science Network|Newcastle University |
February 1 2023 | Not Applicable |
| NCT05609682 | Recruiting | Post Operative Pain |
University of Oklahoma |
November 29 2022 | Early Phase 1 |
| NCT05750875 | Completed | Pruritus|Uremia|Chronic Kidney Diseases |
King Edward Medical University |
May 1 2022 | Phase 4 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
