pour la recherche uniquement
Rofecoxib COX inhibiteur
Réf. CatalogueS3043
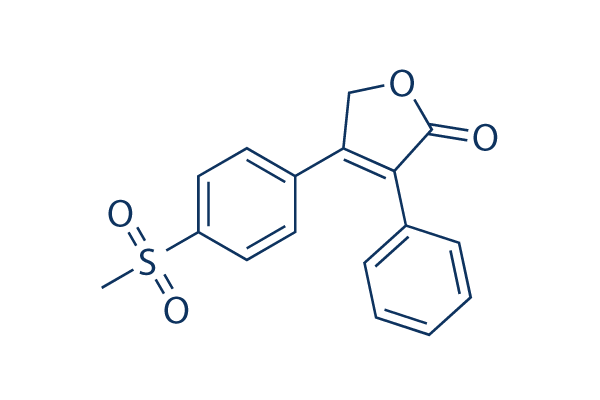
Structure chimique
Poids moléculaire: 314.36
Contrôle Qualité
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| J774 | Function assay | In vitro inhibitory activity against Prostaglandin G/H synthase 2 in murine J774 cells, IC50=0.012 μM | ||||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 314.36 | Formule | C17H14O4S |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 162011-90-7 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | MK-0966 | Smiles | CS(=O)(=O)C1=CC=C(C=C1)C2=C(C(=O)OC2)C3=CC=CC=C3 | ||
Solubilité
|
In vitro |
DMSO
: 63 mg/mL
(200.4 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
COX-2
18 nM
|
|---|---|
| In vitro |
Le Rofecoxib inhibe la production de PGE2 dépendante de la COX-2 dans les cellules d'ostéosarcome humain avec une IC50 de 26 nM. Ce composé est un inhibiteur temps-dépendant de la COX-2 humaine recombinante purifiée avec une IC50 de 0,34 μM. Il provoque l'inhibition de la COX-1 humaine purifiée de manière non dépendante du temps. Dans un essai sur sang total humain, ce produit chimique inhibe sélectivement la synthèse de PGE2 dérivée de la COX-2, induite par le lipopolysaccharide, avec une valeur IC50 de 0,53 μM, comparée à une valeur IC50 de 18,8 μM pour l'inhibition de la synthèse de thromboxane B2 dérivée de la COX-1 après coagulation sanguine. Il inhibe modérément la O-dééthylation de la phénacétine avec une IC50 de 23 μM. Et une préincubation de 30 minutes avec des microsomes et du NADPH augmente considérablement l'effet inhibiteur de ce composé avec une IC50 de 4,2 μM. L'inactivation du CYP1A2 par le rofécoxib nécessite du NADPH et est caractérisée par un K i de 4,8 μM.
|
| Essai kinase |
Essais biochimiques et pharmacologiques in vitro
|
|
études d'inhibition avec les COX-1 et COX-2 humaines recombinantes
|
|
| In vivo |
Des préparations microsomales de COX-1 et COX-2 humaines recombinantes sont préparées à partir d'un système d'expression de cellules vaccinia virus-COS-7. Les COX-1 et COX-2 humaines recombinantes sont exprimées dans des cellules de baculovirus-Sf9, et les enzymes sont purifiées. L'activité enzymatique est surveillée en continu soit par un test de fluorescence mesurant l'apparition de la forme oxydée de l'acide homovanillique, cosubstrat réducteur, soit par la consommation d'oxygène. L'essai HPLC pour l'évaluation de l'inhibition de la COX-1 purifiée par ce composé avec une concentration de substrat d'acide arachidonique de 0,1 μM, la détermination de la stoechiométrie du complexe entre COX-2 et ce produit chimique, la constante de vitesse de dissociation du complexe enzyme-inhibiteur par récupération de l'activité enzymatique, et la récupération de ce composé intact de ce complexe sont tous effectués comme décrit précédemment. Le système de solvant pour l'analyse HPLC de ce produit chimique est 15:85 MeOH/phosphate de potassium aqueux (1 g/litre), avec élution par un gradient linéaire de 15 à 75 % de MeOH sur 25 minutes avec détection à 275 nm sur une colonne Novapak C18.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT00637988 | Completed | Barrett''s Esophagus |
AstraZeneca |
April 2002 | Phase 4 |
| NCT00038389 | Terminated | Glioma|Brain Neoplasms |
M.D. Anderson Cancer Center |
October 2001 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
