pour la recherche uniquement
Zanamivir Neuraminidase inhibiteur
Réf. CatalogueS3007
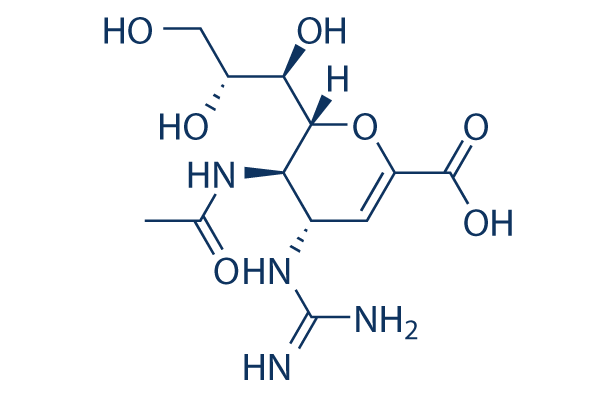
Structure chimique
Poids moléculaire: 332.31
Contrôle Qualité
| Cibles apparentées | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite Reverse Transcriptase HIV |
|---|---|
| Autre Neuraminidase Inhibiteurs | Laninamivir Octanoate Laninamivir |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 332.31 | Formule | C12H20N4O7 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 139110-80-8 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | GG167,GR 121167X | Smiles | CC(=O)NC1C(C=C(OC1C(C(CO)O)O)C(=O)O)N=C(N)N | ||
Solubilité
|
In vitro |
Water : 25 mg/mL
DMSO
: 2 mg/mL
(6.01 mM)
Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
neuraminidase
|
|---|---|
| In vitro |
Zanamivir, un nouvel inhibiteur de la neuraminidase, est efficace pour diminuer la réplication du virus in vitro. Ce composé entraîne une sensibilité réduite chez la variante Influenza A/H1N1 His274Asn, ainsi que His274Gly, His274Ser et His274Gln. Il bloque l'Influenza neuraminidase et empêche le clivage des résidus d'acide sialique, interférant ainsi avec la dispersion du virus progénique dans les sécrétions muqueuses et réduisant l'infectiosité virale. Cet agent prévient l'hémadsorption et la fusion des cellules infectées de manière persistante avec les cellules non infectées. Il réduit le nombre (mais pas la surface) des plaques si présent uniquement pendant la période d'adsorption et réduit la surface des plaques (mais pas le nombre) si ajouté seulement après la période d'adsorption de 90 minutes dans les tests de plaques. Le composé réduit également la surface des plaques formées par une variante déficiente en neuraminidase, confirmant que son interférence avec la fusion cellule-cellule est sans rapport avec l'inhibition de l'activité de la neuraminidase. Il n'a aucun effet sur l'hémadsorption mais inhibe la fusion des globules rouges HA2b, comme en témoignent le mélange lipidique et le mélange de contenu. |
| In vivo |
Zanamivir réduit les titres pulmonaires du virus et diminue la morbidité et la mortalité dans un modèle de défi létal chez la souris. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04597437 | Recruiting | Dengue Fever |
George Washington University|Naval Medical Research Center|Clinica de la Costa|Global Disease Research |
March 15 2024 | Early Phase 1 |
| NCT04494412 | Recruiting | Influenza Human|Arthralgia |
GlaxoSmithKline |
November 21 2022 | Phase 2 |
| NCT02377401 | Completed | Influenza Human |
GlaxoSmithKline |
April 28 2015 | Phase 1 |
| NCT01527110 | Completed | Influenza Human |
GlaxoSmithKline |
January 1 2012 | Phase 3 |
| NCT01353768 | Completed | Infections Respiratory Tract |
GlaxoSmithKline |
July 2011 | -- |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
