pour la recherche uniquement
Enzastaurin PKC inhibiteur
Réf. CatalogueS1055
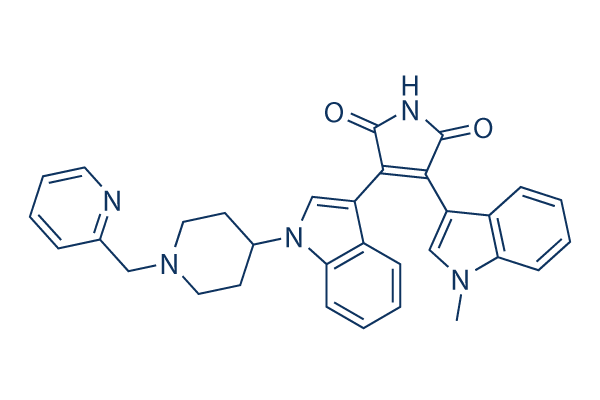
Structure chimique
Poids moléculaire: 515.61
Contrôle Qualité
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| A673 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| Saos-2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| LAN-5 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for LAN-5 cells | 29435139 | |||
| OHS-50 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| MG 63 (6-TG R) | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for MG 63 (6-TG R) cells | 29435139 | |||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 515.61 | Formule | C32H29N5O2 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 170364-57-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | LY317615 | Smiles | CN1C=C(C2=CC=CC=C21)C3=C(C(=O)NC3=O)C4=CN(C5=CC=CC=C54)C6CCN(CC6)CC7=CC=CC=N7 | ||
Solubilité
|
In vitro |
DMSO
: 14 mg/mL
(27.15 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
PKCβ
(Cell-free assay) 6 nM
PKCα
(Cell-free assay) 39 nM
PKCγ
(Cell-free assay) 83 nM
PKCε
(Cell-free assay) 110 nM
|
|---|---|
| In vitro |
L'application d'Enzastaurin entraîne une inhibition marquée et dose-dépendante de la croissance dans toutes les lignées cellulaires de myélome multiple (MM) étudiées, y compris MM.1S, MM.1R, RPMI 8226 (RPMI), RPMI-Dox40 (Dox40), NCI-H929, KMS-11, OPM-2 et U266, avec des IC50 de 0,6 à 1,6 μM. Ce composé a un impact direct sur les cellules tumorales humaines, induisant l'apoptose et supprimant la prolifération dans les cellules tumorales cultivées. Il supprime également la phosphorylation de la GSK3βser9, de la protéine ribosomale S6S240/244 et de l'AKTThr308, sans effet direct sur la phosphorylation du VEGFR. Ce produit chimique augmente l'apoptose dans les lymphocytes malins du CTCL. Lorsqu'il est combiné à des inhibiteurs de GSK3, il a démontré une amélioration des niveaux de cytotoxicité. Le traitement combiné de ce composé et de l'inhibiteur de GSK3 AR-A014418 a entraîné une augmentation des niveaux de protéine totale β-caténine et de la transcription médiatisée par la β-caténine. Le blocage de la transcription médiatisée par la β-caténine ou le silençage par petit ARN en épingle à cheveux (shRNA) de la β-caténine a induit les mêmes effets cytotoxiques que ceux du composé combiné à l'AR-A014418. De plus, le traitement avec le composé et l'AR-A014418 a diminué les niveaux d'ARNm et l'expression de surface de CD44. |
| Essai kinase |
Tests d'inhibition de kinases
|
|
L'inhibition de l'activité de la PKCβII, PKCα, PKCε ou PKCγ par Enzastaurin est déterminée en utilisant un format de test sur plaque filtrante mesurant l'incorporation de 33P dans le substrat protéique basique de la myéline. Les réactions sont réalisées dans des volumes de réaction de 100 μL dans des plaques de polystyrène à 96 puits avec les conditions finales suivantes : 90 mM HEPES (pH 7,5), 0,001 % Triton X-100, 4 % DMSO, 5 mM MgCl2, 100 μM CaCl2, 0,1 mg/mL de phosphatidylsérine, 5 μg/mL de diacétyl glycérol, 30 μM ATP, 0,005 μCi/μL 33ATP, 0,25 mg/mL de protéine basique de la myéline, des dilutions en série de ce composé (1-2 000 nM) et des enzymes humaines recombinantes PKCβII, PKCα, PKCε ou PKCγ (390, 169, 719 ou 128 pM, respectivement). Les réactions sont initiées par l'ajout de l'enzyme et incubées à température ambiante pendant 60 minutes. Elles sont ensuite éteintes avec 10 % H3PO4, transférées dans des plaques filtrantes à 96 puits en phosphocellulose anionique multiscreen, incubées pendant 30 à 90 minutes, filtrées et lavées avec 4 volumes de 0,5 % H3PO4 sur un collecteur à vide. Un cocktail de scintillation est ajouté et les plaques sont lues sur un compteur à scintillation Microbeta. Les valeurs d'IC50 sont déterminées en ajustant une équation logistique à trois variables aux données de dose-réponse en 10 points à l'aide d'ActivityBase 4.0.
|
|
| In vivo |
Le traitement des xénogreffes avec Enzastaurin et des radiations a produit des réductions plus importantes de la densité des microvaisseaux que chaque traitement seul. La diminution de la densité des microvaisseaux correspondait à un retard de la croissance tumorale. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | p27 / Cyclin D1 / Bcl-2 / Survivin p-ERK / ERK / p-AKT / AKT PKCα / PKCβ / PKCδ / PKCε / PKCθ / p-PKCε / p-PKCθ p-eIF2a / eIF2a / p-ATF2 / ATF2 / CHOP / p21 / ATF6 / IRE1α |
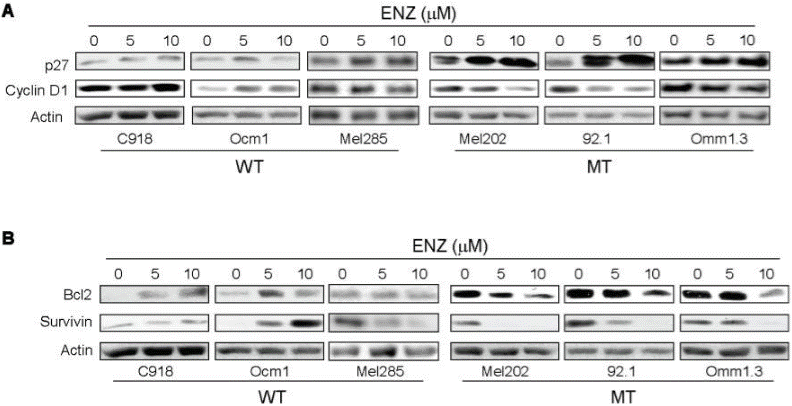
|
22253748 |
| Growth inhibition assay | Cell viability |
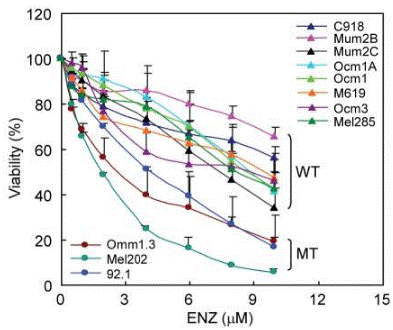
|
22253748 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03263026 | Completed | Diffuse Large B-Cell Lymphoma |
Denovo Biopharma LLC |
March 20 2018 | Phase 3 |
| NCT01432951 | Completed | Solid Tumor|Lymphoma Malignant |
Eli Lilly and Company |
November 2011 | Phase 1 |
| NCT01388335 | Completed | Solid Tumor|Lymphoma Malignant |
Eli Lilly and Company |
August 2011 | Phase 1 |
| NCT00744991 | Completed | Cutaneous T-Cell Lymphoma |
Eli Lilly and Company |
September 2008 | Phase 2 |
| NCT00709995 | Completed | Metastatic Renal Cell Carcinoma |
Eli Lilly and Company |
June 30 2008 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
