pour la recherche uniquement
Ranitidine Hydrochloride Histamine Receptor antagoniste
Réf. CatalogueS1801
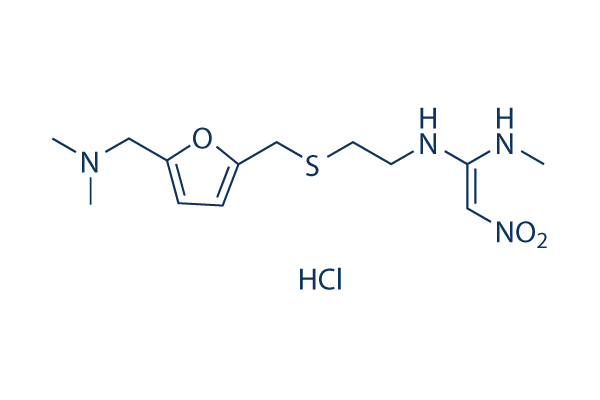
Structure chimique
Poids moléculaire: 350.86
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- HPLC
- SDS
- Fiche technique
| Cibles apparentées | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Autre Histamine Receptor Inhibiteurs | GSK2879552 Dihydrochloride JNJ-7777120 Ebastine Ciproxifan Maleate Mianserin HCl Astemizole Lafutidine Mizolastine Rupatadine Fumarate Betahistine 2HCl |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 350.86 | Formule | C13H22N4O3S.HCl |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 66357-59-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | AH19065 | Smiles | CNC(=C[N+](=O)[O-])NCCSCC1=CC=C(O1)CN(C)C.Cl | ||
Solubilité
|
In vitro |
DMSO
: 70 mg/mL
(199.5 mM)
Water : 70 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Histamine H2 receptor
|
|---|---|
| In vitro |
Ranitidine sensibilise les hépatocytes à la destruction par les produits cytotoxiques des neutrophiles activés, tandis que la famotidine n'a pas cette capacité. Ranitidine inhibe la production du facteur de nécrose tumorale alpha (TNF-alpha) dans les monocytes stimulés par le lipopolysaccharide in vitro. Ranitidine réduit la Kel de la morphine de manière dose-dépendante avec un effet maximal de 50 %, et augmente la concentration relative de morphine-6-glucuronide par rapport à la morphine-3-glucuronide dans les hépatocytes isolés de cobaye. Ranitidine diminue progressivement le rapport morphine-3-glucuronide/morphine-6-glucuronide jusqu'à 21 %.
|
| In vivo |
Ranitidine entraîne des lésions hépatiques, comme en témoigne l'augmentation des activités sériques de l'alanine aminotransférase, de l'aspartate aminotransférase et de la gamma-glutamyl transférase dans les 6 heures suivant l'administration de Ranitidine chez le rat. Ranitidine inhibe l'augmentation des niveaux tissulaires hépatiques de TNF-alpha, du chimiotactant des neutrophiles induit par les cytokines, et l'accumulation hépatique de neutrophiles chez le rat, induite par l'ischémie/reperfusion hépatique. Le co-traitement par Ranitidine améliore la coagulation induite par le LPS avant la lésion hépatique, et les anticoagulants réduisent les lésions hépatiques chez les rats traités par LPS/RAN. Les rats traités par Ranitidine/LPS entraînent la formation de caillots de fibrine dans les sinusoïdes hépatiques, et la prévention du dépôt de fibrine est associée à une réduction des lésions hépatocellulaires. Le co-traitement par Ranitidine améliore l'augmentation du TNF induite par le LPS avant l'apparition des lésions hépatocellulaires chez le rat. Ranitidine présente des effets anxiolytiques dans le labyrinthe en croix élevé, comme l'indique une augmentation du temps passé dans les bras ouverts, davantage de balayage des bras ouverts et davantage d'excursions terminales chez les rats.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05399927 | Completed | Music Therapy|Cardiovascular Diseases|Critical Care|Emergencies |
Universidad Miguel Hernandez de Elche |
July 2015 | Not Applicable |
| NCT01539655 | Completed | Medullary Thyroid Cancer |
Sanofi |
February 2012 | Phase 1 |
| NCT01017198 | Completed | Advanced Solid Tumors |
Biogen |
November 2009 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
