pour la recherche uniquement
Betahistine 2HCl Histamine Receptor inhibiteur
Réf. CatalogueS3176
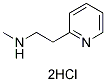
Structure chimique
Poids moléculaire: 209.12
Contrôle Qualité
| Cibles apparentées | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Autre Histamine Receptor Inhibiteurs | GSK2879552 Dihydrochloride JNJ-7777120 Ebastine Ciproxifan Maleate Mianserin HCl Astemizole Lafutidine Mizolastine Rupatadine Fumarate Levodropropizine |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 209.12 | Formule | C8H12N2.2HCl |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 5579-84-0 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | PT-9 | Smiles | CNCCC1=CC=CC=N1.Cl.Cl | ||
Solubilité
|
In vitro |
DMSO
: 38 mg/mL
(181.71 mM)
Water : 38 mg/mL Ethanol : 38 mg/mL |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Histamine H3 receptor
1.9 μM
|
|---|---|
| In vitro |
La Betahistine augmente progressivement la formation de l'AMPc avec un effet maximal, observé jusqu'à 10 nM, dans les cellules CHO(H3R) incubées avec 3 μM de forskoline. En revanche, à des concentrations supérieures à 10 nM, la Betahistine inhibe progressivement la formation de l'AMPc dans les cellules CHO(H3R) incubées avec 3 μM de forskoline. La Betahistine réduit progressivement la libération d'acide [3H]arachidonique évoquée par l'A23187 (EC50=0,1 nM) avec un effet maximal, observé jusqu'à 30 nM, de libération d'acide [3H]arachidonique évoquée par l'A23187 à partir des cellules CHO(H3R). La Betahistine a progressivement augmenté la libération d'acide [3H]arachidonique évoquée par l'A23187 à partir des cellules CHO(H3R) à des concentrations supérieures à 30 nM.
|
| In vivo |
La Betahistine (< 30 mg/kg) augmente les niveaux de t-MeHA de manière dose-dépendante avec une ED50 de 2 mg/kg et un effet maximal d'environ 35 % atteint à 30 mg/kg dans le cerveau de souris. La Betahistine (16 mg deux fois par jour pendant 3 mois) a un effet significatif sur la fréquence, l'intensité et la durée des crises de vertige, les symptômes associés et la qualité de vie sont également significativement améliorés chez les patients atteints de la maladie de Menière. Le dichlorhydrate de Betahistine (16 mg trois fois par jour et 48 mg trois fois par jour) montre que le nombre de crises par mois a diminué avec le temps pour les deux doses dans la maladie de Menière. Le traitement à la Betahistine (50 mg/kg) induit des changements symétriques avec une régulation positive de l'ARNm de l'histidine décarboxylase dans le noyau tuberomammillaire et une réduction du marquage par la [3H]N-alpha-méthylhistamine à la fois dans le noyau tuberomammillaire, le complexe des noyaux vestibulaires et les noyaux de l'olive inférieure dans des coupes de cerveau de chats.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT00852956 | Completed | Healthy |
OBEcure Ltd. |
February 2009 | Phase 1 |
| NCT00585585 | Terminated | Recurrent Major Depressive Disorder With Atypical Features |
University of Cincinnati |
July 2007 | Phase 2 |
| NCT00459992 | Completed | Obesity|Overweight|Overnutrition |
Eunice Kennedy Shriver National Institute of Child Health and Human Development (NICHD)|National Institutes of Health Clinical Center (CC) |
April 10 2007 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
