pour la recherche uniquement
Enalaprilat Dihydrate RAAS inhibiteur
Réf. CatalogueS1657
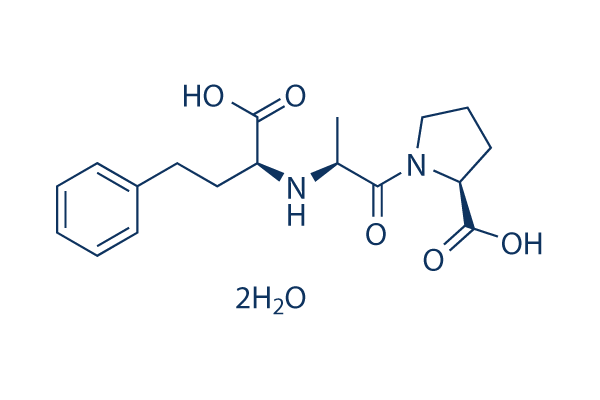
Structure chimique
Poids moléculaire: 348.4
Contrôle Qualité
| Cibles apparentées | Adrenergic Receptor Estrogen/progestogen Receptor GPR Androgen Receptor Glucocorticoid Receptor ACE Progesterone Receptor Opioid Receptor PGES THR |
|---|---|
| Autre RAAS Inhibiteurs | Temocapril HCl Imidapril HCl VTP-27999 TFA Temocapril Zofenopril calcium Delapril Hydrochloride |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 348.4 | Formule | C18H24N2O5.2H2O |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 84680-54-6 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | MK-422 Dihydrate | Smiles | CC(C(=O)N1CCCC1C(=O)O)NC(CCC2=CC=CC=C2)C(=O)O.O.O | ||
Solubilité
|
In vitro |
DMSO
: 70 mg/mL
(200.91 mM)
Water : 5 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Caractéristiques |
The 1st dicarboxylate-containing ACE inhibitor developed to overcome captopril limitations.
|
|---|---|
| Targets/IC50/Ki |
ACE
1.94 nM
|
| In vitro |
Enalaprilat a une forte affinité pour l'ECA endothéliale humaine avec une IC50 de 1,94 nM dans un essai de liaison in vitro en déplaçant une concentration saturante de [125I]351A, un analogue radiomarqué du lisinopril, des sites de liaison de l'ECA, et montre un rapport de sélectivité bradykinine/angiotensine I de 1,00 calculé à partir d'expériences de double déplacement. Enalaprilat a un fort effet inhibiteur sur l'activité de conversion de l'Aβ42 en Aβ40 trouvée dans le N-domaine de l'ECA, présentant une IC50 (0,003~0,01 μM) 10 fois inférieure à celle du captopril (0,03~0,1 μM). Enalaprilat (100 nM) bloque la protéine kinase C epsilon en activant directement le récepteur B1 de la bradykinine au niveau du site de liaison canonique du Zn2+, entraînant une production prolongée d'oxyde nitrique (NO) dans les cellules endothéliales microvasculaires pulmonaires humaines traitées aux cytokines. Enalaprilat atténue la croissance des fibroblastes cardiaques de rats nouveau-nés induite par l'IGF-I (réduction de 30 %) de manière concentration-dépendante, avec une IC50 de 90 mM.
|
| Essai kinase |
Essai de liaison par déplacement simple
|
|
L'essai de liaison est basé sur le déplacement compétitif du [125I]351A par Enalaprilat effectué sur des cellules endothéliales entières. Les HUVEC subconfluentes dans des plaques à 6 puits sont rincées avec 2 mL de tampon de liaison (140 mM NaCl, 2,7 mM KCl, 1,8 mM CaCl2, 1,03 mM MgCl2, 0,42 mM NaH2PO4, 10 mM HEPES, 2 mM pyruvate de sodium et 5 mM glucose, pH 7,4), et le milieu de culture est remplacé par 2,5 mL de tampon de liaison frais contenant 5 % de sérum de veau fœtal (SVF). L'Enalaprilat (2,5-12,5 μL, 0,1-50 nM) ou des volumes équivalents de diluant sont ajoutés au tampon de liaison. Une quantité saturante de [125I]351A (10 μL, typiquement 106 cpm) est ensuite ajoutée à chaque échantillon et les plaques sont incubées à 37 °C pendant 2 heures dans un bain thermostatique. Les cellules sont ensuite rincées deux fois avec 1,5 mL de tampon de liaison. Enfin, les cellules sont extraites avec 0,5 mL de NaOH 1 N, incubées pendant 5 minutes, et la radioactivité est comptée avec un compteur gamma. Le rapport du [125I]351A spécifique lié à l'activité totale liée (B/B0) est calculé, et la puissance inhibitrice d'Enalaprilat est exprimée comme la concentration d'inhibiteurs de l'ECA capables de déplacer 50 % du radioligand lié, c'est-à-dire l'IC50.
|
|
| In vivo |
Enalaprilat présente des caractéristiques d'ionisation défavorables pour permettre une puissance suffisante pour l'administration orale, ainsi Enalaprilat n'est adapté qu'à l'administration intraveineuse, ce qui est surmonté par l'estérification avec de l'éthanol pour produire Enalapril. L'administration d'Enalaprilat induit une réduction significative de la PAM à 70 minutes par rapport au groupe placebo lors d'un choc hémorragique chez le rat, et entraîne une réduction de 50 % du DC, une tendance générale à l'extravasation d'EB qui est significative dans le rein et les poumons, et une augmentation significative de l'extravasation d'EB iléale (53 %). Enalaprilat n'a pas d'effet sur les cœurs non hypertrophiés, mais atténue significativement l'augmentation plus importante de la pression télédiastolique ventriculaire gauche dans les cœurs hypertrophiés par rapport à l'absence de médicament.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03051282 | Active not recruiting | Healthy Volunteers |
University of Michigan |
April 1 2017 | Phase 4 |
| NCT02654678 | Unknown status | Heart Failure|Dilated Cardiomyopathy|Congenital Heart Disease |
Ethicare GmbH |
March 2016 | Phase 2|Phase 3 |
| NCT02652728 | Unknown status | Heart Failure|Dilated Cardiomyopathy |
Ethicare GmbH |
January 2016 | Phase 2|Phase 3 |
| NCT02652741 | Unknown status | Heart Failure|Congenital Heart Disease |
Ethicare GmbH |
January 2016 | Phase 2|Phase 3 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
