pour la recherche uniquement
Ivacaftor (VX-770) Potentiateur de CFTR
Réf. CatalogueS1144
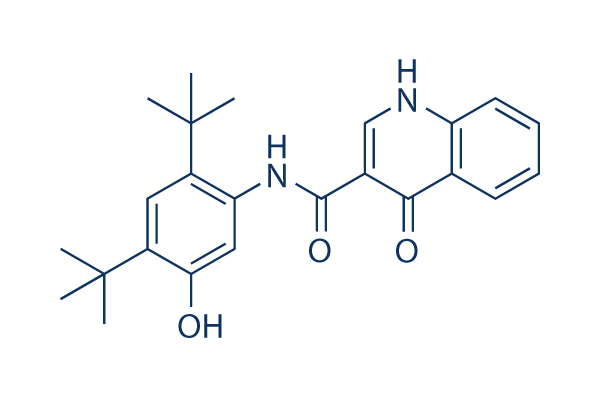
Structure chimique
Poids moléculaire: 392.49
Contrôle Qualité
Produits souvent utilisés avec Ivacaftor (VX-770)
| Cibles apparentées | CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase GluR |
|---|---|
| Autre CFTR Inhibiteurs | Vanzacaftor (VX-121) VX-561(CTP-656) GLPG1837 FDL169 Galicaftor (ABBV-2222) GlyH-101 IOWH032 PPQ-102 KM11060 Steviol (Hydroxydehydrostevic acid) |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| HBE | Function Assay | 10 μM | 10 min | augments CFTR-dependent ion transport | 24106801 | |
| CFBE41o- | Function Assay | 10 µM | induces robust increases in anion transport | 22768130 | ||
| HBE | Function Assay | 10 µM | augments CFTR-dependent anion transport activity | 22768130 | ||
| HBE | Function Assay | 10 µM | 24 h | induces a modest but significant increase in ASL depth | 22768130 | |
| HBE | Function Assay | 10 µM | potentiates CFTR-dependent Isc, regardless of prior administration of CSE | 22768130 | ||
| HBE | Function Assay | 10 µM | partially restores depletion of ASL depth in CSE treated monolayers | 22768130 | ||
| mouse NIH-3T3 cells | Function assay | 30 mins | Potentiation of human CFTR F508del mutant expressed in mouse NIH-3T3 cells after 30 mins by fluorescent voltage sensing optical assay, EC50 = 0.003 μM. | 25441013 | ||
| human bronchial epithelial cells | Function assay | Potentiation of human CFTR F508del/G551D mutant in human bronchial epithelial cells by Ussing chambers recording technique, EC50 = 0.022 μM. | 25441013 | |||
| human CFBE41o cells | Function assay | 10 mins | Potentiation of CFTR F508del mutant (unknown origin) expressed in human CFBE41o cells incubated for 10 mins in presence of forskolin measured for 7 secs by YFP halide assay, EC50 = 0.126 μM. | 29148763 | ||
| human bronchial epithelial cells | Function assay | Potentiation of human CFTR F508del mutant in human bronchial epithelial cells by Ussing chambers recording technique, EC50 = 0.236 μM. | 25441013 | |||
| HEK293 cells | Function assay | 10 mins | Potentiation of CFTR G551D mutant (unknown origin) expressed in HEK293 cells incubated for 10 mins in presence of forskolin measured for 2 mins by YFP halide assay, EC50 = 1.3 μM. | 29148763 | ||
| NRK-49F cells | Function assay | Inhibition of TGF-beta1-induced total collagen accumulation in rat NRK-49F cells, IC50 = 4 μM. | 25467157 | |||
| DAOY cells | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for DAOY cells | 29435139 | |||
| NB-EBc1 cells | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for NB-EBc1 cells | 29435139 | |||
| MG 63 (6-TG R) cells | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for MG 63 (6-TG R) cells | 29435139 | |||
| RD cells | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for RD cells | 29435139 | |||
| SK-N-MC cells | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for SK-N-MC cells | 29435139 | |||
| Saos-2 cells | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for Saos-2 cells | 29435139 | |||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 392.49 | Formule | C24H28N2O3 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 873054-44-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | VX-770 | Smiles | CC(C)(C)C1=CC(=C(C=C1NC(=O)C2=CNC3=CC=CC=C3C2=O)O)C(C)(C)C | ||
Solubilité
|
In vitro |
DMSO
: 79 mg/mL
(201.27 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Caractéristiques |
The first potent and orally available CFTR potentiator to enter human clinical trials.
|
|---|---|
| Targets/IC50/Ki |
F508del-CFTR
(Fisher rat thyroid cells) 25 nM(EC50)
G551D-CFTR
(Fisher rat thyroid cells) 100 nM(EC50)
|
| In vitro |
L'Ivacaftor (VX-770) (10 μM) augmente significativement la sécrétion de Cl- stimulée par la forskoline (IT) d'environ 4 fois avec une EC50 de 100 nM dans les cellules thyroïdiennes de rat Fisher (FRT) recombinantes exprimant la mutation de gating G551D de CFTR, et d'environ 6 fois avec une EC50 de 25 nM dans les cellules recombinantes exprimant la mutation de traitement F508del corrigée en température de CFTR. Conformément aux augmentations de l'IT stimulée par la forskoline, ce composé augmente la probabilité d'ouverture (Po) des CFTR G551D, F508del et de type sauvage d'environ 6 fois, 5 fois et 2 fois, respectivement, indiquant qu'il agit directement sur CFTR pour augmenter son activité de gating. Dans les épithéliums bronchiques humains (HBE) de culture primaire atteints de mucoviscidose portant les mutations G551D et F508del de CFTR, l'Ivacaftor augmente puissamment l'IT stimulée par la forskoline d'environ 10 fois, passant de 5 % à un niveau maximal de 48 % de celui mesuré dans les HBE non-mucoviscidosiques, avec une EC50 de 236 nM, démontrant une puissance environ 70 fois supérieure à celle de la génistéine, un potentiateur de CFTR couramment utilisé, qui a une EC50 de 16 μM. Dans les HBE avec CFTR F508del homozygote, il provoque une augmentation significative de l'IT stimulée par la forskoline avec une EC50 de 22 nM, à un degré moindre de 4 % à 16 % des HBE non-mucoviscidosiques par rapport à l'effet dans les HBE G551D/F508del. En raison de la potentialisation de CFTR, ce composé inhibe l'absorption excessive de Na+ et de fluide médiatisée par l'ENaC avec une IC50 de 43 nM, et diminue la réponse, entraînant une augmentation du fluide de surface et de la fréquence de battement ciliaire (CBF) dans les HBE G551D/F508del. |
| Essai kinase |
Enregistrements en chambre d'Ussing
|
|
L'effet d'Ivacaftor (VX-770) sur la sécrétion de Cl- médiatisée par CFTR est caractérisé en mesurant l'IT médiatisée par CFTR dans des chambres utilisant des cellules thyroïdiennes de rat Fisher (FRT) recombinantes exprimant G551D, ou F508del CFTR. Les cellules sont cultivées sur des inserts de culture cellulaire Costar Snapwell maintenus à 37 °C avant l'enregistrement. Les inserts de culture cellulaire sont montés dans une chambre d'Ussing pour enregistrer l'IT en mode de voltage-clamp (Vhold = 0 mV). Pour les cellules FRT, la membrane basolatérale est un gradient de Cl- basolatéral à apical est établi. La solution de bain basolatéral contient 135 mM de NaCl, 1,2 mM de CaCl2, 1,2 mM de MgCl2, 2,4 mM de K2HPO4, 0,6 mM de KHPO4, 10 mM de N-2-hydroxyéthylpipérazine-N
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | PPARγ / pERK NLRP3 Rδf508 |
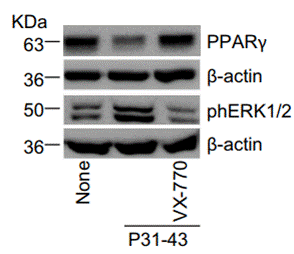
|
30498130 |
| Immunofluorescence | F-actin |
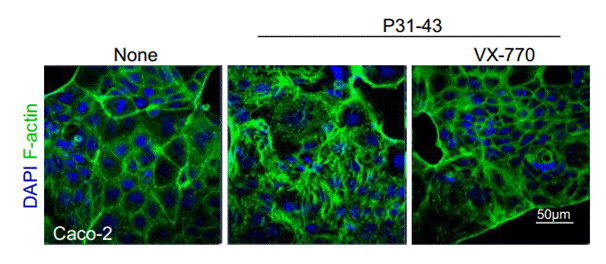
|
30498130 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06331000 | Not yet recruiting | Cystic Fibrosis |
University Hospital Strasbourg France |
March 2024 | -- |
| NCT05519020 | Recruiting | Cystic Fibrosis |
Sheffield Teaching Hospitals NHS Foundation Trust |
July 27 2022 | -- |
| NCT04254705 | Withdrawn | Cystic Fibrosis |
Universitaire Ziekenhuizen KU Leuven|Vertex Pharmaceuticals Incorporated|KU Leuven|University of Lisbon |
March 1 2020 | Not Applicable |
| NCT03085485 | Completed | Chronic Obstructive Pulmonary Disease|Chronic Bronchitis |
University of Alabama at Birmingham|National Heart Lung and Blood Institute (NHLBI)|Vertex Pharmaceuticals Incorporated |
March 16 2017 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
