pour la recherche uniquement
Neferine NF-κB inhibiteur
Réf. CatalogueS5144
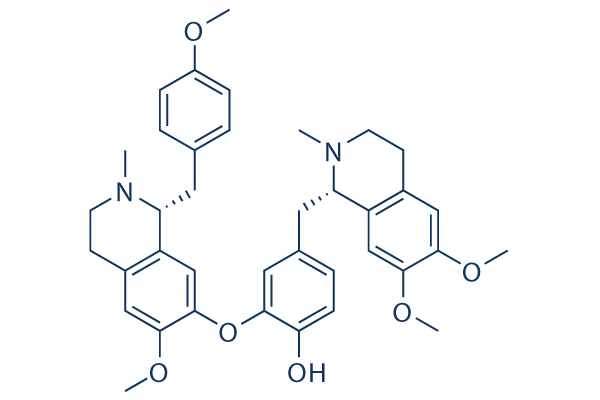
Structure chimique
Poids moléculaire: 624.77
Contrôle Qualité
| Cibles apparentées | HDAC Antioxidant ROS IκB/IKK Nrf2 AP-1 MALT NOD |
|---|---|
| Autre NF-κB Inhibiteurs | DCZ0415 Omaveloxolone (RTA-408) BAY 11-7082 (BAY 11-7821) JSH-23 QNZ (EVP4593) Caffeic Acid Phenethyl Ester SC75741 DHA (Dihydroartemisinin) Withaferin A (WFA) Andrographolide |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 624.77 | Formule | C38H44N2O6 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 2292-16-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | (R)-1,2-Dimethoxyaporphine | Smiles | CN1CCC2=CC(=C(C=C2C1CC3=CC=C(C=C3)OC)OC4=C(C=CC(=C4)CC5C6=CC(=C(C=C6CCN5C)OC)OC)O)OC | ||
Solubilité
|
In vitro |
DMSO
: 100 mg/mL
(160.05 mM)
|
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
NF-κB
|
|---|---|
| In vitro |
La Neferine induit une apoptose dépendante des caspases médiée par les espèces réactives de l'oxygène dans les cellules de cancer du foie et du poumon, inverse la résistance multidrogue dans les cellules de cancer du sein humain (MCF-7/ADM), l'hépatocarcinome humain (HepG2/ADR) et les cellules de carcinome gastrique humain (SGC7901/VCR). Ce composé améliore le potentiel cytotoxique du cisplatine dans les cellules A549 et augmente l'accumulation de Sub-G1 induite par le cisplatine. Il inhibe la migration et l'invasion des cellules de cancer du poumon humain et diminue les activités des enzymes antioxydantes. Ce produit chimique sensibilise les cellules de cancer du poumon au cisplatine et induit l'apoptose par l'arrêt du cycle cellulaire en G1, la production en amont de ROS, l'épuisement du pool d'antioxydants cellulaires, la réduction du potentiel de membrane mitochondriale (ΔΨm) avec une expression accrue de Bax, Bad, Bak, une régulation négative de l'expression de Bcl2, la libération de cytochrome c, de caspase-9 clivée, de caspase-3 clivée et de PARP. |
| In vivo |
La Neferine a un effet antifibrose sur la fibrose hépatique induite par le CCl4 chez la souris, peut-être en partie grâce à la diminution de l'expression du TGF-β1 dans le foie. Les courbes de concentration plasmatique en fonction du temps de ce composé (10, 20 et 50 mg/kg, i.g.) montrent des doubles pics d'absorption avec le premier pic à 10 min et le second pic à 1 h. Les tβ1/2 sont de 15,6 h, 22,9 h et 35,5 h, respectivement pour chacune de ces doses. Ce composé se distribue rapidement dans différents systèmes d'organes, avec les concentrations les plus élevées trouvées dans le foie, suivies par les poumons, les reins et le cœur à des doses de 10 ou 20 mg/kg. À une dose de 50 mg/kg, les concentrations rénales et pulmonaires sont plus élevées que celles des autres. De plus, ce composé est principalement métabolisé dans le foie et partiellement converti par le CYP2D6 en liensinine, isoliensinine, desméthyl-liensinine et desméthyl-isoliensinine. |
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
