pour la recherche uniquement
Ropinirole HCl Dopamine Receptor inhibiteur
Réf. CatalogueS3189
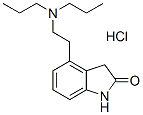
Structure chimique
Poids moléculaire: 296.84
Contrôle Qualité
| Cibles apparentées | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Autre Dopamine Receptor Inhibiteurs | MPTP Hydrochloride Trifluoperazine Trifluoperazine 2HCl Penfluridol Sulpiride Levosulpiride SCH-23390 hydrochloride Domperidone Rotundine Azaperone |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 296.84 | Formule | C16H24N2O.HCl |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 91374-20-8 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | SKF-101468A | Smiles | CCCN(CCC)CCC1=C2CC(=O)NC2=CC=C1.Cl | ||
Solubilité
|
In vitro |
Water : 59 mg/mL
DMSO
: 30 mg/mL
(101.06 mM)
Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
D2 receptor
29 nM(Ki)
|
|---|---|
| In vitro |
Le Ropinirole piège les radicaux libres et supprime la peroxydation lipidique dans le système de réaction Fe2+–H2O2.
|
| In vivo |
Le Ropinirole (50 mg/kg, i.p.) provoque une activité locomotrice spontanée biphasique chez les souris. Le Ropinirole (0,05-1,0 mg/kg SC) inhibe de manière dose-dépendante les dyskinésies induites par le 2-di-n-propylamino-5,6-dihydroxytétraline chez les souris. Le Ropinirole, à des doses de 1 et 10 μg, injecté unilatéralement directement dans le striatum du rat, provoque une asymétrie marquée et un comportement de rotation controlatéraux (loin du côté de l'injection) chez les souris. Le Ropinirole (0,05-1,0 mg/kg SC ou 0,1 mg/kg PO) inverse tous les déficits moteurs et comportementaux induits par le MPTP chez les marmousets. Le Ropinirole (2 mg/kg, i.p.) pendant 7 jours augmente les activités de la GSH, de la catalase et de la SOD dans le striatum et protège les neurones dopaminergiques striataux contre la 6-hydroxydopamine (6-OHDA) chez les souris. Le Ropinirole (0,2 mg/kg, i.p.) améliore l'utilisation du membre antérieur auparavant akinétique et produit un comportement de rotation robuste chez les rats lésés avec une surexpression striatale des D2R et D3R par rapport aux animaux lésés qui ont reçu un vecteur vide. La dose subthérapeutique de Ropinirole ne génère que des effets moteurs modestes chez les rats lésés avec une seule surexpression de D2R ou D3R. Le Ropinirole (1-8 mg t.i.d.) est rapidement et complètement absorbé avec une biodisponibilité orale de 55 %, une clairance de 780 mL/min, une demi-vie d'élimination de 6 heures chez le volontaire sain. Étant donné que la principale voie d'élimination du Ropinirole est le système enzymatique CYP, principalement par le CYP1A2 et également par le CYP3A4, l'inhibition du premier et éventuellement du second peut réduire la clairance de l'agent et entraîner une accumulation de médicament. Le traitement par Ropinirole (0,25 mg-4,0 mg par jour) améliore significativement la capacité des patients à initier le sommeil, la quantité de sommeil de stade 2 et l'adéquation du sommeil par rapport au placebo. Les mouvements périodiques des membres avec éveil par heure diminuent de 7,0 à 2,5 avec le Ropinirole mais augmentent de 4,2 à 6,0 avec le placebo. Les mouvements périodiques des membres pendant l'éveil par heure diminuent de 56,5 à 23,6 avec le Ropinirole mais augmentent de 46,6 à 56,1 avec le placebo.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03708237 | Terminated | Restless Legs Syndrome|End Stage Renal Disease |
University of Alberta |
February 19 2019 | Phase 2 |
| NCT03250117 | Terminated | Parkinson Disease |
Titan Pharmaceuticals |
October 10 2017 | Phase 1|Phase 2 |
| NCT00823836 | Completed | Parkinson Disease |
GlaxoSmithKline |
March 2009 | Phase 3 |
| NCT00530790 | Completed | Restless Legs Syndrome |
GlaxoSmithKline |
August 23 2007 | Phase 2 |
| NCT00460148 | Completed | Parkinson Disease |
GlaxoSmithKline |
April 2007 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
