pour la recherche uniquement
Telbivudine Reverse Transcriptase inhibiteur
Réf. CatalogueS1651
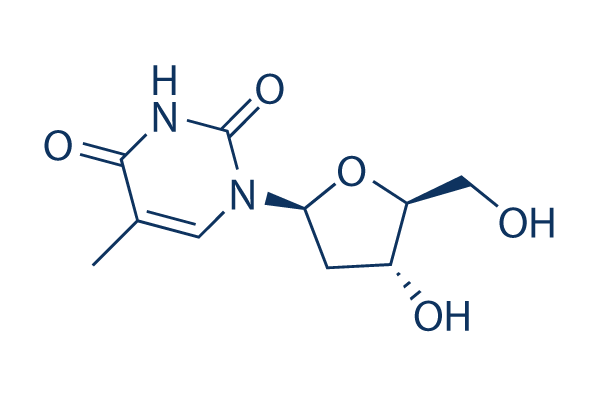
Structure chimique
Poids moléculaire: 242.23
Contrôle Qualité
| Cibles apparentées | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite HIV HCV Protease |
|---|---|
| Autre Reverse Transcriptase Inhibiteurs | Dapivirine (TMC120) Fangchinoline Salicylanilide 3'-Fluoro-3'-deoxythymidine (Alovudine) Ulonivirine Lersivirine (UK-453061) Bifendate 4-Chloro-2-(trifluoroacetyl)aniline hydrochloride |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 242.23 | Formule | C10H14N2O5 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 3424-98-4 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | NV 02B | Smiles | CC1=CN(C(=O)NC1=O)C2CC(C(O2)CO)O | ||
Solubilité
|
In vitro |
DMSO
: 48 mg/mL
(198.15 mM)
Water : 48 mg/mL Ethanol : 2 mg/mL |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
HBV RT
|
|---|---|
| In vitro |
Telbivudine présente une activité antivirale puissante, sélective et spécifique contre le VHB et d'autres virus hepadna. Ce composé est phosphorylé par les thymidine kinases intracellulaires en forme triphosphate active, qui a une demi-vie intracellulaire de 14 heures. Son 5′-triphosphate inhibe l'ADN polymérase du VHB (reverse transcriptase) en compétition avec le substrat naturel, le dTTP. Ce produit chimique augmente de manière significative la production de facteur de nécrose tumorale alpha et d'interleukine-12 dans les macrophages induits par le MHV-3. Il élève significativement les niveaux sériques d'interféron-gamma. Ce traitement améliore la capacité des lymphocytes T à proliférer et à sécréter des cytokines, mais n'affecte pas la cytotoxicité des hépatocytes infectés. Il supprime l'expression du ligand 1 de la mort programmée sur les lymphocytes T. Le composé reste actif comme le montrent les changements de 0,5 (N236T) et 1,0 (A181V et A194T) respectivement. Il n'est pas actif contre les souches de VHB portant les mutations L180M/M204V/I de la lamivudine, mais reste actif contre le mutant simple M204V in vitro, expliquant potentiellement la différence de profils de résistance entre la Telbivudine et la lamivudine. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT02956850 | Completed | Hepatitis B Chronic |
Hoffmann-La Roche |
December 12 2016 | Phase 1 |
| NCT02894554 | Terminated | HBsAg-positive Renal Allograft Recipients |
National Taiwan University Hospital |
July 2014 | Phase 4 |
| NCT01379508 | Completed | Chronic Hepatitis B |
Novartis Pharmaceuticals|Novartis |
March 21 2011 | Phase 4 |
| NCT01163240 | Completed | Liver Diseases|Hepatitis Chronic|Hepatitis Viral Human|Hepatitis|Virus Diseases|Digestive System Diseases|Hepatitis B Chronic|Hepatitis B|DNA Virus Infections |
Novartis Pharmaceuticals|Novartis |
June 2009 | -- |
| NCT00877149 | Completed | Compensated Chronic Hepatitis B |
Novartis Pharmaceuticals|Novartis |
March 2009 | Phase 4 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
