pour la recherche uniquement
BGJ398 (Infigratinib) FGFR inhibiteur
Réf. CatalogueS2183
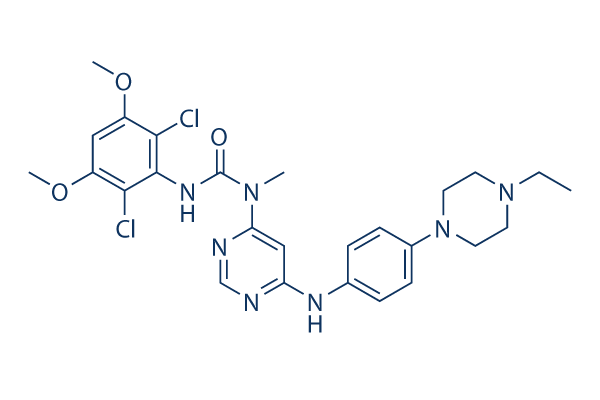
Structure chimique
Poids moléculaire: 560.48
Contrôle Qualité
Produits souvent utilisés avec BGJ398 (Infigratinib)
| Cibles apparentées | EGFR VEGFR JAK PDGFR Src HIF FLT FLT3 HER2 Bcr-Abl |
|---|---|
| Autre FGFR Inhibiteurs | PD173074 AZD4547 (Fexagratinib) BLU9931 Futibatinib (TAS-120) LY2874455 PD-166866 Zoligratinib (Debio-1347) H3B-6527 Fisogatinib (BLU-554) SSR128129E |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| HCC | Growth Inhibition Assay | 1-2500 nM | 48 h | IC50= 2359 nm | 25688743 | |
| HCC | Growth Inhibition Assay | 1-2500 nM | 48 h | IC50=1124 nm | 25688743 | |
| HCT116 | Growth Inhibition Assay | 48 h | IC50=3 μM | 24503538 | ||
| HKH2 | Growth Inhibition Assay | 48 h | IC50=4 μM | 24503538 | ||
| RKO | Growth Inhibition Assay | 48 h | IC50=1.2 μM | 24503538 | ||
| LS174T | Growth Inhibition Assay | 48 h | IC50=4 μM | 24503538 | ||
| HCD9 | Growth Inhibition Assay | 0.5-5 μM | 48/72 h | DMSO | decreases cell viability | 24135816 |
| HCT116 | Growth Inhibition Assay | 0.5-5 μM | 48/72 h | DMSO | decreases cell viability | 24135816 |
| SNU-C1 | Growth Inhibition Assay | 0.5-5 μM | 48/72 h | DMSO | no effect | 24135816 |
| MFE280 | Growth Inhibition Assay | IC50=2.63 ± 0.82 μM | 23443805 | |||
| AN3CA | Growth Inhibition Assay | IC50=1.00 ± 0.20 μM | 23443805 | |||
| HEC155 | Growth Inhibition Assay | IC50=4.74 ± 1.09 μM | 23443805 | |||
| MFE296 | Growth Inhibition Assay | IC50=2.86 ± 0.20 μM | 23443805 | |||
| SPAC1S | Growth Inhibition Assay | IC50=3.19 ± 0.93 μM | 23443805 | |||
| RL952 | Growth Inhibition Assay | IC50=3.41 ± 0.23 μM | 23443805 | |||
| EN1 | Growth Inhibition Assay | IC50=4.75 ± 0.62 μM | 23443805 | |||
| SNGII | Growth Inhibition Assay | IC50=4.29 ± 0.58 μM | 23443805 | |||
| ISHIKAWA | Growth Inhibition Assay | IC50=5.48 ± 0.03 μM | 23443805 | |||
| HEC1A | Growth Inhibition Assay | IC50=10.00 ± 1.00 μM | 23443805 | |||
| KLE | Growth Inhibition Assay | IC50=3.03 ± 0.11 μM | 23443805 | |||
| SNGM | Growth Inhibition Assay | IC50=5.00 ± 0.41 μM | 23443805 | |||
| USPC2 | Growth Inhibition Assay | IC50=7.00 ± 0.21 μM | 23443805 | |||
| EN | Growth Inhibition Assay | IC50=6.03 ± 0.31 μM | 23443805 | |||
| MFE319 | Growth Inhibition Assay | IC50=5.37 ± 0.03 μM | 23443805 | |||
| EFE184 | Growth Inhibition Assay | IC50=8.04 ± 0.69 μM | 23443805 | |||
| ECC1 | Growth Inhibition Assay | IC50=6.74 ± 0.59 μM | 23443805 | |||
| HEC1B | Growth Inhibition Assay | IC50=6.45 ± 0.67 μM | 23443805 | |||
| USPC1 | Growth Inhibition Assay | IC50=5.75 ± 0.50 μM | 23443805 | |||
| SPAC1L | Growth Inhibition Assay | IC50=4.92 ± 0.50 μM | 23443805 | |||
| HCC827 | Function assay | Displacement of [3H]-cyclopamine from SMO V404M mutant in gefitinib resistant human HCC827 cells by scintillation counting, Ki = 0.0465 μM. | 28787156 | |||
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| sf9 | Function assay | 60 mins | Inhibition of non-phosphorylated N-terminal His6-tagged FGFR4 C552A mutant (G442 to E753 residues) (unknown origin) expressed in sf9 cells using 5-Fluo-Ahx-KKKKEEIYFFFG-NH2 as substrate after 60 mins by microfluidic mobility shift assay, IC50 = 0.00082 μM. | ChEMBL | ||
| sf9 | Function assay | 60 mins | Inhibition of wild type non-phosphorylated N-terminal His6-tagged FGFR4 (G442 to E753 residues) (unknown origin) expressed in sf9 cells using 5-Fluo-Ahx-KKKKEEIYFFFG-NH2 as substrate after 60 mins by microfluidic mobility shift assay, IC50 = 0.062 μM. | ChEMBL | ||
| sf9 | Function assay | 60 mins | Inhibition of non-phosphorylated N-terminal His6-tagged FGFR4 C477A mutant (G442 to E753 residues) (unknown origin) expressed in sf9 cells using 5-Fluo-Ahx-KKKKEEIYFFFG-NH2 as substrate after 60 mins by microfluidic mobility shift assay, IC50 = 0.064 μM. | ChEMBL | ||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 560.48 | Formule | C26H31Cl2N7O3 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 872511-34-7 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | NVP-BGJ398 | Smiles | CCN1CCN(CC1)C2=CC=C(C=C2)NC3=CC(=NC=N3)N(C)C(=O)NC4=C(C(=CC(=C4Cl)OC)OC)Cl | ||
Solubilité
|
In vitro |
DMSO
: 3 mg/mL
(5.35 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
FGFR1
(Cell-free assay) 0.9 nM
FGFR3
(Cell-free assay) 1.0 nM
FGFR2
(Cell-free assay) 1.4 nM
FGFR3 (K650E)
(Cell-free assay) 4.9 nM
FGFR4
(Cell-free assay) 60 nM
|
|---|---|
| In vitro |
Infigratinib (BGJ398) prévient également VEGFR2 avec une faible puissance, avec un IC50 de 0,18 μM pour l'inhibition de cette cible. Il supprime d'autres kinases, y compris ABL, FYN, KIT, LCK, LYN et YES avec des valeurs d'IC50 de 2,3 μM, 1,9 μM, 0,75 μM, 2,5 μM, 0,3 μM et 1,1 μM, respectivement. Au niveau cellulaire, ce composé inhibe la prolifération des cellules BaF3 dépendantes de FGFR1, FGFR2-Q et FGFR3 avec des IC50 de 2,9 μM, 2,0 μM et 2 μM, respectivement. Il interfère avec l'autophosphorylation sur des résidus tyrosine spécifiques, y compris FGFR-WT, FGFR2-WT, FGFR3-K650E, FGFR3-S249C et FGFR4-WT avec des IC50 de 4,6 nM, 4,9 nM, 5 nM, 5 nM et 168 nM, respectivement. De plus, il supprime la prolifération des cellules cancéreuses avec surexpression de FGFR3 de type sauvage (WT) telles que RT112, RT4, SW780 et JMSU1 avec des IC50 de 5 nM, 30 nM, 32 nM et 15 nM, respectivement.
|
| Essai kinase |
Essai de kinase radiométrique
|
|
L'activité kinase enzymatique est évaluée en mesurant la phosphorylation d'un substrat synthétique par le domaine kinase FGFR3-K650E de fusion GST purifié, en présence d'ATP radiomarqué. Les activités enzymatiques sont mesurées en mélangeant 10 μL d'une solution 3 fois concentrée d'Infigratinib (BGJ398) ou d'un contrôle avec 10 μL du mélange de substrat correspondant (substrat peptidique, ATP et [γ33P]ATP). Les réactions sont initiées par l'ajout de 10 μL d'une solution 3 fois concentrée de l'enzyme dans le tampon d'essai. Les concentrations finales des composants de l'essai sont les suivantes : 10 ng de GST-FGFR3-K650E, 20 mM Tris-HCl, pH 7,5, 3 mM MnCl2, 3 mM MgCl2, 1 mM DTT, 250 μg/mL PEG 20000, 2 μg/mL poly(EY) 4:1, 1% DMSO et 0,5 μM ATP (γ-[33P]-ATP 0,1 μCi). L'essai est réalisé selon la méthode de liaison sur filtre (FB) dans des plaques à 96 puits à température ambiante pendant 10 minutes dans un volume final de 30 μL incluant ce composé. Les réactions enzymatiques sont arrêtées par l'ajout de 20 μL d'EDTA 125 mM, et l'incorporation de 33P dans les substrats polypeptidiques est quantifiée comme suit : 30 μL du mélange réactionnel arrêté sont transférés sur des membranes Immobilon-PVDF préalablement trempées pendant 5 minutes dans du méthanol, rincées à l'eau, trempées pendant 5 minutes dans 0,5% H3PO4, et montées sur un collecteur sous vide avec une source de vide déconnectée. Après le dépôt, le vide est connecté, et chaque puits est rincé avec 0,5% H3PO4 (200 μL). Les membranes libres sont retirées et lavées quatre fois sur un agitateur avec 1% H3PO4 et une fois avec de l'éthanol. Les membranes sont séchées et recouvertes de 10 μL/puits d'un liquide de scintillation. Les plaques sont finalement scellées et comptées dans un compteur de scintillation à microplaques. Les valeurs IC50 sont calculées par analyse de régression linéaire du pourcentage d'inhibition.
|
|
| In vivo |
Dans ce modèle orthotopique de xénogreffe de cancer de la vessie, BGJ398 induit une inhibition de la croissance tumorale et une stase après administration orale pendant 12 jours consécutifs aux doses de 10 et 30 mg/kg, respectivement. Fait intéressant, les animaux ayant reçu ce composé ne présentent aucune perte de poids corporel (10 mg/kg) ou une prise de poids corporel de 10 % (30 mg/kg), ce qui est une indication supplémentaire d'efficacité. Des rats Rowett femelles porteurs de tumeurs RT112 reçoivent une administration orale unique du sel monophosphate d'Infigratinib (BGJ398) aux doses de 4,25 et 8,51 mg/kg. Il diminue significativement les niveaux de pFRS2 et pMAPK de manière dose-dépendante. De plus, il inhibe significativement l'Angiogenesis stimulée par le bFGF de manière dose-dépendante. Cependant, il n'altère pas la formation de vaisseaux sanguins induite par le VEGF.
|
Références |
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | pFGFR1 / FGFR1 / pFRS2 / FRS2 / MEK / ERK p-YAP (S127) / YAP Mcl-1 Cyclin D1 / Cyclin A / Cyclin B / γ-H2AX / Cleaved caspase-9 / PARP Snail / Slug / ZEB1 p-FRS2 / FRS2 / p-AKT / AKT / p-ERK / ERK |
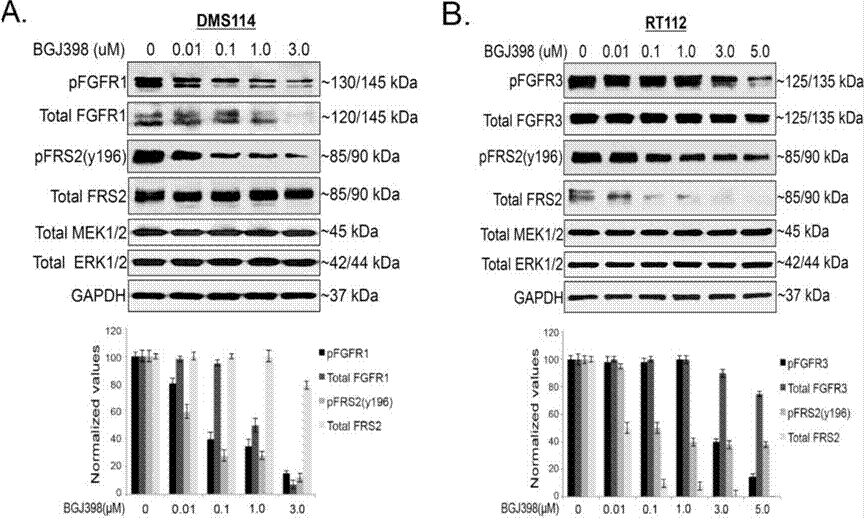
|
28255027 |
| Immunofluorescence | YAP |
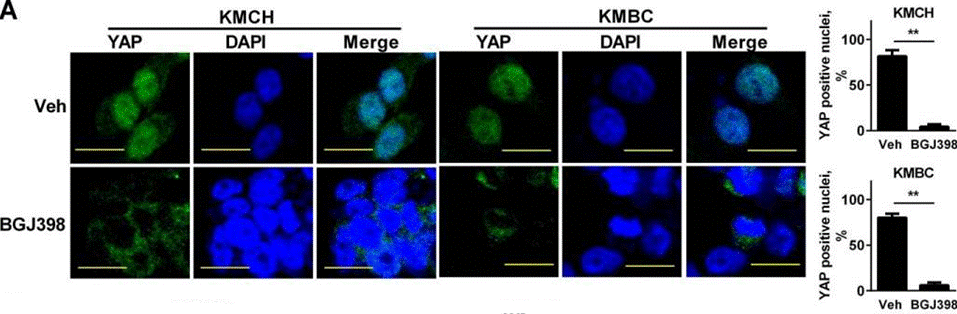
|
26826125 |
| Growth inhibition assay | Cell viability IC50 |
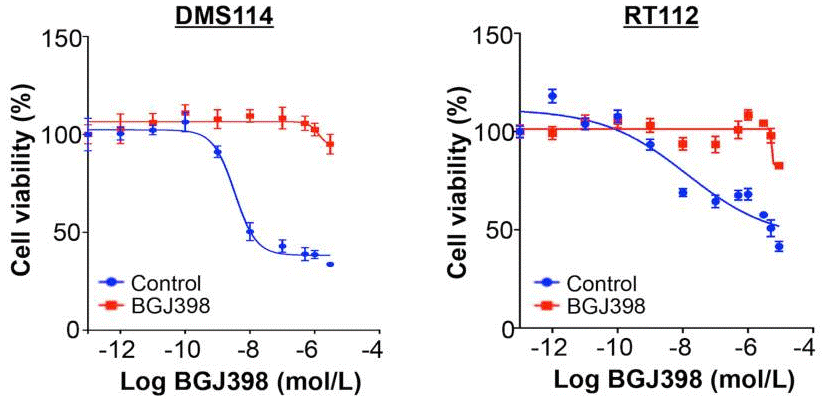
|
28255027 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03510455 | Terminated | Tumor-Induced Osteomalacia|Oncogenic Osteomalacia |
National Institute of Dental and Craniofacial Research (NIDCR)|National Institutes of Health Clinical Center (CC) |
February 27 2019 | Phase 2 |
| NCT02312804 | Withdrawn | Cancer of Cervix|Tumors |
The University of Texas Health Science Center at San Antonio |
January 2015 | Phase 1 |
| NCT02160041 | Terminated | Solid Tumor|Hematologic Malignancies |
Novartis Pharmaceuticals|Novartis |
July 24 2014 | Phase 2 |
| NCT01928459 | Completed | Advanced Solid Tumors|Metastatic Solid Tumors |
Novartis Pharmaceuticals|Novartis |
October 2013 | Phase 1 |
| NCT01004224 | Completed | Advanced Solid Tumors With Alterations of FGFR1 2 and or 3|Squamous Lung Cancer With FGFR1 Amplification|Bladder Cancer With FGFR3 Mutation or Fusion|Advanced Solid Tumors With FGFR1 Amplication|Advanced Solid Tumors With FGFR2 Amplication|Advanced Solid Tumors With FGFR3 Mutation |
Novartis Pharmaceuticals|Novartis |
December 11 2009 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
Foire aux questions
Question 1:
If you have any suggestions about the formulation of this compound for a direct oral gavage administration?
Réponse :
It can be dissolved in 30% PEG400/0.5% Tween80/5% Propylene glycol at 30 mg/ml as a suspension.
