pour la recherche uniquement
lurasidone Dopamine Receptor antagoniste
Réf. CatalogueS5714
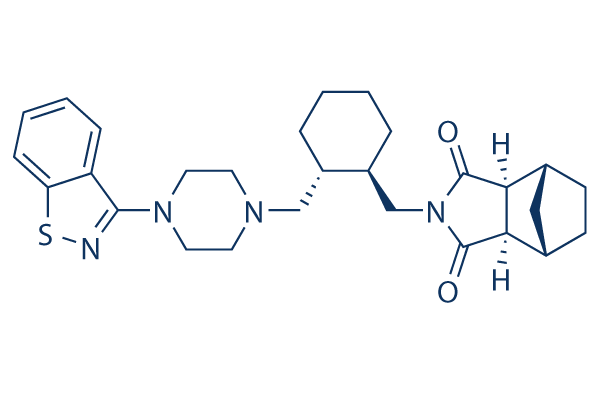
Structure chimique
Poids moléculaire: 492.68
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- SDS
- Fiche technique
| Cibles apparentées | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Autre Dopamine Receptor Inhibiteurs | MPTP Hydrochloride Trifluoperazine Trifluoperazine 2HCl Penfluridol Sulpiride Levosulpiride SCH-23390 hydrochloride Domperidone Rotundine Azaperone |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 492.68 | Formule | C28H36N4O2S |
Stockage (À compter de la date de réception) | 3 years -20°C powder |
|---|---|---|---|---|---|
| N° CAS | 367514-87-2 | -- | Stockage des solutions mères |
|
|
| Synonymes | SM-13496 | Smiles | C1CCC(C(C1)CN2CCN(CC2)C3=NSC4=CC=CC=C43)CN5C(=O)C6C7CCC(C7)C6C5=O | ||
Solubilité
|
In vitro |
DMSO
: 7 mg/mL
(14.2 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
5-HT2A
(Cell-free assay) 0.5 nM(Ki)
5-HT7 receptor
(Cell-free assay) 0.5 nM(Ki)
D2 receptor
(Cell-free assay) 1 nM(Ki)
5-HT1A receptor
(Cell-free assay) 6.4 nM(Ki)
|
|---|---|
| In vitro |
Lurasidone est un nouvel antipsychotique atypique de la classe chimique des benzoisothiazoles. Comme la plupart des antipsychotiques de deuxième génération, c'est un antagoniste complet des récepteurs dopamine D2 et sérotonine 5-HT2A, et un agoniste partiel des récepteurs 5-HT1A. Il a une affinité beaucoup plus grande pour les récepteurs du sous-type 5-HT7 que les autres antipsychotiques atypiques. Ce composé a également une affinité élevée pour le sous-type 5-HT1A, les récepteurs alpha2c-adrénergiques et une faible affinité pour les récepteurs alpha1-adrénergiques. Il a une affinité minimale pour les récepteurs 5-HT2C et une affinité négligeable pour les récepteurs histaminiques H1 et muscariniques.
|
| In vivo |
Lurasidone est rapidement absorbé, atteignant des concentrations maximales en 1,5 à 3 heures (tmax) après des doses orales uniques et multiples. Une fois absorbé, il se distribue largement dans les tissus et pénètre rapidement dans le SNC. Ce composé a une forte liaison à l'albumine plasmatique humaine et à l'alpha-1-glycoprotéine (>=99%). Un traitement à long terme de la schizophrénie avec cet agent a montré une réduction du risque de rechute. La demi-vie d'élimination de cette substance chimique est d'environ 20-40 h. La Cmax moyenne et l'aire sous la courbe (AUC) pour ce médicament étaient approximativement trois fois et deux fois plus grandes, respectivement, lors d'une comparaison entre l'administration avec de la nourriture et à jeun. Son absorption est indépendante de la teneur en matières grasses des aliments. Il est métabolisé principalement via le CYP3A4. Dans les études animales, ce composé a pénétré la barrière placentaire et s'est distribué dans le fœtus, et a été excrété dans le lait pendant la lactation.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03627195 | Completed | Schizophrenia |
Sumitomo Pharma America Inc. |
June 7 2018 | Phase 1 |
| NCT02731612 | Recruiting | Bipolar Disorder |
Nazlin Walji|University of British Columbia |
May 8 2017 | Phase 3 |
| NCT02147379 | Completed | Bipolar I Disorder |
University of British Columbia |
May 2014 | Phase 3 |
| NCT02174523 | Completed | Schizophrenia |
Sumitomo Pharma (Suzhou) Co. Ltd.|Xuhui Central Hospital Shanghai |
April 2014 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
