pour la recherche uniquement
OSI-930 c-Kit inhibiteur
Réf. CatalogueS1220
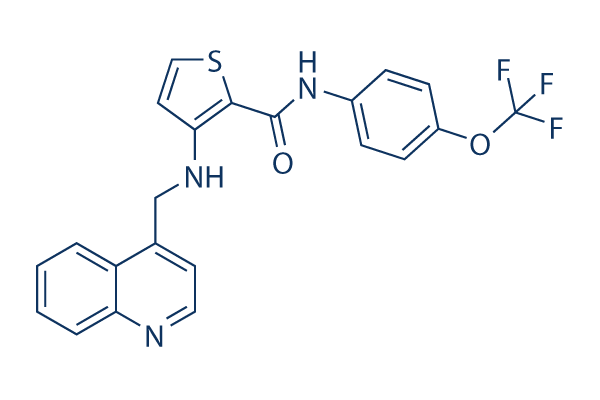
Structure chimique
Poids moléculaire: 443.44
Contrôle Qualité
| Cibles apparentées | EGFR VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 |
|---|---|
| Autre c-Kit Inhibiteurs | Masitinib Amuvatinib (MP-470) Sitravatinib (MGCD516) PDGFR inhibitor 1 ISCK03 AZD3229 Masitinib mesylate Bezuclastinib Elenestinib phosphate M4205(IDRX-42) |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 443.44 | Formule | C22H16F3N3O2S |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 728033-96-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | C1=CC=C2C(=C1)C(=CC=N2)CNC3=C(SC=C3)C(=O)NC4=CC=C(C=C4)OC(F)(F)F | ||
Solubilité
|
In vitro |
DMSO
: 89 mg/mL
(200.7 mM)
Ethanol : 3 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
FLT1
(Cell-free assay) 8 nM
KDR
(Cell-free assay) 9 nM
CSF-1R
(Cell-free assay) 15 nM
LCK
(Cell-free assay) 22 nM
C-Raf
(Cell-free assay) 41 nM
Kit
(Cell-free assay) 80 nM
|
|---|---|
| In vitro |
OSI-930 inhibe la prolifération cellulaire dans la lignée cellulaire HMC-1 avec une IC50 de 14 nM sans effet significatif sur la croissance de la lignée cellulaire COLO-205 qui n'exprime pas de récepteur tyrosine kinase mutant constitutivement actif. De plus, ce composé induit également l'apoptose dans la lignée cellulaire HMC-1 avec une EC50 de 34 nM. Une étude récente montre que ce produit chimique inactive le cytochrome P450 (P450) 3A4 purifié et recombinant avec un Ki de 24 μM de manière dépendante du temps et de la concentration.
|
| Essai kinase |
Tests de protéine kinase
|
|
Les tests de protéine kinase sont effectués en interne par des méthodes d'analyse basées sur ELISA (Kit, KDR, PDGFRα et PDGFRβ) ou par une méthode radiométrique. Les tests ELISA internes utilisaient du poly(Glu:Tyr) comme substrat lié à la surface de plaques d'analyse à 96 puits ; la phosphorylation est ensuite détectée à l'aide d'un anticorps anti-phosphotyrosine conjugué à la HRP. L'anticorps lié est ensuite quantifié à l'aide d'ABTS comme substrat de peroxydase en mesurant l'absorbance à 405/490 nm. Toutes les analyses utilisent des domaines catalytiques de kinase recombinants purifiés qui sont exprimés dans des cellules d'insectes ou dans des bactéries. La protéine Kit et EGFR utilisée pour les analyses internes est préparée en interne ; d'autres enzymes sont obtenues. La protéine recombinante Kit est exprimée sous forme de protéine de fusion glutathion S-transférase NH2-terminale dans des cellules d'insectes et est initialement purifiée comme une enzyme non phosphorylée (non activée) avec un Km relativement élevé pour l'ATP (400 μM). Dans certaines analyses, une forme activée (tyrosine phosphorylée) de l'enzyme est préparée par incubation avec 1 mM d'ATP pendant 1 heure à 30 °C. La protéine phosphorylée est ensuite passée à travers une colonne de dessalage pour éliminer la majorité de l'ATP et stockée à -80 °C dans un tampon contenant 50 % de glycérol. La préparation résultante a une activité spécifique considérablement plus élevée et un Km pour l'ATP (25 μM) plus faible que la préparation initiale non phosphorylée. L'inhibition de l'autophosphorylation de Kit par ce composé est testée par incubation de l'enzyme non phosphorylée à 30 °C en présence de 200 μM d'ATP et de diverses concentrations de ce produit chimique. La réaction est arrêtée par le prélèvement d'aliquotes dans un tampon d'échantillon SDS-PAGE suivi d'un chauffage à 100 °C pendant 5 minutes. Le degré de phosphorylation de Kit est ensuite déterminé par immunotransfert pour le Kit total et le Kit phosphorylé.
|
|
| In vivo |
OSI-930, administré à la dose maximale efficace de 200 mg/kg par gavage oral, présente une activité antitumorale puissante dans un large éventail de modèles de xénogreffes précliniques, y compris les modèles de xénogreffes HMC-1, NCI-SNU-5, COLO-205 et U251.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT00513851 | Completed | Advanced Solid Tumors |
Astellas Pharma Inc|OSI Pharmaceuticals |
April 2006 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
