pour la recherche uniquement
Abacavir Reverse Transcriptase inhibiteur
Réf. CatalogueS5215
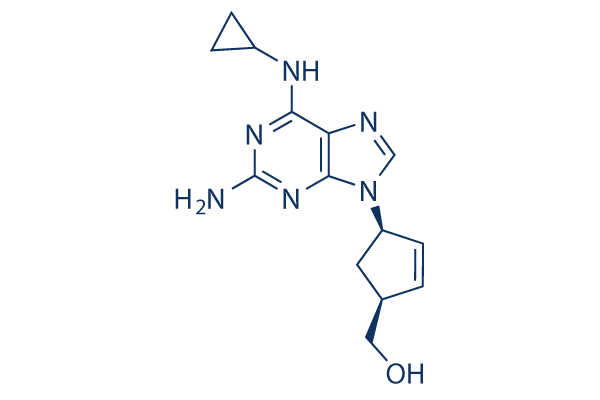
Structure chimique
Poids moléculaire: 286.33
Contrôle Qualité
| Cibles apparentées | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite HIV HCV Protease |
|---|---|
| Autre Reverse Transcriptase Inhibiteurs | Dapivirine (TMC120) Fangchinoline Salicylanilide 3'-Fluoro-3'-deoxythymidine (Alovudine) Ulonivirine Lersivirine (UK-453061) Bifendate 4-Chloro-2-(trifluoroacetyl)aniline hydrochloride |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 286.33 | Formule | C14H18N6O |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 136470-78-5 | -- | Stockage des solutions mères |
|
|
| Synonymes | 1592U89 | Smiles | C1CC1NC2=C3C(=NC(=N2)N)N(C=N3)C4CC(C=C4)CO | ||
Solubilité
|
In vitro |
DMSO
: 57 mg/mL
(199.07 mM)
Ethanol : 57 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Reverse transcriptase
|
|---|---|
| In vitro |
Abacavir (ABC) présente une puissante activité antivirale in vitro contre le VIH-1 de type sauvage (IC50 4,0 μM, cellules MT-4). Ce composé induit des cassures double brin (DSB) chromosomiques et tue ainsi les cellules ATL mais pas les cellules non infectées par le HTLV-1. Une fois incorporé dans les cellules, il est phosphorylé dans un anabolisme progressif unique pour être converti en carbovir (CBV), un analogue guanine triphosphaté, puis incorporé dans l'ADN chromosomique de l'hôte par les ADN polymérases réplicatives, entraînant une terminaison prématurée de la réplication de l'ADN, un effondrement de la fourche de réplication et la formation de DSB. Ce produit chimique induit un arrêt en phase S/G2 et l'apoptose dans les cellules ED-40515(−), mais pas dans les cellules Jurkat.
|
| In vivo |
Abacavir inhibe efficacement la croissance des xénogreffes de cellules ATL chez les souris NOD/SCID. Chez l'adulte, ce composé est rapidement absorbé après administration orale, avec des concentrations maximales survenant 0,63-1 heure après la prise. La biodisponibilité absolue de l'Abacavir est d'environ 83%. Sa pharmacocinétique est linéaire et proportionnelle à la dose sur la plage de 300-1200 mg/jour. Le volume de distribution apparent après administration intraveineuse est d'environ 0,86 ± 0,15 L/kg, ce qui suggère qu'il est distribué dans les espaces extravasculaires. La liaison aux protéines plasmatiques est d'environ 50% et est indépendante de la concentration plasmatique d'Abacavir. Ce produit chimique est largement métabolisé par le foie; moins de 2% sont excrétés sous forme de médicament inchangé dans l'urine. Il est principalement métabolisé par deux voies, l'uridine diphosphate glucuronyltransférase et l'alcool déshydrogénase, produisant le métabolite glucuronide inactif et le métabolite carboxylate inactif. La demi-vie d'élimination terminale est d'environ 1,5 heure. L'effet antiviral est dû à son anabolite intracellulaire, le carbovirtriphosphate (CBV-TP). Ce composé n'est pas significativement métabolisé par les enzymes du cytochrome P450 (CYP), et il n'inhibe pas non plus ces enzymes.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04133012 | Completed | HIV-1 Infection |
ANRS Emerging Infectious Diseases|ViiV Healthcare |
February 10 2020 | Not Applicable |
| NCT02708342 | Completed | HIV |
IRCCS San Raffaele|Merck Sharp & Dohme LLC |
April 2016 | -- |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
