pour la recherche uniquement
Dexlansoprazole Proton Pump inhibiteur
Réf. CatalogueS4099
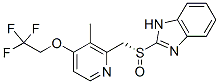
Structure chimique
Poids moléculaire: 369.36
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase |
|---|---|
| Autre Proton Pump Inhibiteurs | Bafilomycin A1 (Baf-A1) Ilaprazole Tenatoprazole Revaprazan Hydrochloride Ilaprazole sodium PF-3716556 Ufiprazole |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 369.36 | Formule | C16H14F3N3O2S |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 138530-94-6 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | T 168390, TAK 390,(R)-Lansoprazole | Smiles | CC1=C(C=CN=C1CS(=O)C2=NC3=CC=CC=C3N2)OCC(F)(F)F | ||
Solubilité
|
In vitro |
DMSO
: 74 mg/mL
(200.34 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Caractéristiques |
A modified release formulation of an enantiomer of lansoprazole.
|
|---|---|
| Targets/IC50/Ki |
Proton pump
H(+),K(+)-ATPase
|
| In vitro |
Le Dexlansoprazole, qui constitue >80 % du médicament en circulation après administration orale de lansoprazole, offre une clairance plus faible et une exposition systémique 5 fois supérieure à celle de l'énantiomère S après administration orale de lansoprazole. Ce composé MR est une formulation à libération modifiée de Dexlansoprazole, qui utilise une nouvelle technologie de double libération retardée (DDR) qui délivre le médicament en deux phases de libération distinctes, inhibant ainsi les pompes à protons nouvellement activées qui se renouvellent après l'inactivation initiale de la H+,K+-ATPase par les IPP. Cette formulation maintient les concentrations plasmatiques du médicament au-dessus du seuil plus longtemps que le lansoprazole à toutes les doses, ce qui entraîne une relation optimisée entre l'exposition au médicament et le pH intragastrique. Il supprime sélectivement la sécrétion d'acide gastrique par inhibition directe de la pompe à protons H+K+-ATPase dans la cellule pariétale gastrique, l'inhibition de cette enzyme de la membrane cellulaire bloque finalement la dernière étape de la production d'acide. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT02442752 | Withdrawn | Pediatric Gastroesophageal Reflux Disease |
Takeda |
June 15 2025 | Phase 1 |
| NCT03316976 | Completed | Healthy Volunteers |
Takeda |
November 22 2017 | Phase 1 |
| NCT03079050 | Completed | GERD|Proton Pump Inhibitor |
American University of Beirut Medical Center|Takeda |
February 27 2017 | Phase 4 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
