pour la recherche uniquement
LY2510924 CXCR antagoniste
Réf. CatalogueS8505
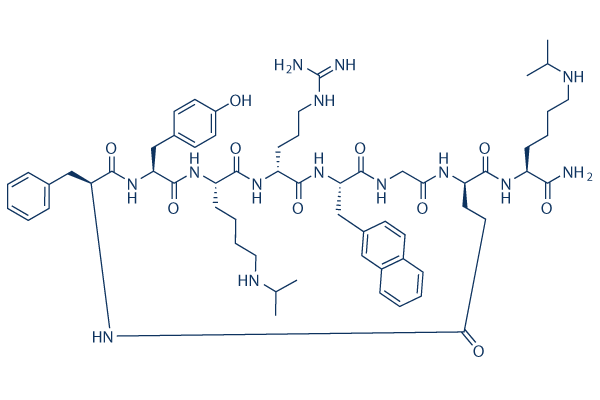
Structure chimique
Poids moléculaire: 1189.45
Contrôle Qualité
| Cibles apparentées | PD-1/PD-L1 STING AhR Immunology & Inflammation related CD markers Interleukins Anti-infection Antioxidant COX Histamine Receptor |
|---|---|
| Autre CXCR Inhibiteurs | AZD5069 SB 225002 Reparixin (Repertaxin) WZ811 Navarixin (SCH-527123) LIT-927 AMG 487 SX-682 Danirixin (GSK1325756) SB 265610 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 1189.45 | Formule | C62H88N14O10 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1088715-84-7 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CC(C)NCCCCC1C(=O)NC(C(=O)NC(C(=O)NCC(=O)NC(CCC(=O)NC(C(=O)NC(C(=O)N1)CC2=CC=C(C=C2)O)CC3=CC=CC=C3)C(=O)NC(CCCCNC(C)C)C(=O)N)CC4=CC5=CC=CC=C5C=C4)CCCN=C(N)N | ||
Solubilité
|
In vitro |
Water : 100 mg/mL |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
CXCR4
(Cell-free) 0.079 nM
|
|---|---|
| In vitro |
Dans les cellules de lymphome humain U937 exprimant CXCR4 endogène, LY2510924 inhibe la migration cellulaire induite par SDF-1 avec une valeur d'IC50 de 0,26 nmol/L et inhibe la signalisation intracellulaire médiatisée par SDF-1/CXCR4. Ce composé présente une inhibition dose-dépendante de phospho-ERK et phospho-Akt stimulés par SDF-1 dans les cellules tumorales. Les analyses biochimiques et cellulaires révèlent qu'il n'a pas d'activité agoniste apparente. Il n'a pas d'activités inhibitrices contre d'autres récepteurs de chimiokines, y compris CCR1, CCR2, CXCR2 et CXCR3, aux concentrations testées. De même, aucune activité n'a été observée parmi les récepteurs de la sérotonine, de la dopamine et des opioïdes.
|
| In vivo |
LY2510924 a une stabilité in vivo acceptable et un profil pharmacocinétique similaire à celui d'un inhibiteur de petite molécule typique chez les espèces précliniques. Ce composé montre une inhibition dose-dépendante de la croissance tumorale dans des modèles de xénogreffes humaines développés avec des cellules de lymphome non hodgkinien, de carcinome rénal, de cancer du poumon et du côlon exprimant CXCR4 fonctionnel. Dans le modèle de métastase du cancer du sein MDA-MB-231, il inhibe la métastase tumorale en bloquant le processus de migration/d'homing des cellules tumorales vers le poumon et en inhibant la prolifération cellulaire après l'homing des cellules tumorales. Cette substance chimique présente une stabilité in vivo considérablement améliorée avec une demi-vie de 3 à 5 heures chez les espèces précliniques et de 9,16 heures chez l'homme à la dose de phase II recommandée.
|
Références |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT02737072 | Terminated | Solid Tumor |
Eli Lilly and Company|AstraZeneca |
September 2016 | Phase 1 |
| NCT02652871 | Completed | Leukemia |
M.D. Anderson Cancer Center|Eli Lilly and Company|High Impact Clinical Research Support Program |
May 9 2016 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
