pour la recherche uniquement
Leucovorin Calcium Pentahydrate (Folinic acid) Inhibiteur de la DHFR
Réf. CatalogueS1236
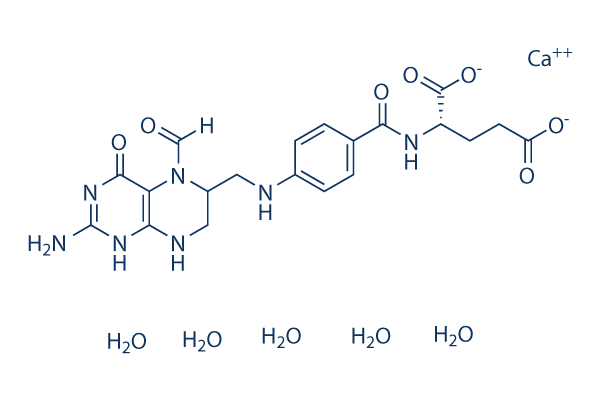
Structure chimique
Poids moléculaire: 601.58
Contrôle Qualité
| Cibles apparentées | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Autre DHFR Inhibiteurs | Calcium Folinate Aminopterin Diaveridine |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 601.58 | Formule | C20H31CaN7O12 |
Stockage (À compter de la date de réception) | 4°C (in the dark) |
|---|---|---|---|---|---|
| N° CAS | 6035-45-6 | Télécharger le SDF | Stockage des solutions mères | Les solutions sont instables. Préparer des solutions fraîches ou acheter des formats petits et préemballés. Reconditionner dès réception. | |
| Synonymes | NSC-3590 Calcium Pentahydrate, Calcium Folinatc, Citrovorum Factor | Smiles | C1C(N(C2=C(N1)N=C(NC2=O)N)C=O)CNC3=CC=C(C=C3)C(=O)NC(CCC(=O)[O-])C(=O)[O-].O.O.O.O.O.[Ca+2] | ||
Solubilité
|
In vitro |
Water : 10 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
thymidylate synthase
|
|---|---|
| In vitro |
L'administration de Leucovorin augmente le niveau de folates réduits dans les tissus, ce qui favorise l'inhibition de la thymidylate synthase dans deux tumeurs murines du côlon. Leucovorin, Gemcitabine, Oxaliplatin et 5-fluorouracil constituent un régime antitumoral et immunomodulateur puissant qui peut faire des cellules tumorales un moyen approprié pour induire une réponse CTL Ag-spécifique. Leucovorin (20 mM) augmente la cytotoxicité dans les trois expériences répétées dans 10 des 11 lignées cellulaires de carcinome colorectal humain. Leucovorin améliore la cytotoxicité du trimetrexate/fluorouracil, mais pas du methotrexate/fluorouracil, dans les cellules CCRF-CEM. Leucovorin (LV) est un cofacteur folique réduit qui entre en compétition avec RTX pour le transport et la polyglutamation dans les tissus tumoraux et normaux et a donc un potentiel en tant qu'agent de sauvetage. Leucovorin inverse les effets inhibiteurs de croissance et potentiellement cytotoxiques de RTX sur les populations de cellules viables. |
| In vivo |
Leucovorin (200 mg/kg), administré après l'apparition d'une perte de poids sévère et de diarrhée (deux fois par jour, jours 5-7) chez les souris, prévient une perte de poids supplémentaire et induit une récupération plus précoce. Leucovorin (100 ou 200 mg/kg ; deux fois par jour les jours 4-6) réduit la concentration de RTX dans le foie de 2 à 4 fois aux jours 7, 9 et 11 par rapport aux contrôles. Les combinaisons Leucovorin/5-FU et Gastrimmune (200 mg/mL) (12,5 et 20 mg/kg) augmentent les effets thérapeutiques sur la croissance in vivo des tumeurs DHDK12 par rapport aux agents administrés seuls. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06403189 | Not yet recruiting | Plexus Choroideus|Metabolic Syndrome |
Assistance Publique - Hôpitaux de Paris |
July 1 2024 | Not Applicable |
| NCT05013164 | Completed | Autism Spectrum Disorder |
Nishtar Medical University |
October 1 2020 | Phase 2 |
| NCT04060030 | Recruiting | Autism Spectrum Disorder|Language Disorders |
Southwest Autism Research & Resource Center|Autism Speaks|State University of New York - Downstate Medical Center |
October 8 2020 | Phase 2 |
| NCT04060017 | Recruiting | Autism Spectrum Disorder|Language Disorders |
Southwest Autism Research & Resource Center|State University of New York - Downstate Medical Center|United States Department of Defense |
September 22 2020 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
