pour la recherche uniquement
Ranolazine Calcium Channel inhibiteur
Réf. CatalogueS1799
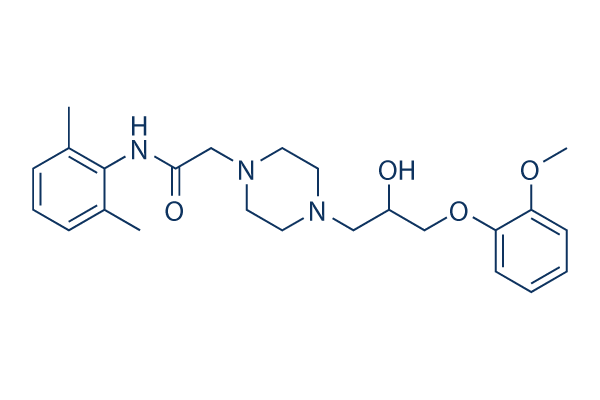
Structure chimique
Poids moléculaire: 427.54
Contrôle Qualité
| Cibles apparentées | CFTR CRM1 CD markers AChR Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase GluR |
|---|---|
| Autre Calcium Channel Inhibiteurs | Bay K 8644 Tetrandrine Nilvadipine Flunarizine 2HCl Cilnidipine YM-58483 (BTP2) Ionomycin Imperatorin Manidipine 2HCl Astragaloside A |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 427.54 | Formule | C24H33N3O4 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 95635-55-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | CVT 303, RS 43285-003 | Smiles | CC1=C(C(=CC=C1)C)NC(=O)CN2CCN(CC2)CC(COC3=CC=CC=C3OC)O | ||
Solubilité
|
In vitro |
DMSO
: 86 mg/mL
(201.15 mM)
Ethanol : 20 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Calcium channel
|
|---|---|
| In vitro |
Il a été constaté que la Ranolazine se lie plus fortement à l'état inactivé qu'à l'état de repos du canal sodique sous-jacent à I(NaL), avec des constantes de dissociation apparentes K(dr)=7,47 mM et K(di)=1,71 mM, respectivement. La Ranolazine à 5 mM et 10 mM raccourcit de manière réversible la durée des TC et abolit la post-contraction. La Ranolazine inhibe la composante tardive de INa et atténue la prolongation de la durée du potentiel d'action lorsque INa tardif est augmenté, en l'absence et en présence de médicaments bloquant IK. La Ranolazine (10 mM) réduit de 89 % l'augmentation de 13,6 fois de la variabilité de l'APD causée par 10 nM d'ATX-II. |
| In vivo |
La Ranolazine raccourcit de manière significative et réversible la durée du potentiel d'action (APD) des myocytes stimulés à 0,5 ou 0,25 Hz de manière dose-dépendante dans les myocytes ventriculaires gauches de chiens. La Ranolazine (10 mM) augmente de manière significative l'oxydation du glucose de 1,5 à 3 fois dans des conditions où la contribution du glucose à la production globale d'ATP est faible (faible Ca, FA élevé, avec insuline), élevée (Ca élevé, Fa faible, avec stimulation), ou intermédiaire dans les cœurs de rats en fonctionnement. La Ranolazine (10 mM) augmente de manière similaire l'oxydation du glucose dans les cœurs de Langendorff normoxiques (Ca élevé, FA faible ; 15 mL/min) de rats. La Ranolazine améliore de manière significative les résultats fonctionnels dans les cœurs ischémiques reperfusés en fonctionnement, ce qui est associé à des augmentations significatives de l'oxydation du glucose. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03486561 | Unknown status | Chronic Stable Angina |
OBS Pakistan |
April 1 2018 | Phase 4 |
| NCT03044964 | Unknown status | Angina |
Amit Malhotra MD|Gilead Sciences|Stern Cardiovascular Foundation Inc. |
January 10 2017 | Phase 4 |
| NCT02252406 | Completed | Stable Angina|Metabolic Syndrome |
University of Florida |
September 2015 | Phase 4 |
| NCT02360397 | Completed | Ventricular Premature Complexes|Myocardial Ischemia |
Kent Hospital Rhode Island|Gilead Sciences |
December 2014 | Phase 2 |
| NCT02156336 | Terminated | Diabetic Peripheral Neuropathic Pain |
Horizons International Peripheral Group|Gilead Sciences |
May 2014 | Phase 4 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
