pour la recherche uniquement
Delanzomib Proteasome inhibiteur
Réf. CatalogueS1157
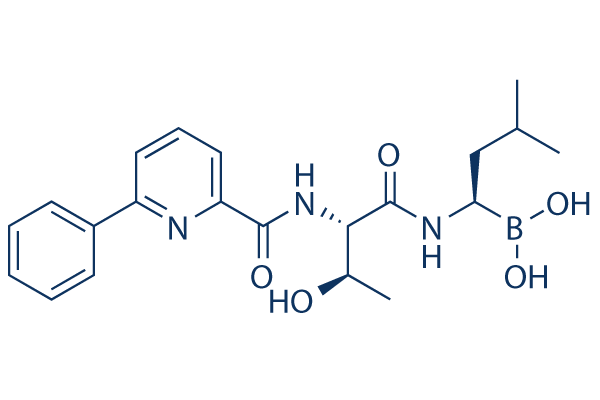
Structure chimique
Poids moléculaire: 413.28
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- HPLC
- SDS
- Fiche technique
| Cibles apparentées | HDAC Caspase Secretase MMP HCV Protease Cysteine Protease DPP Tyrosinase HIV Protease Serine Protease |
|---|---|
| Autre Proteasome Inhibiteurs | MG132 Celastrol Epoxomicin (BU-4061T) ONX-0914 (PR-957) Oprozomib VR23 Marizomib (Salinosporamide A) PI-1840 KSQ-4279 (USP1-IN-1) Isoginkgetin |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 413.28 | Formule | C21H28BN3O5 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 847499-27-8 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | CEP-18770 | Smiles | B(C(CC(C)C)NC(=O)C(C(C)O)NC(=O)C1=CC=CC(=N1)C2=CC=CC=C2)(O)O | ||
Solubilité
|
In vitro |
DMSO
: 83 mg/mL
(200.83 mM)
Ethanol : 83 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Chymotrypsin-like proteasome
3.8 nM
|
|---|---|
| In vitro |
Le CEP-18770 démontre une prévention marginale des activités trypsiques et peptidyl-glutamyl du Proteasome. Le CEP-18770 inhibe les cellules cancéreuses ovariennes A2780, le cancer de la prostate PC3, le H460, le cancer du côlon LoVo, le myélome multiple RPMI8226 et le lymphome non hodgkinien anaplasique HS-Sultan avec des valeurs de CI50 de 13,7, 22,2, 34,2, 11,3, 5,6 et 8,2 nM, respectivement. Le CEP-18770 bloque la voie ubiquitine-Proteasome dans plusieurs MM et dans la lignée cellulaire de leucémie myéloïde chronique, K562. Le CEP-18770 provoque une accumulation de protéines ubiquitinées sur 4 à 8 heures. La dégradation de l'IκBα est complètement bloquée par un prétraitement au CEP-18770. Le CEP-18770 inhibe significativement les niveaux élevés d'activité NF-κB dans les cellules RPMI-8226 et U266. La suppression dépendante du temps et de la concentration de l'activité de liaison à l'ADN du NF-kB dans les lignées cellulaires de MM par le CEP-18770 entraîne une diminution de l'expression de plusieurs gènes modulés par le NF-κB médiant la croissance et la survie des cellules tumorales, y compris l'IkBα lui-même, la protéine inhibitrice de l'apoptose liée au chromosome X (XIAP), les cytokines pro-inflammatoires TNF-α et l'interleukine-1β (IL-1β), la molécule d'adhésion intracellulaire (ICAM1) et le facteur pro-angiogénique facteur de croissance endothélial vasculaire. L'expression de ces gènes médiés par le NF-κB est associée à une meilleure réponse clinique à cet agent, soulignant leur valeur pronostique potentielle en réponse à l'exposition au CEP-18770. L'activité pro-apoptotique du CEP-18770 contre le MM n'est pas limitée uniquement aux lignées cellulaires de MM dérivées de tumeurs, mais s'étend aux explants primaires de MM de patients en rechute ou réfractaires. De plus, le CEP-18770 en combinaison produit une inhibition synergique de la viabilité des cellules de MM in vitro. |
| Essai kinase |
Sondage de l'activité du Proteasome dans les extraits cellulaires
|
|
Les cellules humaines de myélome multiple sont lavées deux fois avec du sérum physiologique tamponné au phosphate froid, centrifugées et lysées avec un volume de billes de verre (<106 microns, lavées à l'acide) et un volume égal de tampon d'homogénéisation (50 mM Tris (pH 7,4), 1 mM dithiothréitol, 5 mM MgCl2, 2 mM ATP et 250 mM saccharose) par vortexage à haute vitesse pendant 15 à 30 min à 4 °C. Les billes, les fractions membranaires, les noyaux et les débris cellulaires sont ensuite retirés du surnageant par centrifugation à 16 000 g pendant 5 min. La teneur en protéines des extraits est quantifiée à l'aide de l'essai de Bradford. L'activité du Proteasome est mesurée comme décrit ci-dessous. Des quantités égales (typiquement 60 g) de protéines sont dénaturées par ébullition dans un tampon d'échantillon réducteur, séparées par SDS-PAGE à 12,5 % et transférées électriquement sur des membranes de difluorure de polyvinylidène (PVDF). L'immunoblotting est effectué à l'aide d'un anticorps polyclonal dansyl-sulfonamidohexanoyl (1:7 500, lapin) et d'un anticorps secondaire de chèvre ou de porc anti-lapin couplé à la peroxydase de raifort, suivi d'une chimioluminescence améliorée.
|
|
| In vivo |
Le CEP-18770 révèle une inhibition relative du poids tumoral dose-dépendante et soutenue. Le CEP-18770 conduit à des régressions tumorales complètes dose-dépendantes, ce qui entraîne une incidence de 50 % de CR à sa dose maximale tolérée (DMT) de 1,2 mg/kg par voie intraveineuse. Le CEP-18770 révèle une augmentation dose-dépendante de l'incidence de souris sans tumeur à la fin de ces études (120 jours après la transplantation tumorale). L'administration orale de CEP-18770 produit une diminution marquée du poids tumoral et une incidence dose-dépendante notable de régression tumorale complète avec des changements minimaux du poids corporel des animaux au cours des études de 120 jours.ELes doses équiactives de CEP-18770 révèlent une inhibition plus importante et plus soutenue de l'activité du Proteasome tumoral, correspondant temporairement à l'induction maximale de l'activité des caspases-3 et 7. Le signal apoptotique maximal est 2,5 fois plus élevé pour le CEP-18770. En revanche, les profils d'inhibition du Proteasome du CEP-18870 sont comparables dans les tissus périphériques normaux de souris examinés (foie, poumons, sang total et cerveau [aucune activité]) tant par leur magnitude que par leur durée. Aucune inhibition du Proteasome n'est détectée dans le tissu cérébral à aucun moment pour le CEP-18770 ou. Le CEP-18770 PO en monothérapie montre également des effets anti-MM marqués dans ces modèles de xénogreffe. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT01348919 | Completed | Multiple Myeloma |
Teva Branded Pharmaceutical Products R&D Inc. |
August 3 2011 | Phase 1|Phase 2 |
| NCT01023880 | Terminated | Multiple Myeloma |
Cephalon|Teva Branded Pharmaceutical Products R&D Inc. |
January 2010 | Phase 1|Phase 2 |
| NCT00572637 | Completed | Solid Tumors|Lymphoma Non-Hodgkin |
Ethical Oncology Science |
November 2007 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
