pour la recherche uniquement
Lycorine hydrochloride ADC Cytotoxin inhibiteur
Réf. CatalogueS3800
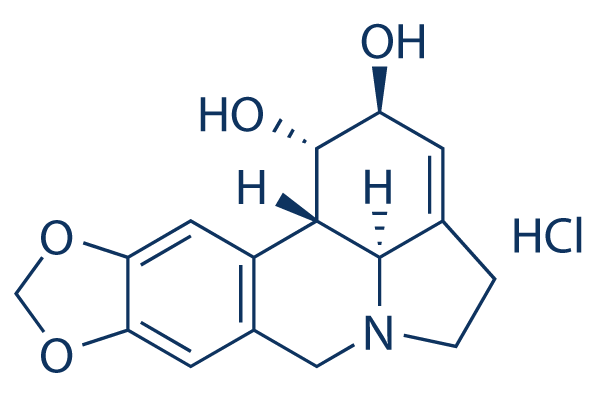
Structure chimique
Poids moléculaire: 323.77
Contrôle Qualité
| Cibles apparentées | HDAC Caspase Proteasome Secretase MMP HCV Protease Cysteine Protease DPP Tyrosinase HIV Protease |
|---|---|
| Autre ADC Cytotoxin Inhibiteurs | Triptolide SN-38 Luteolin (+)-Bicuculline Rutin Artemisinin BHQ Pinocembrin Harmine hydrochloride Luteoloside |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 323.77 | Formule | C16H17NO4.HCl |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 2188-68-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Galanthidine hydrochloride, Amarylline hydrochloride, Narcissine hydrochloride, Licorine hydrochloride | Smiles | C1CN2CC3=CC4=C(C=C3C5C2C1=CC(C5O)O)OCO4.Cl | ||
Solubilité
|
In vitro |
DMSO
: 65 mg/mL
(200.75 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
La Lycorine possède non seulement de forts effets pharmacologiques sur de nombreuses maladies, notamment l'anti-leucémie, l'anti-tumeur, l'anti-angiogenèse, l'anti-virus, l'anti-bactéries, l'anti-inflammation et l'anti-paludisme, mais exerce également de nombreuses autres fonctions biologiques, telles que l'inhibition de l'acétylcholinestérase et de la topoisomérase, la suppression de la biosynthèse de l'acide ascorbique et le contrôle de la durée de la période circadienne. La Lycorine inhibe la prolifération cellulaire et induit l'apoptose cellulaire dans la lignée cellulaire de leucémie myéloïde aiguë (AML) HL-60, la lignée cellulaire de leucémie monocytaire U937 et la lignée cellulaire de leucémie à cellules T Jurkat. La Lycorine bloque également le cycle cellulaire des cellules KM3 du myélome multiple, induit l'arrêt du cycle cellulaire des cellules K562 en phase G0/G1 et supprime la tumorigenèse et la croissance de diverses cellules tumorales, notamment le mélanome C8161, le cancer de l'ovaire Hey1B, le cancer du poumon A549, le glioblastome U373 et le cancer de l'œsophage OE21. La Lycorine peut inhiber la synthèse des protéines dans les cellules eucaryotes et l'activité de l'acétylcholinestérase.
|
|---|---|
| In vivo |
La Lycorine présente ses nombreux effets pharmacologiques sur diverses maladies avec une très faible toxicité et des effets secondaires légers. Dans les études in vivo, la lycorine inhibe efficacement la croissance tumorale dans plusieurs modèles de xénogreffes de souris. Elle inhibe efficacement la néovascularisation tumorale. La lycorine a une toxicité triviale pour les cellules normales et les organismes normaux. Les expériences toxicologiques animales montrent que le taux de mortalité létale à 50% (DL50) de la lycorine chez la souris est de 112,2 ± 0,024 mg/kg par injection intrapéritonéale. La DL50 de la lycorine chez la souris est de 344 mg/kg par injection par gavage gastrique, ce qui suggère que la lycorine a une très faible toxicité en administration gastro-intestinale. Les études in vivo montrent que la lycorine a une cinétique plasmatique linéaire avec une demi-vie d'élimination moyenne de 0,67 et 0,3 h après une administration unique s.c. et i.v. respectivement. La biodisponibilité orale moyenne est estimée à environ 40%. Les paramètres biochimiques et hématologiques des études de sécurité n'indiquent aucun signe pathologique.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
