pour la recherche uniquement
Syringic acid Antioxidant produit chimique
Réf. CatalogueS3629
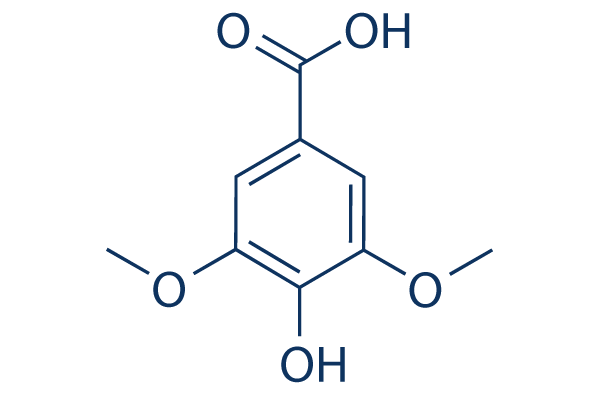
Structure chimique
Poids moléculaire: 198.17
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- SDS
- Fiche technique
| Cibles apparentées | EGFR VEGFR JAK PDGFR FGFR Src HIF FLT FLT3 HER2 |
|---|---|
| Autre Antioxidant Inhibiteurs | Elamipretide (SS-31, MTP-131) Tangeretin (+)-Catechin Silymarin Oleuropein (-)Epicatechin Hydroxygenkwanin Cocoa Extract Sesamol Flavanone |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 198.17 | Formule | C9H10O5 |
Stockage (À compter de la date de réception) | 3 years -20°C powder (seal) |
|---|---|---|---|---|---|
| N° CAS | 530-57-4 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | 3,5-dimethyl ether Gallic Acid, 3,5-dimethoxy-4-hydroxy Benzoic Acid, NSC 2129, SYRA | Smiles | COC1=CC(=CC(=C1O)OC)C(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 39 mg/mL
(196.8 mM)
Ethanol : 39 mg/mL Water : 1 mg/mL |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
Syringic acid améliore les expressions de TH, DAT et VMAT2 et atténue également significativement l'augmentation de l'expression des marqueurs inflammatoires induite par MPTP/p2. Ce prétraitement composé inhibe évidemment les lésions des cellules RGC-5 induites par H2O2 et diminue également la production de ROS et le contenu en MDA induits par H2O2. Il peut protéger les cellules RGC-5 contre l'apoptose induite par H2O2 par l'activation de la voie de signalisation PI3K/Akt. Ce produit chimique montre un effet antimitogénique dépendant du temps et de la dose (IC50 = 0,95-1,2 mg/mL) contre les cellules cancéreuses avec peu de cytotoxicité sur les fibroblastes normaux (≤20%). Il altère le cycle cellulaire (phases S/G2-M ou G1/G2-M) de manière dépendante du temps, induit l'apoptose, inhibe l'activité de liaison à l'ADN de NFκB (p ≤ 0,0001), les activités chymotrypsine-like/PGPH (peptidyl-glutamyl peptide-hydrolyzing) (p ≤ 0,0001) et trypsine-like (p ≤ 0,002) du protéasome 26S et l'Angiogenesis. Il sensibilise également différentiellement les cellules cancéreuses aux chimiothérapies standard avec une augmentation marquée de leur sensibilité au camptothécine (500 fois), au 5FU (20 000 fois), à la doxorubicine (210 fois), au taxol (3134 fois), à la vinblastine (1000 fois), à la vincristine (130 fois) et à l'amsacrine (107 fois) par rapport aux médicaments standard seuls. Ce composé exerce ses effets chimiothérapeutiques et chimiosensibilisants par une série de mécanismes, y compris l'arrêt du cycle cellulaire, l'induction de l'apoptose, l'inhibition de la prolifération cellulaire, la migration cellulaire, l'Angiogenesis, la liaison à l'ADN de NFκB et les activités du protéasome. |
|---|---|
| In vivo |
Syringic acid a des effets hépatoprotecteurs dans divers modèles animaux. L'administration orale de ce composé (10 mg/kg de poids corporel) a été rapportée comme une récupération partielle de l'apprentissage et des troubles de la mémoire induits par la neurotoxicité de l'amyloïde β chez les souris. Il facilite également les effets protecteurs sur les reins en cas de lésion d'ischémie-reperfusion rénale. Des activités antimicrobiennes de ce produit chimique sont également rapportées contre divers agents pathogènes. Ses effets anticancéreux ont été explorés sur les cellules de carcinome pulmonaire A549 et il a été constaté qu'il présentait des effets apoptotiques avec une IC50 de 30 μM. Cet acide atténue l'élévation des composants glycoprotéiques chez les rats normaux et diabétiques. Il peut augmenter la sécrétion d'insuline des cellules β du pancréas et normaliser le niveau de glucose plasmatique. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05025189 | Completed | Healthy |
University of California Los Angeles|The California Table grape Commission |
October 5 2020 | Not Applicable |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
