pour la recherche uniquement
Tropifexor (LJN452) FXR agoniste
Réf. CatalogueS8733
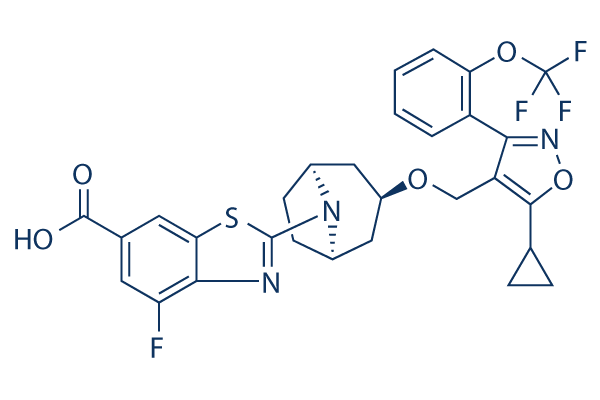
Structure chimique
Poids moléculaire: 603.58
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- HPLC
- SDS
- Fiche technique
Informations chimiques, stockage et stabilité
| Poids moléculaire | 603.58 | Formule | C29H25F4N3O5S |
Stockage (À compter de la date de réception) | 3 years -20°C powder |
|---|---|---|---|---|---|
| N° CAS | 1383816-29-2 | -- | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | C1CC1C2=C(C(=NO2)C3=CC=CC=C3OC(F)(F)F)COC4CC5CCC(C4)N5C6=NC7=C(C=C(C=C7S6)C(=O)O)F | ||
Solubilité
|
In vitro |
DMSO
: 100 mg/mL
(165.67 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
FXR
(HTRF assay) 0.2 nM(EC50)
|
|---|---|
| In vitro |
Dans des études pharmacologiques in vitro, Tropifexor (LJN452) s'est avéré être un puissant agoniste humain de FXR avec une sélectivité > 30 000 fois supérieure aux autres récepteurs nucléaires. Il pourrait augmenter l'expression de BSEP et SHP dans les hépatocytes humains primaires. |
| In vivo |
Dans la pharmacocinétique chez le rat, Tropifexor (LJN452) a une faible clairance (CL = 9 mL/min/kg) et une demi-vie terminale significativement plus longue (T1/2 = 3,7 h). La biodisponibilité orale de ce composé chez le rat est de 20 % à partir d'une formulation de microémulsion aqueuse. Chez la souris, après administration IV, il présente une faible clairance et un faible volume de distribution avec une demi-vie de 2,6 h. Chez le chien, après injection IV, la clairance était faible et la T1/2 était de 7,4 h, également avec un faible volume de distribution (0,46 L/kg). Les données précliniques démontrent une augmentation dose-dépendante des niveaux de facteur de croissance des fibroblastes 19 (FGF-19) avec celui-ci, dans les études à dose unique ou à doses multiples, avec son engagement cible dans les FXR des entérocytes. Il améliore les transaminases hépatiques et la fibrose dans le modèle ANIT. |
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04408937 | Completed | Liver Disease |
Novartis Pharmaceuticals|Novartis |
May 29 2020 | Phase 1 |
| NCT02855164 | Terminated | Non-alcoholic Steatohepatitis (NASH) |
Novartis Pharmaceuticals|Novartis |
August 1 2016 | Phase 2 |
| NCT02713243 | Completed | Primary Bile Acid Diarrhea |
Novartis Pharmaceuticals|Novartis |
January 16 2016 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
