pour la recherche uniquement
AG-14361 PARP inhibiteur
Réf. CatalogueS2178
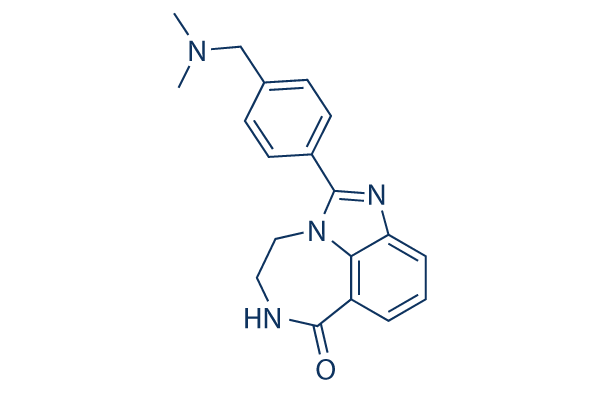
Structure chimique
Poids moléculaire: 320.39
Contrôle Qualité
| Cibles apparentées | HDAC ATM/ATR DNA-PK WRN DNA/RNA Synthesis Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Autre PARP Inhibiteurs | XAV-939 AZD5305 (Saruparib) Veliparib (ABT-888) PJ34 HCl Iniparib (BSI-201) G007-LK Pamiparib UPF 1069 A-966492 Stenoparib (E7449) |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| LoVo cells | Function assay | Concentration that gives 50% growth inhibition in LoVo cells, activity expressed as GI50, GI50=11.2 μM | ||||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 320.39 | Formule | C19H20N4O |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 328543-09-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CN(C)CC1=CC=C(C=C1)C2=NC3=CC=CC4=C3N2CCNC4=O | ||
Solubilité
|
In vitro |
DMSO
: 51 mg/mL
(159.18 mM)
Ethanol : 21 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Caractéristiques |
The 1st high-potency PARP-1 inhibitor with the specificity & in vivo activity to enhance chemotherapy and radiation therapy of human cancers.
|
|---|---|
| Targets/IC50/Ki |
PARP1
(Cell-free assay) <5 nM(Ki)
|
| In vitro |
AG14361 est au moins 1000 fois plus puissant que les benzamides. L'IC50 pour AG14361 est de 29 nM dans les cellules SW620 perméabilisées et de 14 nM dans les cellules SW620 intactes. L'analyse cristallographique de AG14361 lié au domaine catalytique de la PARP-1 de poulet montre que le système de cycle tricyclique de AG14361 est situé dans une poche composée des résidus d'acides aminés Trp861, His862, Gly863, Tyr896, Phe897, Ala898, Lys903, Ser904, Tyr907 et Glu988. AG14361 forme d'importantes liaisons hydrogène avec Ser904 et Gly863 et une liaison hydrogène médiatisée par l'eau avec Glu988. L'inhibition de la croissance induite par AG14361 n'est pas attribuée aux effets liés à PARP-1 car l'inhibition maximale de PARP-1 est observée à des concentrations beaucoup plus faibles (≤1 μM) que le GI50. AG14361 à 0,4 μM n'affecte pas l'expression génique ou la croissance des cellules cancéreuses, mais il augmente l'activité antiproliférative et inhibe la récupération des dommages potentiellement létaux causés par les rayons γ dans les cellules LoVo de 73%. De plus, 0,4 μM AG14361 n'altère pas substantiellement l'expression génique, comme le montre l'analyse par microréseau. Une exposition de 17 heures de cellules A549 à 0,4 μM AG14361 ne modifie pas l'expression des 6800 gènes. Ainsi, bien que 0,4 μM AG14361 inhibe l'activité cellulaire de PARP-1 de plus de 85%, il ne modifie essentiellement pas l'expression génique et la prolifération cellulaire, indiquant que les effets cellulaires de cette faible concentration de AG14361 sont spécifiques de l'inhibition de PARP-1. Des concentrations plus élevées, inhibitrices de la croissance, de AG14361 affectent l'expression génique, mais ces effets ne sont probablement pas liés à l'inhibition de PARP-1 car la prolifération cellulaire est affectée de manière égale dans les cellules PARP-/- et PARP-1+/+. AG14361 est rapidement absorbé dans la circulation sanguine et distribué à la tumeur et au foie, avec des concentrations plus faibles détectées dans le cerveau. Le rapport de concentration tissu/plasma indique que AG14361 est retenu dans le tissu tumoral au fil du temps dans les deux modèles de xénogreffe, avec des concentrations tumorales (≥15 μM pendant 2 heures) supérieures à celles requises pour inhiber l'activité de PARP-1 in vitro. AG14361 améliore l'activité dans toutes les cellules MMR-compétentes (1,5 à 3,3 fois) mais est plus efficace dans les cellules MMR-déficientes (potentiation de 3,7 à 5,2 fois), surmontant la résistance. En revanche, la benzylguanine n'augmente l'efficacité que dans les cellules MMR-compétentes mais est inefficace dans les cellules MMR-déficientes. AG14361 améliore les effets inhibiteurs de croissance et cytotoxiques des poisons de la topoisomérase I. AG14361 augmente la persistance des cassures simple-brin de l'ADN induites par la camptothécine. |
| Essai kinase |
Tests d'activité PARP-1
|
|
L'activité de la PARP-1 humaine recombinante pleine longueur est mesurée dans un mélange réactionnel contenant 20 nM PARP-1, 500 μM NAD+ plus [32P]NAD+ (0,1–0,3 μCi par mélange réactionnel) et de l'ADN de thymus de veau activé (10 μg/mL) à 25oC; la réaction est arrêtée après 4 minutes par l'ajout de 10% (p/v) d'acide trichloroacétique glacé. Le produit de réaction [32P]ADP-ribose incorporé dans le matériel insoluble dans l'acide est déposé sur des filtres en fibre de verre Whatman GF/C à l'aide d'un appareil de microfiltration Bio-Dot et quantifié avec un PhosphorImager. L'inhibition de l'activité de PARP-1 par AG14361 à 0–600 nM est mesurée, et le Ki pour AG14361 est calculé par analyse de régression non linéaire.
|
|
| In vivo |
Le traitement par AG14361 avant l'irradiation augmente de manière statistiquement significative la sensibilité à la radiothérapie des souris porteuses de xénogreffes LoVo. AG14361 augmente de manière statistiquement significative le flux sanguin dans les xénogreffes et augmente ainsi potentiellement l'apport médicamenteux aux xénogreffes tumorales. In vivo, des doses non toxiques de AG14361 augmentent le délai de croissance des xénogreffes LoVo induit par les rayons X de 2 à 3 fois. La co-administration de AG14361 augmente de manière statistiquement significative l'activité contre les xénogreffes LoVo, le délai de croissance tumorale étant augmenté de 3 jours à 9 jours par AG14361 à 5 mg/kg et à 10 jours par AG14361 à 15 mg/kg. La combinaison de AG14361 provoque une régression complète des tumeurs de xénogreffe SW620. L'activité PARP-1, détectée par analyse pharmacodynamique, dans les xénogreffes SW620 est inhibée de plus de 75% pendant au moins 4 heures après l'administration intrapéritonéale de AG14361 (10 mg/kg), ce qui est cohérent avec la concentration de AG14361 persistant dans la tumeur. |
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
