pour la recherche uniquement
Tivantinib c-Met inhibiteur
Réf. CatalogueS2753
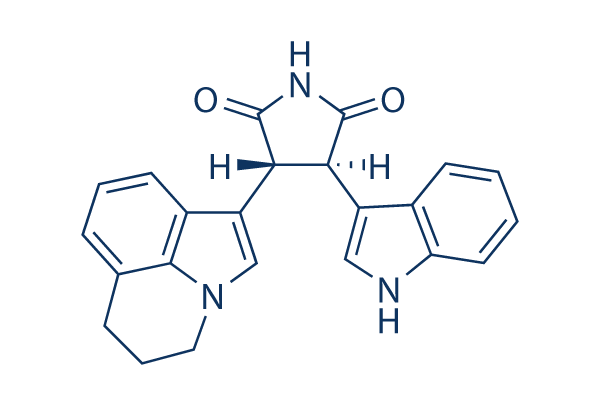
Structure chimique
Poids moléculaire: 369.42
Contrôle Qualité
| Cibles apparentées | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Autre c-Met Inhibiteurs | Tepotinib Dihexa SGX-523 PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 PF-04217903 Savolitinib (AZD6094) |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| MNK-45 | Kinase assay | ~10 μM | inhibits c-Met phosphorylation and downstream c-Met signaling pathways | |||
| HT29 | Kinase assay | ~10 μM | inhibits c-Met phosphorylation and downstream c-Met signaling pathways | |||
| MDA-MB-231 | Kinase assay | ~10 μM | inhibits c-Met phosphorylation and downstream c-Met signaling pathways | |||
| NCI-H441 | Kinase assay | ~10 μM | inhibits c-Met phosphorylation and downstream c-Met signaling pathways | |||
| SK-MEL-28 | Growth inhibitory assay | 33 μM | IC50>33 μM | |||
| NCI-H661 | Growth inhibitory assay | 33 μM | IC50>33 μM | |||
| NCI-H446 | Growth inhibitory assay | 33 μM | IC50=7 μM | |||
| MDA-MB-231 | Growth inhibitory assay | 33 μM | IC50=0.55 μM | |||
| DLD-1 | Growth inhibitory assay | 33 μM | IC50=0.53 μM | |||
| A549 | Growth inhibitory assay | 33 μM | IC50=0.59 μM | |||
| SK-OV-3 | Growth inhibitory assay | 33 μM | IC50=0.66 μM | |||
| NCI-H460 | Growth inhibitory assay | 33 μM | IC50=0.6 μM | |||
| A375 | Growth inhibitory assay | 33 μM | IC50=0.42 μM | |||
| NCI-H441 | Growth inhibitory assay | 33 μM | IC50=0.3 μM | |||
| HT29 | Growth inhibitory assay | 33 μM | IC50=0.49 μM | |||
| MKN-45 | Growth inhibitory assay | 33 μM | IC50=0.58 μM | |||
| HT29 | Apoptosis assay | ~10 μM | significantly induces apoptosis by 80-90%. | |||
| MKN-45 | Apoptosis assay | ~10 μM | significantly induces apoptosis by 80-90%. | |||
| MDA-MB-231 | Apoptosis assay | ~10 μM | modestly induces apoptosis by 35%. | |||
| MDA-MB-231/TGL | Growth inhibitory assay | ~100 μM | GI50=1.2 μM | |||
| 1833/TGL | Growth inhibitory assay | ~100 μM | GI50=3.7 μM | |||
| EBC1 | Cytotoxic assay | ~10 μM | inhibits the cell growth. | |||
| SNU638 | Cytotoxic assay | ~10 μM | inhibits the cell growth. | |||
| A549 | Cytotoxic assay | ~10 μM | not affect | |||
| H460 | Cytotoxic assay | ~10 μM | not affect | |||
| HCC827 | Cytotoxic assay | ~10 μM | not affect | |||
| A549 | Function assay | 10 μM | disrupts microtubule | |||
| EBC1 | Function assay | 10 μM | disrupts microtubule | |||
| H460 | Function assay | 10 μM | inhibits tubulin polymerization | |||
| K562/VCR | Cytotoxic assay | ~10 μM | shows cytotoxic activity | |||
| CEM/VBL | Cytotoxic assay | ~10 μM | shows cytotoxic activity | |||
| U266 | Cytotoxic assay | ~3 μM | IC50=1.1 μM | |||
| OPM-2 | Cytotoxic assay | ~3 μM | IC50=1.8 μM | |||
| MM.1S | Cytotoxic assay | ~3 μM | IC50=1.6 μM | |||
| MM.1R | Growth inhibitory assay | 3 μM | inhibits cell growth by 49% | |||
| RPMI-8226 | Cytotoxic assay | ~3 μM | IC50=0.9 μM | |||
| ANBL-6 | Cytotoxic assay | 1 μM | induces cell death by more than 50% | |||
| ANLB-6/V10R | Cytotoxic assay | 1 μM | induces cell death by more than 50% | |||
| KAS-6/1 | Cytotoxic assay | 1 μM | induces cell death by more than 50% | |||
| KAS-6/V10R | Cytotoxic assay | 1 μM | induces cell death by more than 50% | |||
| KAS-6/R10R | Cytotoxic assay | 1 μM | induces cell death by more than 50% | |||
| 8226/S | Growth inhibitory assay | 3 μM | inhibits cell growth by 54% | |||
| 8226/LR-5 | Growth inhibitory assay | 3 μM | inhibits cell growth by 54% | |||
| Huh7 | Cytotoxic assay | ~4.8 μM | DMSO | IC50=9.9 nM | ||
| Hep3B | Cytotoxic assay | ~4.8 μM | DMSO | IC50=448.7 nM | ||
| HepG2 | Cytotoxic assay | ~4.8 μM | DMSO | IC50=139.77 nM | ||
| Chang | Cytotoxic assay | ~4.8 μM | DMSO | IC50=448.7 nM | ||
| Huh7 | Function assay | 1.6 μM | DMSO | causes a G2/M cell cycle arrest | ||
| Hep3B | Function assay | 1.6 μM | DMSO | causes a G2/M cell cycle arrest | ||
| HepG2 | Function assay | 1.6 μM | DMSO | causes a G2/M cell cycle arrest | ||
| Chang | Function assay | 1.6 μM | DMSO | causes a G2/M cell cycle arrest | ||
| MHCC97L | Growth inhibitory assay | ~10 μM | DMSO | IC50=315 nM | ||
| MHCC97H | Growth inhibitory assay | ~10 μM | DMSO | IC50=368 nM | ||
| Huh7 | Growth inhibitory assay | ~10 μM | DMSO | IC50=265 nM | ||
| HepG2 | Growth inhibitory assay | ~10 μM | DMSO | IC50=392 nM | ||
| MHCC97L | Function assay | 1 μM | DMSO | induces microtubules depolymerization | ||
| Huh7 | Function assay | 1 μM | DMSO | induces microtubules depolymerization | ||
| MHCC97L | Apoptosis assay | 1 μM | DMSO | induces apoptosis | ||
| Huh7 | Apoptosis assay | 1 μM | DMSO | induces apoptosis | ||
| C3H 10T1/2 mouse fibroblasts | Kinase assay | 25 μM | DMSO | reduces Histone H3 and H4 acetylation levels | ||
| H23 | Growth inhibitory assay | 25 μM | DMSO | significantly inhibits cell growth. | ||
| WM35 | Growth inhibitory assay | 10 μM | DMSO | significantly inhibits cell growth. | ||
| NIH 3T3 | Growth inhibitory assay | 10 μM | DMSO | does not have a significant inhibitory effect | ||
| H838 | Growth inhibitory assay | 10 μM | DMSO | does not have a significant inhibitory effect | ||
| H1395 | Growth inhibitory assay | 10 μM | DMSO | does not have a significant inhibitory effect | ||
| Quiescent S2 | Kinase assay | 30 μM | DMSO | completely abrogates TSA-induced hyperacetylation of H3K4me3 histones | ||
| PC3 | Apoptosis assay | 20 μM | DMSO | induces apoptosis | ||
| Du145 | Apoptosis assay | 20 μM | DMSO | induces apoptosis | ||
| LNCaP | Apoptosis assay | 20 μM | DMSO | induces apoptosis | ||
| LAPC-4 | Apoptosis assay | 20 μM | DMSO | induces apoptosis | ||
| LNCaP | Function assay | 20 μM | DMSO | decreases PSA secretion and p65 expression levels | ||
| LAPC-4 | Function assay | 20 μM | DMSO | decreases PSA secretion and p65 expression levels | ||
| Kasumi-1 | Growth inhibitory assay | ~50 μM | DMSO | inhibits cell proliferation | ||
| SKNO-1 | Growth inhibitory assay | ~50 μM | DMSO | inhibits cell proliferation | ||
| Kasumi-1 | Kinase assay | ~10 μM | DMSO | reduces expression of acetylated histone H3, c-kit and bcl-2 | ||
| SKNO-1 | Kinase assay | ~10 μM | DMSO | reduces expression of acetylated histone H3, c-kit and bcl-2 | ||
| A549 | Function assay | 10 μM | DMSO | enhances mitotic catastrophe | ||
| NRK-52E | Function assay | 10 μM | DMSO | inhibits Ang II-induced STAT3 nuclear translocation and the expression of TGF-β1, collagen IV and fibronectin | ||
| PC12 | Growth inhibitory assay | ~12.5 μM | DMSO | prevents TSA-induced neurite formation | ||
| HPMCs | Function assay | reverses epithelial to mesenchymal transition of human peritoneal mesothelial cells | ||||
| A549 | Function assay | ~50 μM | DMSO | affects the viral life cycle and host response | ||
| RAW264.7 | Function assay | ~30 μM | DMSO | reduces pro-inflammatory gene expression | ||
| MEMM | Kinase assay | 15 µM | DMSO | decreases acetylation of histone H3 | ||
| MEMM | Growth inhibitory assay | ~20 µM | DMSO | inhibits cell proliferation | ||
| MEMM | Apoptosis assay | 15 µM | DMSO | induces the presence of the apoptosis protein, cleaved Caspase-3 | ||
| T47D | Growth inhibitory assay | 10 μM | DMSO | IC50=72 nM | ||
| ZR-75-1 | Growth inhibitory assay | 10 μM | DMSO | IC50=79 nM | ||
| BT474 | Growth inhibitory assay | 10 μM | DMSO | IC50=86 nM | ||
| HCC1954 | Growth inhibitory assay | 10 μM | DMSO | IC50=119 nM | ||
| MDA-MB-453 | Growth inhibitory assay | 10 μM | DMSO | IC50=975 nM | ||
| MDA-MB-468 | Growth inhibitory assay | 10 μM | DMSO | IC50=3208 nM | ||
| SkBr3 | Growth inhibitory assay | 10 μM | DMSO | IC50>10,000 nM | ||
| MDA-MB-231 | Growth inhibitory assay | 10 μM | DMSO | IC50>10,000 nM | ||
| HCT116 | Growth inhibitory assay | 10 μM | DMSO | IC50=5836 nM | ||
| HT29 | Growth inhibitory assay | 10 μM | DMSO | IC50>10,000 nM | ||
| HFF | Growth inhibitory assay | 10 μM | DMSO | IC50=7615 nM | ||
| HN5 | Growth inhibitory assay | 10 μM | DMSO | IC50>10,000 nM | ||
| 786-0 | Growth inhibitory assay | 10 μM | DMSO | IC50=4009 nM | ||
| H157 | Growth inhibitory assay | 10 μM | DMSO | IC50=2642 nM | ||
| NCI-H460 | Growth inhibitory assay | 10 μM | DMSO | IC50>2,500 nM | ||
| SKOV-3 | Growth inhibitory assay | 10 μM | DMSO | IC50=2126 nM | ||
| OVCAR-3 | Growth inhibitory assay | 10 μM | DMSO | IC50=2918 nM | ||
| BXPC3 | Growth inhibitory assay | 10 μM | DMSO | IC50=3141 nM | ||
| MiaPaCa | Growth inhibitory assay | 10 μM | DMSO | IC50=5433 nM | ||
| PANC-1 | Growth inhibitory assay | 10 μM | DMSO | IC50=8681 nM | ||
| LNCaP | Growth inhibitory assay | 10 μM | DMSO | IC50=147 nM | ||
| DU145 | Growth inhibitory assay | 10 μM | DMSO | IC50=3812 nM | ||
| PC3 | Growth inhibitory assay | 10 μM | DMSO | IC50>10,000 nM | ||
| BT474 | Kinase assay | 10 μM | DMSO | inhibits pGSK3β with IC50 of 160 nM | ||
| 786-0 | Kinase assay | 10 μM | DMSO | inhibits pGSK3β with IC50 of 150 nM | ||
| LNCaP | Kinase assay | 10 μM | DMSO | inhibits pGSK3β with IC50 of 43 nM | ||
| PC3 | Kinase assay | 10 μM | DMSO | inhibits pGSK3β with IC50 of 49 nM | ||
| KARPAS-231 | Growth inhibitory assay | 10 μM | DMSO | EC50=41 nM | ||
| CCRFSB | Growth inhibitory assay | 10 μM | DMSO | EC50=155 nM | ||
| SUP B15 | Growth inhibitory assay | 10 μM | DMSO | EC50=197 nM | ||
| SD-1 | Growth inhibitory assay | 10 μM | DMSO | EC50=320 nM | ||
| RS4;11 | Growth inhibitory assay | 10 μM | DMSO | EC50=654 nM | ||
| MN-60 | Growth inhibitory assay | 10 μM | DMSO | EC50=3602 nM | ||
| Tanoue | Growth inhibitory assay | 10 μM | DMSO | EC50=4517 nM | ||
| RCH-ACV | Growth inhibitory assay | 10 μM | DMSO | EC50=152 nM | ||
| SEM | Growth inhibitory assay | 10 μM | DMSO | EC50=202 nM | ||
| KASUMI-2 | Growth inhibitory assay | 10 μM | DMSO | EC50=225 nM | ||
| REH | Growth inhibitory assay | 10 μM | DMSO | EC50=288 nM | ||
| 697 | Growth inhibitory assay | 10 μM | DMSO | EC50=338 nM | ||
| NALM-6 | Growth inhibitory assay | 10 μM | DMSO | EC50=421 nM | ||
| MHH-CALL–3 | Growth inhibitory assay | 10 μM | DMSO | EC50=812 nM | ||
| MHH-CALL–2 | Growth inhibitory assay | 10 μM | DMSO | EC50=2114 nM | ||
| J.GAMMA-1 | Growth inhibitory assay | 10 μM | DMSO | EC50=65 nM | ||
| JR45.01 | Growth inhibitory assay | 10 μM | DMSO | EC50=68 nM | ||
| A3 | Growth inhibitory assay | 10 μM | DMSO | EC50=69 nM | ||
| I 2.1 | Growth inhibitory assay | 10 μM | DMSO | EC50=73 nM | ||
| MOLT-3 | Growth inhibitory assay | 10 μM | DMSO | EC50=74 nM | ||
| P116 | Growth inhibitory assay | 10 μM | DMSO | EC50=78 nM | ||
| J.Cam1.6 | Growth inhibitory assay | 10 μM | DMSO | EC50=79 nM | ||
| I 9.2 | Growth inhibitory assay | 10 μM | DMSO | EC50=80 nM | ||
| LOUCY | Growth inhibitory assay | 10 μM | DMSO | EC50=117 nM | ||
| J.RT3-T3.5 | Growth inhibitory assay | 10 μM | DMSO | EC50=123 nM | ||
| 800000 | Growth inhibitory assay | 10 μM | DMSO | EC50=163 nM | ||
| Jurkat | Growth inhibitory assay | 10 μM | DMSO | EC50=225 nM | ||
| MOLT-4 | Growth inhibitory assay | 10 μM | DMSO | EC50=232 nM | ||
| Molt-16 | Growth inhibitory assay | 10 μM | DMSO | EC50=241 nM | ||
| CEM/C3 | Growth inhibitory assay | 10 μM | DMSO | EC50=257 nM | ||
| CEM/C2 | Growth inhibitory assay | 10 μM | DMSO | EC50=271 nM | ||
| CCRFCEM | Growth inhibitory assay | 10 μM | DMSO | EC50=327 nM | ||
| CEM/C1 | Growth inhibitory assay | 10 μM | DMSO | EC50=382 nM | ||
| SUPTI[VB] | Growth inhibitory assay | 10 μM | DMSO | EC50=619 nM | ||
| CCRF–HSB-2 | Growth inhibitory assay | 10 μM | DMSO | EC50=2117 nM | ||
| I 2.1 | Apoptosis assay | 10 μM | DMSO | induces apoptosis | ||
| I 9.2 | Apoptosis assay | 10 μM | DMSO | induces apoptosis | ||
| A3 | Apoptosis assay | 10 μM | DMSO | induces apoptosis | ||
| RD | Growth inhibitory assay | 10 μM | IC50>10 μM | |||
| Rh41 | Growth inhibitory assay | 10 μM | IC50=33.8 nM | |||
| Rh18 | Growth inhibitory assay | 10 μM | IC50=303 nM | |||
| Rh30 | Growth inhibitory assay | 10 μM | IC50=4.81 μM | |||
| BT-12 | Growth inhibitory assay | 10 μM | IC50>10 μM | |||
| CHLA-266 | Growth inhibitory assay | 10 μM | IC50=1.22 μM | |||
| TC-71 | Growth inhibitory assay | 10 μM | IC50=2.52 μM | |||
| CHLA-9 | Growth inhibitory assay | 10 μM | IC50=591 nM | |||
| CHLA-10 | Growth inhibitory assay | 10 μM | IC50=102 nM | |||
| CHLA-258 | Growth inhibitory assay | 10 μM | IC50=1.05 μM | |||
| GBM2 | Growth inhibitory assay | 10 μM | IC50=9.15 μM | |||
| NB-1643 | Growth inhibitory assay | 10 μM | IC50=5.4 μM | |||
| NB-Ebc1 | Growth inhibitory assay | 10 μM | IC50>10 μM | |||
| CHLA-90 | Growth inhibitory assay | 10 μM | IC50>10 μM | |||
| CHLA-136 | Growth inhibitory assay | 10 μM | IC50>10 μM | |||
| NALM-6 | Growth inhibitory assay | 10 μM | IC50=265 nM | |||
| COG-LL-317 | Growth inhibitory assay | 10 μM | IC50=6.49 nM | |||
| RS4;11 | Growth inhibitory assay | 10 μM | IC50=147 nM | |||
| MOLT-4 | Growth inhibitory assay | 10 μM | IC50=40 nM | |||
| CCRF-CEM | Growth inhibitory assay | 10 μM | IC50=268 nM | |||
| Kasumi-1 | Growth inhibitory assay | 10 μM | IC50=107 nM | |||
| Karpas-299 | Growth inhibitory assay | 10 μM | IC50=2.93 μM | |||
| Ramos-RA1 | Growth inhibitory assay | 10 μM | IC50=7.35 μM | |||
| H1299 | Kinase assay | 10 μM | inhibits IKBKE-induced Akt Activation | |||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 369.42 | Formule | C23H19N3O2 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 905854-02-6 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | ARQ 197 | Smiles | C1CC2=C3C(=CC=C2)C(=CN3C1)C4C(C(=O)NC4=O)C5=CNC6=CC=CC=C65 | ||
Solubilité
|
In vitro |
DMSO
: 73 mg/mL
(197.6 mM)
Ethanol : 35 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Caractéristiques |
The first selective c-Met inhibitor to be advanced into human clinical trials.
|
|---|---|
| Targets/IC50/Ki |
c-Met
(Cell-free assay) 0.355 μM(Ki)
|
| In vitro |
Il a été démontré qu'ARQ-197 prévient les réponses cellulaires induites par HGF/c-met in vitro. Ce composé possède une activité antitumorale ; il inhibe la prolifération des cellules A549, DBTRG et NCI-H441 avec une IC50 de 0,38, 0,45, 0,29 μM. Le traitement avec cet agent entraîne une diminution de la phosphorylation de la cascade de signalisation MAPK et la prévention de l'invasion et de la migration. De plus, l'expression ectopique de c-Met dans NCI-H661, une lignée cellulaire n'ayant aucune expression endogène de c-Met, lui confère un phénotype invasif qui est également supprimé par ce produit chimique. Bien que l'ajout de concentrations croissantes de cet inhibiteur n'affecte pas significativement le Km de l'ATP, l'exposition de c-Met à 0,5 μM de cette substance a diminué la Vmax de c-Met d'environ 3 fois. La capacité de cette molécule à diminuer la Vmax sans affecter le Km de l'ATP a confirmé qu'elle inhibe c-Met par un mécanisme non-ATP-compétitif et peut donc expliquer son degré élevé de sélectivité de kinase. Elle empêche le c-Met humain recombinant avec une constante inhibitrice calculée Ki d'environ 355 nM. Bien que la concentration d'ATP la plus élevée utilisée soit de 200 μM, la puissance de ce composé contre c-Met n'est pas réduite en utilisant des concentrations d'ATP allant jusqu'à 1 mM. Il bloque la phosphorylation de c-Met et les voies de signalisation en aval de c-Met. Ce produit chimique supprime l'autophosphorylation constitutive et médiée par le ligand de c-Met et, par extension, l'activité de c-Met, entraînant à son tour l'inhibition des effecteurs en aval de c-Met. Son induction de l'apoptose dépendante des caspases est augmentée dans les cellules cancéreuses humaines exprimant c-Met, y compris les cellules HT29, MKN-45 et MDA-MB-231. |
| Essai kinase |
dosage de kinase in vitro par SDS-PAGE de c-Met
|
|
La protéine c-Met recombinante (100 ng) est préincubée avec des concentrations croissantes de ce composé pendant 30 minutes à température ambiante. Après préincubation, 100 μM de substrat poly-Glu-Tyr et diverses concentrations d'ATP contenant 5 μCi de [γ-32P]ATP sont ajoutées au mélange réactionnel. La réaction est incubée pendant 5 minutes à température ambiante, puis arrêtée par l'ajout de 5 μL de gel de SDS-polyacrylamide, réduisant le tampon d'échantillon. Les échantillons sont ensuite chargés sur un gel d'acrylamide à 7,5 % et une SDS-PAGE est réalisée. Les substrats poly-Glu-Tyr phosphorylés sont finalement visualisés par autoradiographie. L'activité de c-Met est quantifiée par densitométrie.
|
|
| In vivo |
Les trois modèles de xénogreffes traités avec Tivantinib présentent des réductions de la croissance tumorale : 66 % dans le modèle HT29, 45 % dans le modèle MKN-45 et 79 % dans le modèle MDA-MB-231. Dans ces études de xénogreffes, aucun changement significatif de poids corporel n'a été observé après administration orale de ce composé à 200 mg/kg. Sur le plan pharmacodynamique, la phosphorylation de c-Met dans les tumeurs xénogreffées de côlon humain (HT29) est fortement inhibée par ce produit chimique, comme l'indique une réduction spectaculaire de l'autophosphorylation de c-Met 24 heures après une seule dose orale de 200 mg/kg de cet agent. Cette même posologie chez la souris montre que les xénogreffes tumorales sont exposées à des niveaux plasmatiques soutenus du composé, ce qui est cohérent avec l'inhibition pharmacodynamique observée de la phosphorylation de c-Met et l'inhibition de la prolifération des lignées cellulaires cancéreuses hébergeant c-Met. Les niveaux plasmatiques de l'agent 10 heures après l'administration sont déterminés à 1,3 μM, soit plus de 3 fois la constante inhibitrice biochimique de cette substance pour c-Met. Par conséquent, il est capable de supprimer sa cible in vivo dans le tissu tumoral humain xénogreffé. En conclusion, cet inhibiteur bloque la croissance des tumeurs humaines xénogreffées dépendantes de c-Met. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
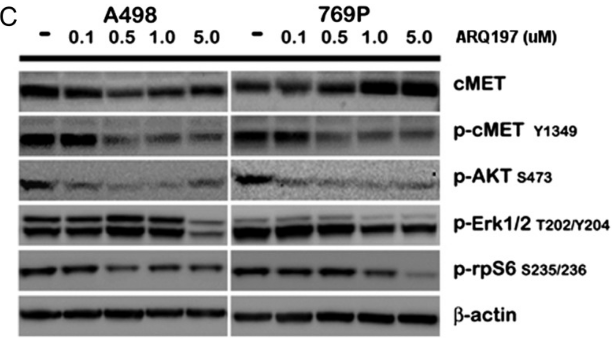
| Western blot | cMET / p-cMET / p-AKT / p-ERK / p-rpS6 |
|
23022995 |
| Growth inhibition assay | Cell viability |
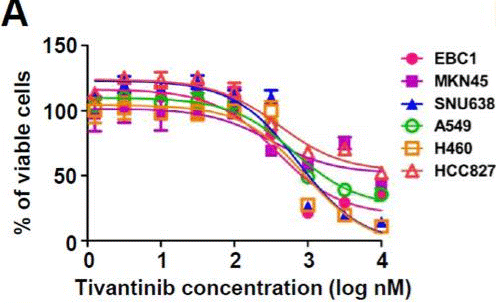
|
23598276 |
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT02150733 | Completed | Hepatic Impairment|Solid Tumor|Cancer |
Daiichi Sankyo|Medpace Inc. |
April 2014 | Phase 1 |
| NCT01892527 | Completed | Colorectal Cancer Metastatic|C-met Overexpression |
Armando Santoro MD|Istituto Clinico Humanitas |
March 2013 | Phase 2 |
| NCT02049060 | Completed | Malignant Pleural Mesothelioma|Nonsquamous Nonsmall Cell Neoplasm of Lung |
Armando Santoro MD|Istituto Clinico Humanitas |
January 2013 | Phase 1|Phase 2 |
| NCT01755767 | Completed | Hepatocellular Carcinoma |
Daiichi Sankyo|ArQule Inc. a subsidiary of Merck Sharp & Dohme LLC a subsidiary of Merck & Co. Inc. (Rahway NJ USA) |
December 27 2012 | Phase 3 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
Foire aux questions
Question 1:
Are there any other solutions (apart from DMSO) I can dissolve it for in vivo experiment?
Réponse :
S2753 This compound (ARQ 197) can be dissolved in 1% methylcellulose at 15 mg/ml as a suspension.
