pour la recherche uniquement
Golvatinib (E7050) c-Met inhibiteur
Réf. CatalogueS2859
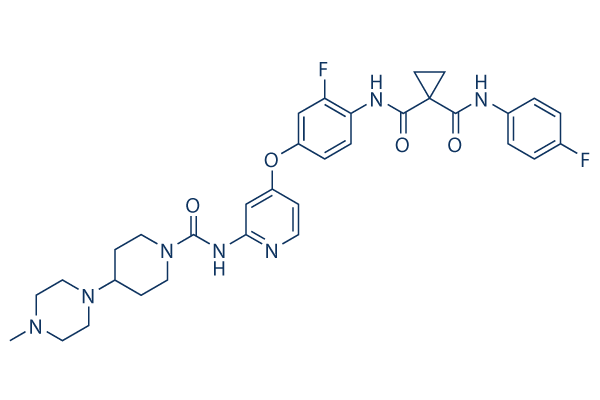
Structure chimique
Poids moléculaire: 633.69
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Autre c-Met Inhibiteurs | Tepotinib Dihexa SGX-523 PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 Tivantinib PF-04217903 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 633.69 | Formule | C33H37F2N7O4 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 928037-13-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CN1CCN(CC1)C2CCN(CC2)C(=O)NC3=NC=CC(=C3)OC4=CC(=C(C=C4)NC(=O)C5(CC5)C(=O)NC6=CC=C(C=C6)F)F | ||
Solubilité
|
In vitro |
DMSO
: 20 mg/mL
(31.56 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
c-Met
14 nM
VEGFR2
16 nM
|
|---|---|
| In vitro |
Des études in vitro indiquent que le Golvatinib (E7050) inhibe puissamment la phosphorylation de c-Met et de VEGFR-2. Il réprime également puissamment la croissance des cellules tumorales amplifiées en c-Met et des cellules endothéliales stimulées par le HGF ou le VEGF. Ce composé contourne la résistance à tous les EGFR-TKIs réversibles, irréversibles et sélectifs des mutants induite par le HGF exogène et/ou endogène dans les lignées cellulaires de cancer du poumon mutantes EGFR, en bloquant la voie Met/Gab1/PI3K/Akt in vitro. Il prévient également l'émergence de cellules HCC827 résistantes au géfitinib induite par une exposition continue au HGF.
|
| Essai kinase |
Analyse par Western blot
|
|
Le statut de phosphorylation de c-Met et VEGFR-2 est détecté par analyse Western blot. Pour c-Met, les cellules MKN45 sont incubées avec une dilution en série de Golvatinib (E7050) dans un milieu complet à 37 °C pendant 2 h. Pour VEGFR-2, les HUVEC sont privées de sérum dans un milieu sans sérum endothélial humain contenant 0,5 % de FBS pendant 24 h. Ensuite, les HUVEC sont incubées avec une dilution en série de ce composé pendant 1 h, puis incubées avec 20 ng/mL de VEGF humain pendant 5 min. Les cellules sont lysées par un tampon de lyse (50 mM HEPES [pH 7,4], 150 mM NaCl, 10 % glycérol, 1 % Triton X-100, 1,5 mM MgCl2, 1 mM EDTA [pH 8,0], 100 mM NaF, 1 mM phénylméthylsulfonylfluorure, 1 mM orthovanadate de sodium, 10 μg/mL aprotinine, 50 μg/mL leupeptine et 1 μg/mL pepstatine A). Les échantillons tumoraux réséqués sont homogénéisés avec un tampon de lyse contenant 25 mM de β-glycérophosphate et 0,5 % (v/v) de cocktail inhibiteur de phosphatase 2 à 4 °C. Les débris cellulaires sont éliminés par centrifugation à 17 860 g pendant 20 min à 4 °C. Des aliquotes des surnageants contenant 5-20 μg de protéines sont soumises à une SDS-PAGE dans des conditions réductrices. Les protéines sont ensuite transférées sur des membranes PVDF, bloquées avec du TBS contenant 0,05 % de Tween-20 et soit 5 % de lait écrémé, soit 5 % de BSA. Les membranes sont sondées avec les anticorps suivants : anticorps polyclonal anti-c-Met (C-28) et anticorps polyclonal anti-VEGFR-2 (C-20) ; anticorps monoclonal anti-phosphotyrosine clone 4G10 ; et anticorps polyclonal anti-VEGFR-2, anticorps polyclonal anti-phospho-VEGFR-2 (Tyr996) et anticorps polyclonal anti-phospho-c-Met (Tyr1234/1235). La détection est réalisée à l'aide d'un kit de chimiluminescence amélioré Super Signal. Les bandes immunoréactives sont visualisées par chimiluminescence avec un système de détection Image Master-VDS-CL. L'intensité de chaque bande est mesurée à l'aide d'un analyseur d'images.
|
|
| In vivo |
Le Golvatinib (E7050) montre une inhibition de la phosphorylation de c-Met et VEGFR-2 dans les tumeurs in vivo, avec une forte suppression de la croissance tumorale et de l'angiogenèse dans les modèles de xénogreffes. Le traitement de certaines lignées tumorales contenant des amplifications de c-Met avec des doses élevées de ce composé (50–200 mg/kg) induit une régression tumorale et une disparition. Dans un modèle de dissémination péritonéale, il démontre un effet antitumoral contre les tumeurs péritonéales ainsi qu'une prolongation significative de la durée de vie chez les souris traitées. Dans une autre étude de xénogreffe, les tumeurs produites par des cellules Ma-1 transfectées par le HGF (Ma-1/HGF) sont plus angiogéniques que les tumeurs du groupe témoin vectoriel et montrent une résistance au ZD1839. L'E7050 seul inhibe l'angiogenèse et retarde la croissance des tumeurs Ma-1/HGF, et lorsqu'il est combiné au ZD1839, il induit une régression marquée de la croissance tumorale.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT01355302 | Terminated | Advanced or Metastatic Solid Tumors|Previously Untreated Gastric Cancer |
Eisai Inc.|Quintiles Inc. |
November 2011 | Phase 1|Phase 2 |
| NCT01433991 | Terminated | Advanced Solid Tumors |
Eisai Inc. |
October 13 2011 | Phase 1|Phase 2 |
| NCT01332266 | Completed | Platinum-Resistant Squamous Cell Carcinoma of the Head and Neck |
Eisai Inc.|PharmaBio Development Inc. |
September 19 2011 | Phase 1|Phase 2 |
| NCT01271504 | Completed | Hepatocellular Carcinoma |
Eisai Inc.|PharmaBio Development Inc. |
July 19 2011 | Phase 1|Phase 2 |
| NCT02533102 | Completed | Healthy Subjects |
Eisai Limited|Eisai Inc. |
November 2010 | Phase 1 |
| NCT00921869 | Completed | Solid Tumors |
Eisai Co. Ltd.|Eisai Inc. |
October 2009 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
