pour la recherche uniquement
Nazartinib (EGF816) EGFR inhibiteur
Réf. CatalogueS7824
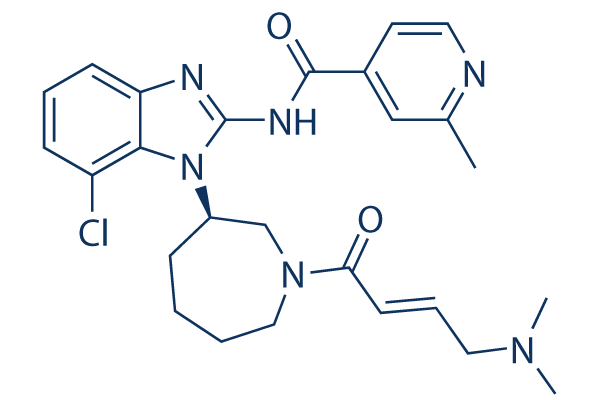
Structure chimique
Poids moléculaire: 495.02
Contrôle Qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- SDS
- Fiche technique
| Cibles apparentées | VEGFR JAK PDGFR FGFR Src HIF FLT FLT3 HER2 Bcr-Abl |
|---|---|
| Autre EGFR Inhibiteurs | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-490 AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 495.02 | Formule | C26H31ClN6O2 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1508250-71-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | NVS-816 | Smiles | CC1=NC=CC(=C1)C(=O)NC2=NC3=C(N2C4CCCCN(C4)C(=O)C=CCN(C)C)C(=CC=C3)Cl | ||
Solubilité
|
In vitro |
DMSO
: 99 mg/mL
(199.99 mM)
Ethanol : 99 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
mutant EGFR
0.031 μM(Ki)
|
|---|---|
| In vitro |
Le Nazartinib (EGF816) est un nouvel inhibiteur covalent de l'EGFR, sélectif des mutants, avec une activité presque équipotente sur les mutations oncogéniques (L858R et ex19del) et résistantes au T790M, et une bonne sélectivité par rapport à l'EGFR WT. Il inhibe puissamment les mutations EGFR les plus courantes, L858R, Ex19del et T790M in vitro. L'activité cellulaire de ce composé sur les mutants EGFR est évaluée à l'aide de trois lignées cellulaires bien caractérisées, H3255, HCC827 et H1975, qui hébergent respectivement les mutations L858R, Ex19del et L858R/T790M. Après incubation avec les cellules pendant 3 heures, il montre une inhibition puissante des niveaux de pEGFR dans H3255, HCC827 et H1975 avec des valeurs d'EC50 de 5, 1 et 3 nmol/L, respectivement. Les essais cellulaires montrent que l'EGF816 est sélectif envers les mutants par rapport à l'EGFR WT.
|
| In vivo |
Le Nazartinib (EGF816) est bien toléré et possède des propriétés physico-chimiques favorables et une bonne biodisponibilité orale chez la souris. Il présente un volume de distribution modéré et une clairance faible à modérée chez les rongeurs (30 % et 35 % du débit sanguin hépatique du rat et de la souris, respectivement). Chez le chien, ce composé présente une clairance élevée et un volume de distribution élevé. Il démontre également une activité antitumorale dans un modèle de mutant par insertion de l'exon 20. À des niveaux supérieurs aux doses efficaces, son traitement entraîne une inhibition minimale de l'EGFR WT et est bien toléré. Dans les études à dose unique, il procure une inhibition soutenue de la phosphorylation de l'EGFR, ce qui est cohérent avec sa capacité de liaison irréversible. Ce composé a une demi-vie plus longue chez l'homme que chez la souris et est actuellement évalué dans des essais cliniques de phase I/II chez des patients porteurs de mutations EGFR, y compris T790M.
|
Références |
|
Informations sur lessai clinique
(données du https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Promoteur/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT03529084 | Withdrawn | Carcinoma Non-small Cell Lung |
Novartis Pharmaceuticals|Novartis |
July 24 2018 | Phase 3 |
| NCT03516214 | Completed | Bronchial Neoplasms |
University of Cologne |
April 25 2018 | Phase 1 |
| NCT03292133 | Active not recruiting | Lung Cancer |
Massachusetts General Hospital|Novartis |
October 31 2017 | Phase 2 |
| NCT02323126 | Terminated | Non Small Cell Lung Cancer |
Novartis Pharmaceuticals|Novartis |
February 9 2015 | Phase 2 |
| NCT02335944 | Terminated | Non Small Cell Lung Cancer |
Novartis Pharmaceuticals|Novartis |
January 13 2015 | Phase 1|Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
