pour la recherche uniquement
NU7026 DNA-PK inhibiteur
Réf. CatalogueS2893
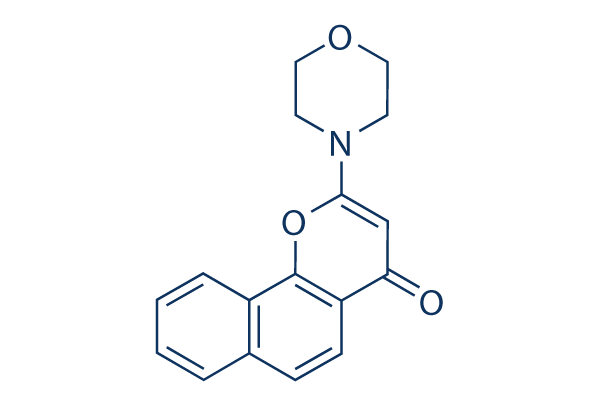
Structure chimique
Poids moléculaire: 281.31
Contrôle Qualité
| Cibles apparentées | HDAC PARP ATM/ATR WRN DNA/RNA Synthesis Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Autre DNA-PK Inhibiteurs | Nedisertib (M3814) AZD7648 NU7441 (KU-57788) KU-0060648 VX-984 CC-115 YU238259 LTURM34 Compound 401 |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| HeLa cells | Function assay | Inhibition of DNA dependent protein kinase isolated from HeLa cells, IC50=0.23 μM | 15658870 | |||
| HeLa cells | Function assay | Inhibition of mTOR protein isolated from HeLa cells, IC50=6.4 μM | 15658870 | |||
| HeLa | Function assay | In vitro inhibition of DNA-dependent protein kinase(DNA-PK) from HeLa (human carcinoma) cells, IC50=0.23μM | 12941339 | |||
| Cliquez pour voir plus de données expérimentales sur la lignée cellulaire | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 281.31 | Formule | C17H15NO3 |
Stockage (À compter de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 154447-35-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | LY293646 | Smiles | C1COCCN1C2=CC(=O)C3=C(O2)C4=CC=CC=C4C=C3 | ||
Solubilité
|
In vitro |
4-Methylpyridine : 5 mg/mL
DMSO
: 1 mg/mL
(3.55 mM)
Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Saisir les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Saisir la formulation in vivo (Ceci est seulement le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouterμL PEG300, mélanger et clarifier, puis ajouterμL Tween 80, mélanger et clarifier, puis ajouter μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, puis ajouter μL Huile de maïs, mélanger et clarifier.
Note : 1. Veuillez vous assurer que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue, lors de lajout précédent, est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie chaud peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
DNA-PK
(Cell-free assay) 0.23 μM
PI3K
(Cell-free assay) 13 μM
|
|---|---|
| In vitro |
NU7026 potentialise la cytotoxicité induite par les rayonnements ionisants de manière concentration-dépendante dans les cellules V3YAC et PARP-1+/+. Ce composé abolit complètement la récupération des dommages potentiellement létaux dans les cellules dont la croissance est arrêtée. Il inhibe la réparation des DSB de l'ADN de 56 % dans la lignée cellulaire V3YAC. Cette substance chimique (10 μM) potentialise les effets inhibiteurs de croissance de la doxorubicine, du mAMSA avec des valeurs de PF50 allant d'environ 19 pour le mAMSA à environ 2 dans les cellules K562. Elle (10 μM) potentialise également l'effet inhibiteur de croissance dans cette lignée cellulaire de leucémie avec une valeur de PF50 de 10,53. Ce composé (10 μM) améliore le blocage du cycle cellulaire en G2 induit par dans les cellules K562. Il potentialise les poisons de la topo II impliquant l'inhibition de la jonction d'extrémité non homologue et un arrêt au point de contrôle G2/M. Une exposition de 4 h à ce composé (10 μM) en combinaison avec 3 Gy de rayonnement est nécessaire pour un effet de radiosensibilisation significatif dans les cellules de cancer de l'ovaire humain CH1. Il (< 10 μM) a une activité cytotoxique synergique à des doses non toxiques de cette substance chimique dans une lignée cellulaire de LLC (I83) et dans des lymphocytes de LLC primaires. Ce composé (10 μM) augmente l'arrêt G(2)/M induit par dans les cellules I83. Il (10 μM) améliore le γH2AX induit par tout au long du cycle cellulaire dans la lignée cellulaire I83. Cette substance chimique (10 μM) augmente l'apoptose induite par dans la lignée cellulaire I83. Il (55 μM) entraîne une induction dramatique de la fusion des télomères dans les MEF p53 nuls et significativement moins de fusions des télomères dans les MEF doubles nuls p53 et ligase IV. |
| Essai kinase |
Test de kinase recombinante
|
|
La DNA-PK mammifère (500 ng/μL) est isolée à partir d'un extrait nucléaire de cellules HeLa après chromatographie utilisant Q-Sepharose, S-Sepharose et Hépérine-agarose. L'activité de la DNA-PK (250 ng) est mesurée à 30℃, dans un volume final de 40 μL, dans un tampon contenant 25 mM HEPES (pH 7,4), 12,5 mM MgCl2, 50 mM KCl, 1 mM DTT, 10 % v/v Glycérol, 0,1 % p/v NP-40, et 1 mg du substrat GST-p53N66 dans des plaques à 96 puits en polypropylène. Au mélange d'essai, diverses concentrations de ce composé (dans du DMSO à une concentration finale de 1 % v/v) sont ajoutées. Après 10 minutes d'incubation, de l'ATP est ajouté pour donner une concentration finale de 50 μM, avec un oligonucléotide d'ADN double brin de 30-mer (concentration finale de 0,5 ng/mL), pour initier la réaction. Après 1 heure d'agitation, 150 μL de PBS sont ajoutés à la réaction, et 5 μL sont ensuite transférés dans une plaque blanche opaque à 96 puits contenant 45 μL de PBS par puits, où le substrat GSTp53N66 est laissé se lier aux puits pendant 1 heure. Les IC50 des composés dans tous les essais enzymatiques sont dérivés de tracés sigmoïdaux utilisant le progiciel graphique Prism, dans lequel l'activité enzymatique dans les concentrations variables de composés est tracée par rapport à la concentration du composé.
|
|
| In vivo |
NU7026 (20 mg/kg, i.v.) subit une clairance plasmatique rapide (0,108/heure) chez la souris, ce qui est largement attribué à un métabolisme étendu. La biodisponibilité après administration intrapéritonéale (i.p.) et p.o. de ce composé à une dose de 20 mg/kg est de 20 et 15 %, respectivement. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | pDNA-PKcs S2056 / DNA-PKcs |

|
22131882 |
| Growth inhibition assay | Cell viability |
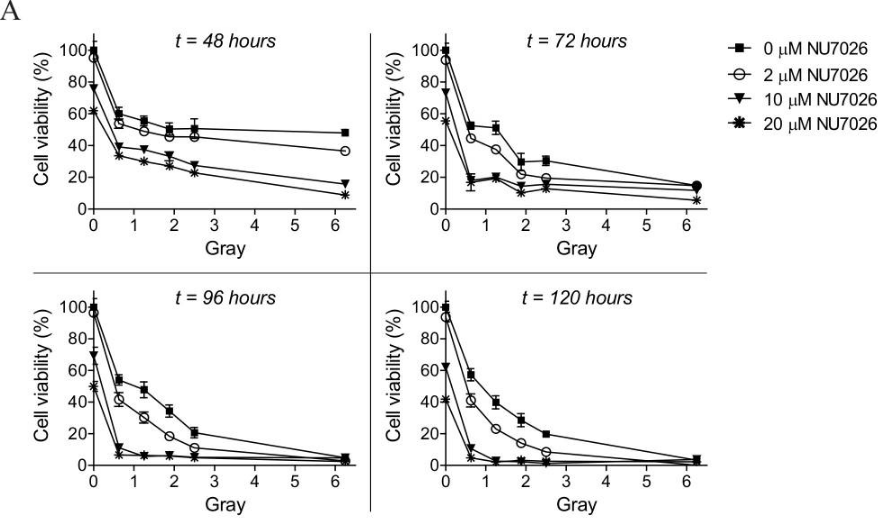
|
26716839 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
